肥胖合并炎症性肠病(IBD)的患者往往更难实现黏膜愈合,但“脂肪组织如何远程拖慢肠道修复”一直缺乏清晰机制。
2026年,四川大学华西医院陈海洋教授团队在《Nature Metabolism》(IF=20.8)正式发表题为”Obesity impairs gut repair via AFABP-mediated iron overload in intestinal stem cells“的突破性研究。
该研究发现:肥胖时脂肪细胞分泌的脂肪细胞脂肪酸结合蛋白(AFABP/FABP4,adipocyte fatty acid–binding protein)会结合血浆转铁蛋白(Transferrin,TSF),造成肠干细胞铁过载,进而压制损伤修复期必需的PPARα-过氧化物酶体提升,最终卡住干细胞分化与上皮再生。更重要的是,研究者用Cre依赖AAV在脂肪组织中“定点”提高AFABP,直接把相关表型在瘦鼠身上复现,为“脂肪-肠道”器官间通讯提供了强有力的因果证据。
本文将为您深度拆解这篇高分研究中的3个核心科学问题与技术高光。

核心问题 1:肥胖肠道修复慢,问题出在增殖还是分化?
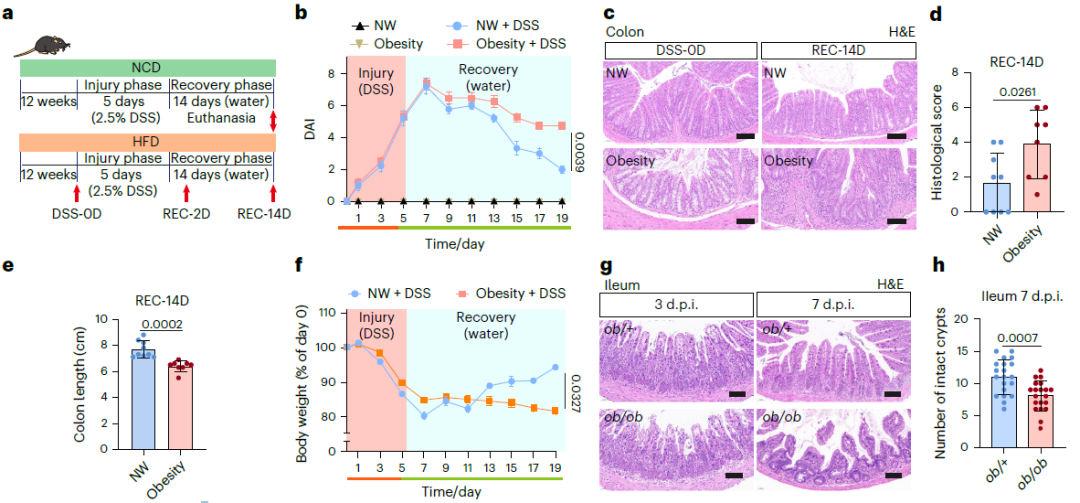
研究团队首先建立了高脂饮食(HFD)诱导的肥胖小鼠模型,并通过 DSS(硫酸葡聚糖钠)诱导结肠炎模拟肠道损伤。结果显示,肥胖小鼠在损伤急性期(DSS-5D)与正常体重小鼠无明显差异,但在恢复期(REC-14D)出现显著缺陷:疾病活动指数(DAI)更高、结肠长度更短、组织学评分更差。
更重要的是,通过 Lgr5 谱系示踪技术发现,肥胖小鼠的肠道干细胞(ISCs)虽然能正常增殖,但分化受阻——表现为未成熟细胞(SOX9+)堆积和成熟上皮细胞(Muc2+)减少。这一表型在 ob/ob 基因缺陷肥胖小鼠和果蝇模型中得到一致性验证,提示这是跨物种保守的病理现象。
核心问题 2:是肠道本身病变,还是脂肪组织在“远程发号施令”?
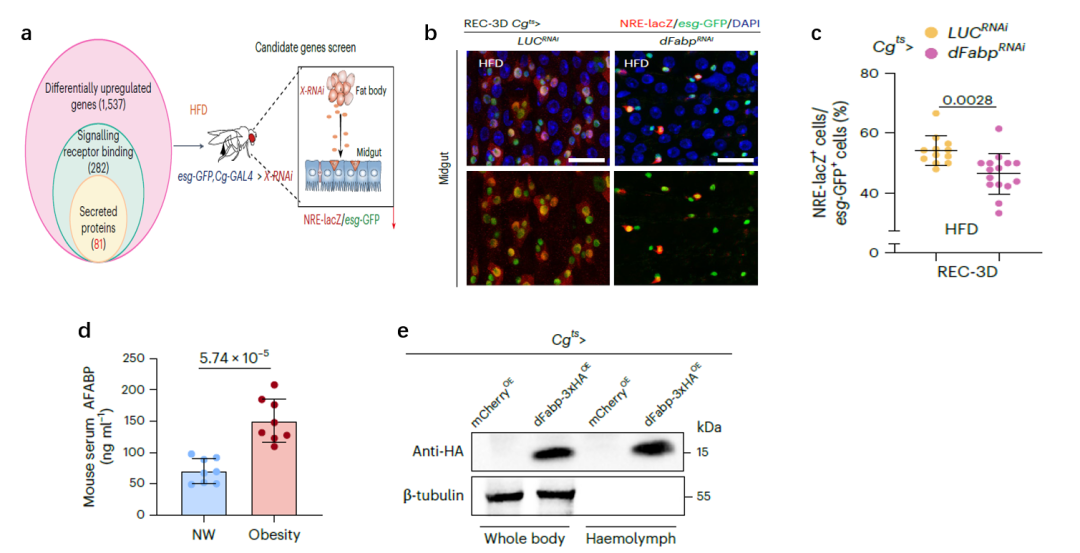
既然损伤发生在肠道,问题是否出在肠道本身?研究团队通过 RNA-seq 分析肠隐窝转录组,结合果蝇脂肪体(fat body,相当于人类脂肪组织)分泌蛋白筛选,锁定了一个关键脂肪因子——AFABP(脂肪细胞脂肪酸结合蛋白)。肥胖小鼠血清 AFABP 水平显著升高,且与肠道修复能力呈负相关。有趣的是,AFABP 在肠道上皮细胞中几乎不表达,说明这是一个脂肪组织向肠道”远程发号施令”的内分泌过程。
技术高光:AAV精准定点表达,证实AFABP的关键驱动作用
为了严格验证 AFABP 的因果作用,研究团队采用了Cre-lox 依赖的 AAV 基因递送系统(AAV-DIO/FLEX)来进行在体因果验证(注:本研究中高滴度、高特异性的AAV载体构建与病毒包装服务由派真生物 PackGene 提供支持)。
通过将装载有mAFABP表达盒的AAV注射入Adipoq-Cre小鼠腹腔,研究者成功实现了脂肪细胞特异性的AFABP过表达。该遗传学模型产生了惊人的表型:即使小鼠处于正常饮食和体重(非肥胖状态),单纯的AFABP升高就足以重现肥胖相关的肠道修复 缺陷——DSS后体重恢复缓慢、DAI评分持续偏高、炎症细胞浸润加剧。
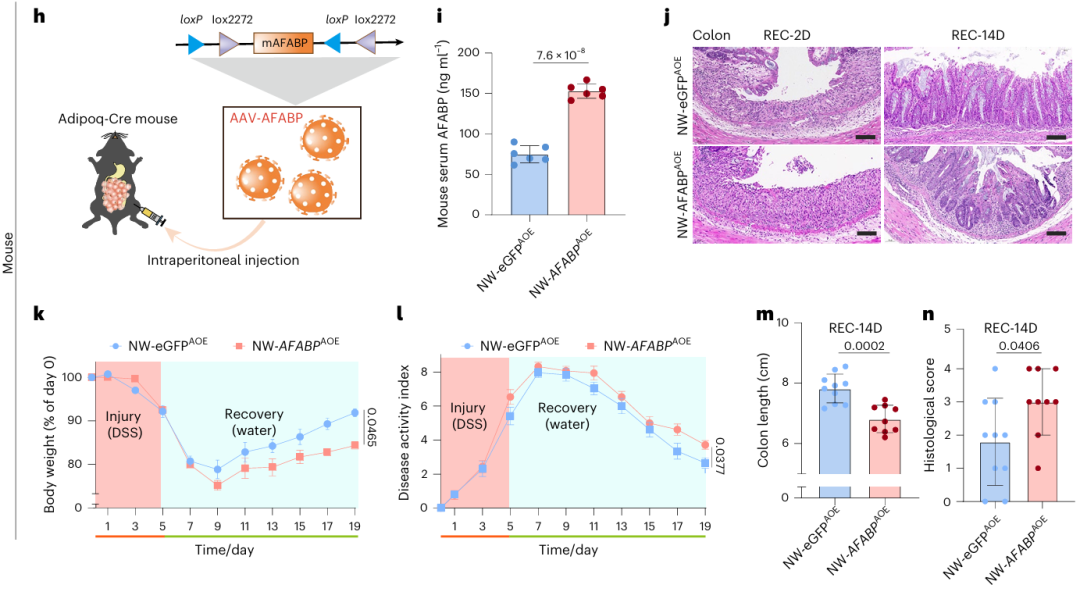
反之,当使用Adipoq-Cre驱动脂肪特异性敲除(AFABPAKO),或用AFABP小分子抑制剂BMS309403处理肥胖小鼠时,肠道再生能力得到显著恢复。这一正一反的强因果证据,彻底夯实了AFABP的核心致病地位。
本研究中的AAV体内递送关键参数
- 表达基因: mAFABP(小鼠脂肪酸结合蛋白)及 eGFP(对照)
- 靶向策略:结合 Adipoq-Cre 雄性小鼠实现脂肪细胞特异性表达
- 注射途径与剂量:腹腔注射(i.p.),1.5×10¹² vg / 只
- 观察周期:注射后维持普通饲料喂养9周,血清ELISA确证高表达后,进入DSS诱导结肠炎实验。
核心问题 3:AFABP如何跨器官引发肠干细胞“铁过载”?能否被药物逆转?
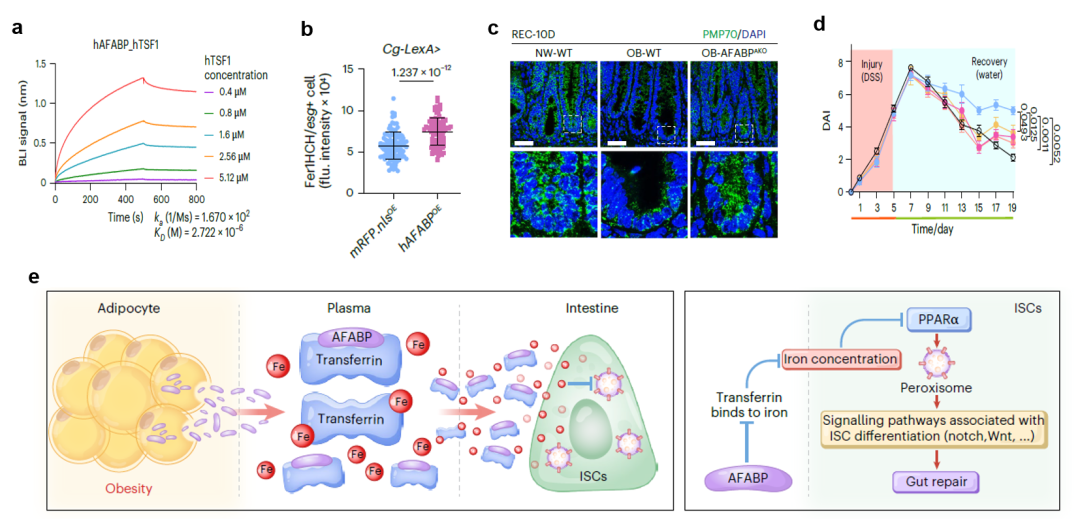
AFABP 如何远程遥控肠道干细胞?通过免疫共沉淀-质谱(IP-MS)和生物层干涉技术(BLI),研究团队发现了完整的分子级联反应。
1. 劫持铁转运: 循环升高的AFABP 与血浆转铁蛋白(Transferrin, TSF)直接结合(解离常数 KD为 2.7×10⁻⁶ M),干扰了 Transferrin 的铁转运功能;
2. 引发铁过载:导致血清非转铁蛋白结合铁(NTBI)升高,引发肠干细胞内铁过载(Fer1HCH 报告基因和 FTH1 免疫组化证实);
3. 过氧化物酶体(peroxisome)功能抑制:铁过载抑制 PPARα 信号,导致损伤后过氧化物酶体标志物 PMP70、ACOX1 及过氧化氢酶(catalase)活性显著下降;
4. 分化信号失衡:铁过载进一步扰乱损伤修复期隐窝内Wnt/Notch等分化相关信号平衡(Notch下降、Wnt偏高),最终阻断成熟上皮分化。
基于这一清晰的AFABP-Transferrin-铁-过氧化物酶体轴,研究者测试了多维度治疗策略:无论是使用铁螯合剂DFO,还是过氧化物酶体/PPAR激活剂(如非诺贝特、NaPB或吡格列酮),均可有效逆转肥胖小鼠的肠道修复缺陷。
总结与转化意义
本研究不仅阐明了肥胖损害肠道修复的分子机制,更为研究器官间代谢通讯(Adipose-gut axis)提供了极具参考价值的范式。对于基因治疗与转化医学领域而言,该研究证实了靶向抑制脂肪组织AFABP或干预下游铁代谢/PPARα通路,是治疗肥胖相关炎症性肠病(IBD)的极具潜力的可成药策略。
文章用到AAV病毒的相关参数和详情

派真生物(PackGene)十分荣幸能够为陈海洋教授团队的这项突破性研究提供专业的质粒构建与AAV病毒包装服务,助力科学家利用AAV-DIO系统精准实现脂肪组织特异性基因表达验证,规避了传统转基因小鼠周期长或全身表达的局限。我们将持续为代谢与基因治疗领域的创新研究提供高质量、高滴度的底层载体技术支持!
参考资料
Liu Z, Chen Y, Yan J, et al. Obesity impairs gut repair via AFABP-mediated iron overload in intestinal stem cells. Nat Metab. 2025. DOI: 10.1038/s42255-025-01425-4
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。