服务优势
-
快速交付
1E+13 GC以内可在6天交付 -
高纯度
AAV纯度95%以上,SDS-PAGE 验证 -
低内毒素
<10 EU/mL,可直接用于体内实验 -
低空壳率
空壳率<30% -
血清型丰富
100+血清型任您选择 -
专业支持
PhD 级 AAV 专家全程护航
服务明细
周期
若插入片段超过包装容量 (4.7 kb),或者要求使用您提供的 rep/cap 质粒或辅助质粒,我们无法保证最终产量或滴度。
| 服务类别 | 规模 (GC) | 交付周期 |
|---|---|---|
| Fast mode(极速模式) | ≤1E13GC | 6个自然日 |
| >1E13GC | 7个自然日 | |
| Normal mode(常规模式) | ≤1E+14 GC | 14个自然日 |
| >1E14GC | 咨询 | |
| Slow mode(休闲模式) | ≤1E+14 GC | 21个自然日 |
| >1E14GC | 咨询 |
- GC = 基因组拷贝数。
- 对于一些没有生产数据的极低产量 AAV 血清型,我们无法保证最终产量或滴度。
- 如果您想使用目前处于专利保护期内或正在申请专利的任何 AAV 血清型,并且您将用于商业用途,我们建议您提前联系专利所有者以获得授权。
关于Fast mode的说明:
- 如需挑单克隆或者特殊内毒素需求,周期需额外评估。
储存条件:
- 将病毒储存在 -80°C冰箱,并在操作过程中将其置于冰上。
- 建议对使用量提前进行预估,出货时按照预定的分装要求进行分装,避免收到货后再次冻融分装影响滴度准确性。如需再次分装使用,推荐使用内壁硅化程度良好的PCR管,或者低蛋白结合率的病毒专用保存管。
- 如需稀释AAV病毒,请将病毒置于冰浴融解后,使用Tris缓冲液或PBS缓冲液稀释。
质量控制
派真生物凭借完善的质量控制(QC)体系,为 AAV 相关研究提供可靠保障。我们的 QC 团队基于多年经验,开发出一系列精准的 AAV 检测方法,全面检测 AAV 病毒颗粒的鉴别、纯度与效力,适用于体外及体内试验。
我们承诺,所交付的 AAV 病毒内毒素水平严格控制在低于 10 EU/mL的范围内。此外,我们还提供 ddPCR、透射电子显微镜(TEM)观察、半数细胞感染量(TCID50)等在内的多项附加 QC 测试服务。如需深入了解 AAV 分析服务详情,可点击查阅 AAV 分析服务板块。
| 类别 | 检测项目 | 备注 |
|---|---|---|
| 鉴别 | GOI 测序 | 可选QC |
| 纯度 | SDS-PAGE 考染 | 免费QC |
| TEM | 可选QC | |
| AUC | 可选QC | |
| 效价 & 含量 | qPCR | 免费QC |
| ddPCR | 可选QC | |
| TCID50 | 可选QC | |
| 衣壳滴度-ELISA | 可选QC | |
| 杂质 | 内毒素检测 | 免费QC |
| 支原体检测 | 可选QC | |
| 无菌检测 | 可选QC | |
| 残留质粒检测 | 可选QC |
产品性能
-
常规质控
- 使用多重核酸内切酶进行限制性酶切分析,以验证用于 AAV 包装的质粒
-
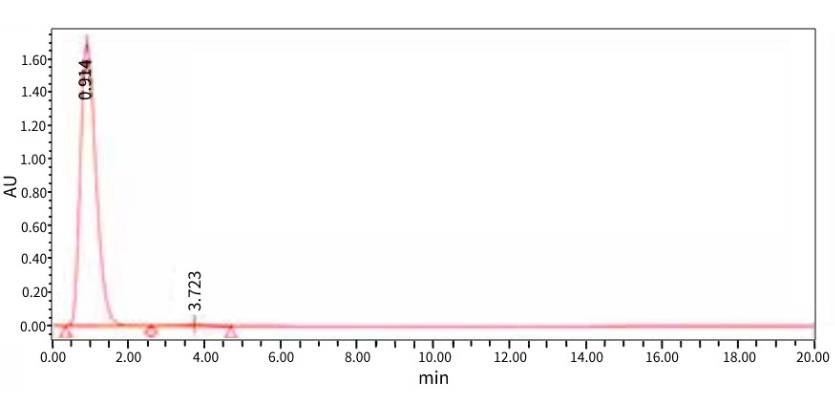
AAV滴度检测,SYBR Green qPCR标准曲线精确定量
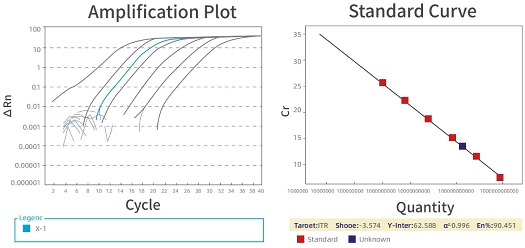
- 通过 LAL 分析进行内毒素检测
- AAV纯度检测,SDS-PAGE电泳与考马斯亮蓝染色确定纯度(可根据要求提供银染)
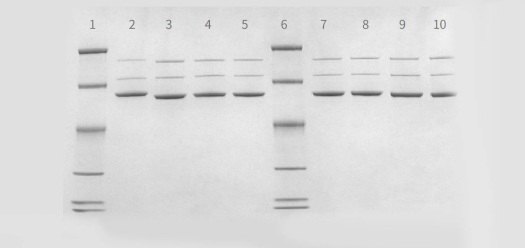
图注: 泳道2-5和7-10为派真生产的AAV 样品,泳道1和6为 Marker -
其他质控