
2023年7月10日,日本制药公司Astellas(安斯泰来)与4D Molecular Therapeutics(简称“4DMT”)宣布已签署一项合作协议,安斯泰来将使用4DMT公司的视网膜靶向的AAV载体R100,开发针对单基因遗传眼病的基因疗法,这笔合作交易总额高达9.62 亿美元。
4D Molecular Therapeutics(4DMT)是一家基于AAV定向进化及精确靶向技术的基因药物开发公司,是临床阶段基因治疗药物研发领域的领导者。基于传统AAV载体存在的挑战,4D Molecular建立了治疗载体进化平台,这一平台支持针对疾病特异性进行产品发现、设计和开发,为特定的组织和疾病定制专有载体。
目前,4D Molecular已从37个专有和多样化的载体库中评估了超过10亿个载体衣壳序列,并对其进行筛选,确定最佳靶向载体,有望克服传统载体存在的挑战。
基于专有的技术平台,4D Molecular围绕着眼科、心脏病、肺病三大疾病领域建立了5大研发管线,并均已进入临床。
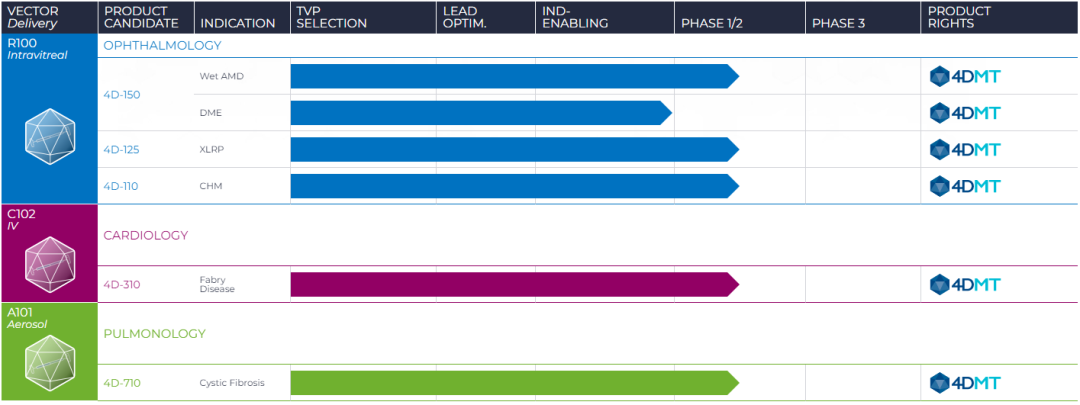
▲ 在研管线(图片来源:4DMT官网)
4D-125是一种能够通过玻璃体内注射的AAV基因疗法,旨在利用R100载体将RPGR基因的功能拷贝传递至视网膜中的感光细胞,用于治疗X连锁性视网膜色素变性(XLRP)。目前,该疗法正处于1/2期临床试验。
4D-710是由进化载体A101和密码子优化的CFTR∆R转基因组成,设计用于气溶胶输送以实现肺气道上皮细胞内的CFTR表达,用于治疗囊性纤维化患者。2022年11月,4D Molecular宣布了4D-710的1/2 期临床试验的中期数据:在3名接受治疗的患者中观察到4D-710 CFTR∆R转基因100%表达,候选药物整体耐受性良好。
4D-310是由C102衣壳携带表达AGA的GLA基因,其中C102衣壳经过特定优化,提高了转染心肌细胞的能力,可通过静脉输注用于治疗心肌疾病。2021年10月公布的首个人体试验显示,三名接受治疗的患者体内关键的α-半乳糖苷酶A(AGA)的活性提高到接近或显著高于正常水平。
4D-110是一类通过玻璃体腔注射治疗无脉络膜症(CHM)的候选药物,优化的AAV载体能够将CHM基因的功能拷贝靶向递送至视网膜。其1期临床试验数据表明了该候选药物具有治疗CHM的较优潜力。
4D Molecular处于临床阶段的候选管线均展示了良好的临床疗效和安全性,证明了其专有的AAV技术平台的卓越性。同时,该企业多条管线并行推进,整体进展可圈可点。未来,随着技术的改进,AAV载体将会被进一步优化,加之工程化手段的改进,相信基因疗法将会朝着更加安全的方向发展。
资料来源:
1.https://4dmoleculartherapeutics.com/
2.https://mp.weixin.qq.com/s/w9BajGdyMOpATnAgo9Wvmg
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。

