
ACDN-01是有史以来第一个临床阶段的RNA外显子编辑疗法,也是唯一针对Stargardt病遗传病因的临床阶段疗法。Ascidian预计于2024年上半年启动ACDN-01治疗Stargardt病和其他ABCA4视网膜病的1/2期STELLAR研究的患者招募。

“FDA是第一个批准ACDN-01进行临床开发的监管机构,这对Ascidian和更广泛的RNA编辑领域来说是一个重要里程碑。” Ascidian Therapeutics总裁兼临时首席执行官博士Michael Ehlers说,“我们选择首先去FDA提交申请,是出于对我们数据的严谨性的信任。并且Ascidian通过编辑RNA而不是DNA,这有着独特的优势,很可能改变Stargardt病患者的生活,从广义上讲,也有可能显著扩大基因医学的范围。”
STELLAR是一项开放标签的1/2期试验,将评估单剂量ACDN-01的安全性和有效性,该剂量通过视网膜下注射给Stargardt病和其他ABCA4视网膜病患者。
关于Stargardt病和 ACDN-01
Stargardt病是最常见的遗传性黄斑变性,起因于ABCA4基因的变异。这些变异引发渐进性视网膜退化和视力损害,通常从儿童期或青少年早期开始。已知ABCA4基因有超过1000种变异导致Stargardt病。由ABCA4功能丧失引起的疾病,由于基因庞大或基因突变的显著多样性而无法通过常规基因替换或单碱基编辑解决。
ACDN-01是一种由单个载体传递的体内RNA外显子编辑疗法。它已在非人灵长类动物视网膜中展示了高效、持久的体内RNA外显子编辑,并在人类视网膜外植体中展示了离体RNA外显子编辑。
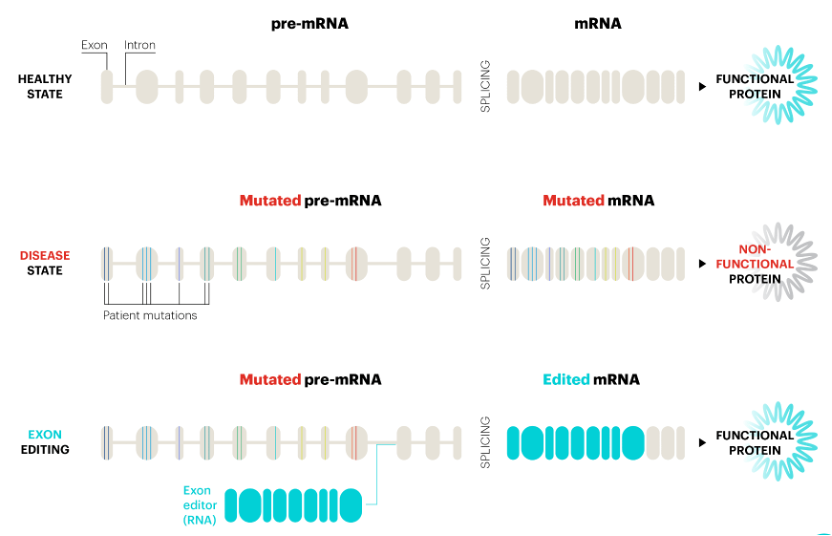
▲RNA外显子编辑疗法的作用机制(图源:Ascidian Therapeutics官网)
资料来源:
1.https://www.prnewswire.com/news-releases/ascidian-therapeutics-announces-first-ever-ind-for-an-rna-exon-editor-as-fda-approves-trial-plan-and-fast-tracks-acdn-01-in-stargardt-disease-and-other-abca4-retinopathies-302046287.html
2.https://mp.weixin.qq.com/s/JJzgSt7gn1i5rFKd2BjeOw
3.https://mp.weixin.qq.com/s/-yUa07WfAWL5ddj98zTphg
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。

