慢病毒载体,作为基因治疗和细胞工程中的一把锋利工具,其结构和设计背后的科学原理为现代医疗研究带来了突破。慢病毒载体的设计融合了分子生物学、遗传学和病毒学的先进概念,在实现安全有效的基因传递上扮演着重要角色。
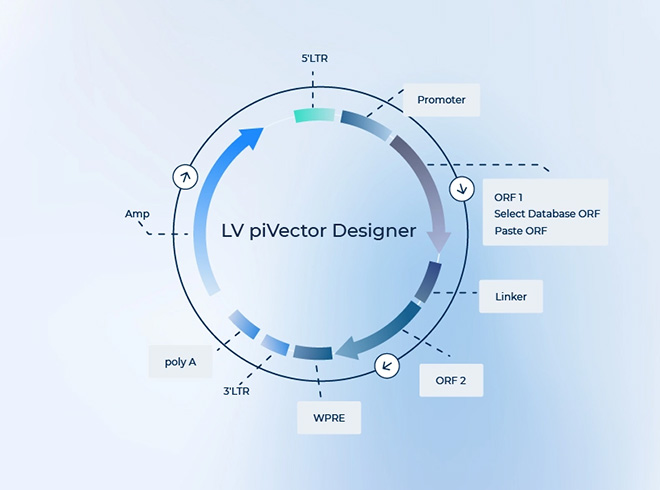
慢病毒载体的结构通常由几个关键组成部分构成:
包装信号(Ψ):这是载体中必不可少的序列,它确保病毒RNA被正确地打包进病毒粒子中。
逆转录酶编码序列:这个序列使得病毒能够在宿主细胞内部通过逆转录过程将其RNA基因组转换成DNA。
长末端重复序列(LTRs):位于病毒基因组的两端,它们在整合进宿主细胞基因组中时非常关键,并参与病毒转录的调控。
助病毒系统:为了提高安全性,慢病毒载体缺少必要的病毒蛋白质编码基因。这意味着它们在独立复制时是不完整的。制作载体病毒粒子时需要提供这些缺失的蛋白,通常在宿主细胞中利用所谓的助病毒(helper virus)或者转染助病毒质粒来补充。
在设计慢病毒载体时,科学家还必须考虑宿主范围(即病毒可以感染的细胞类型)以及靶细胞的特异性。通过改造病毒外壳蛋白(Env),可以增强载体对特定细胞类型的亲和力,这是通过选择或工程化特定的病毒外壳蛋白亚型来实现的。
为了确保病毒载体在宿主细胞中的基因表达是受控的,科学家们还会引入内部启动子和增强子元件,以调节目标基因的表达水平和稳定性。此外,转基因的精确整合位置采用基因组编辑技术如CRISPR/Cas9可以大大提高安全性和减少整合导致的宿主基因组不稳定性。
总体而言,通过对慢病毒载体结构和设计的深入研究,生物技术专业人员能够更精确地操纵基因,为治疗多种遗传性和获得性疾病提供了新的希望和可能性。随着对慢病毒载体理解的不断深入,我们有理由相信,基因治疗的安全性和效果都将得到极大提升。