
ITR基本结构
AAV2 ITR是使用最广泛的,其可以与各种血清型兼容,ITR的Flip构型与3’端靠近的位置为B-B’回文结构,而Flop构型与3’端靠近的位置为C-C’回文结构。AAV基因组两端可以均为Flip构型的ITR,也可以均为Flop构型的ITR,或者一端为Flip构型的ITR,另一端为Flop构型的ITR。ITR的D序列在基因组的两端各出现一次,保持单链状态。ITR的A-A’部分包含末端分辨位点(trs)和Rep结合元件(RBE),trs作为复制的起始位点,Rep结合元件(RBE)是AAV Rep78和Rep68蛋白结合的位置,RBE由一个四核苷酸重复序列(5’-GNGC-3’)组成。ITR的T形结构顶点对应一个额外的RBE (RBE’),它可以稳定Rep78和Rep68蛋白与ITR之间的结合。据报道,两端ITR都是145 bp或130 bp版本的GOI质粒在AAV病毒产量及生物活性方面相似,因此这两个版本均被称为野生型。ITR结构详见Figure1~3:
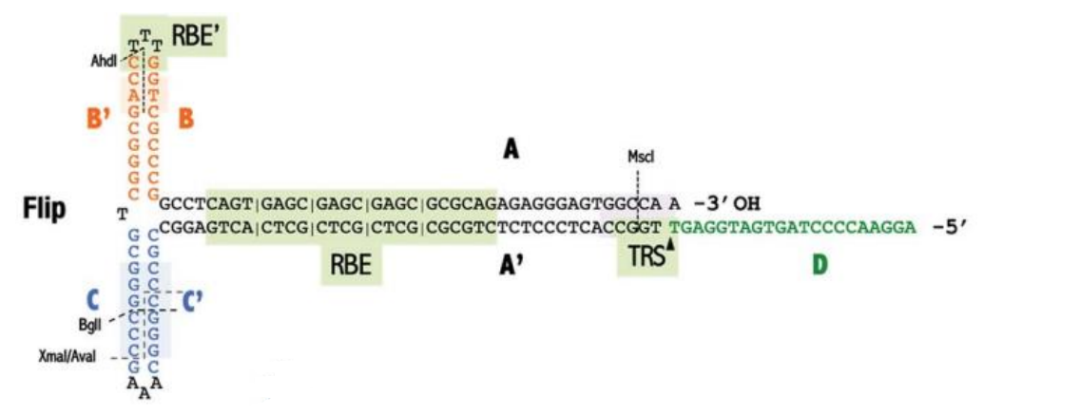
Figure1: AAV2 ITR (Flip, 145 nt)

Figure2: AAV2 ITR (Flop, 145 nt)
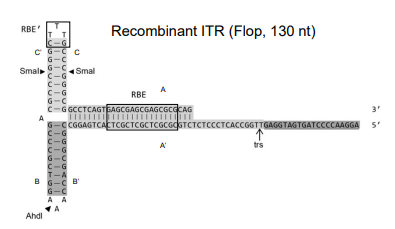
Figure3: Recombinant ITR (Flop, 130 nt)
ITR 在载体基因表达中的作用
在Rep78和Rep68的ATP依赖型DNA解旋酶活性作用下重塑A-A’区域,形成一个顶端为单链形式的末端分辨位点(trs)的茎环结构。在这种构型中,Rep78和Rep68的ATP依赖型链与位点特异性内切酶催化域在trs处引入一个切口,启动后续的复制、转录和表达。ITR在基因表达过程中的作用构象见下图Figure4:
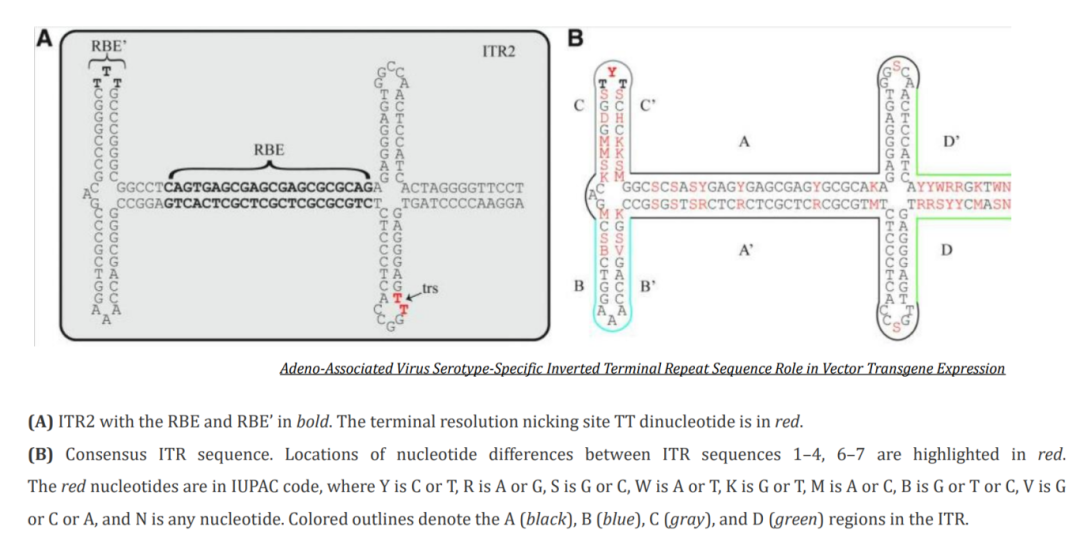
Figure4: ITR role in Vector Transgene Expression
ITR 变异体
ITR最常见的突变是在其中一个ITR的B或C环中出现一个小的缺失,这些小缺失通常被认为不会有什么问题,因为发生突变的ITR在AAV复制过程中具有独特的自我修复能力,这可能是通过位于基因组另一端的完整ITR实现的。据报道,其中一个ITR中的B环、C环或B-C环缺失的AAV病毒与野生型(两端ITR完整)AAV病毒在生物活性方面没有明显差异;其中一个ITR中的A区域缺失的GOI质粒生产的AAV病毒与野生型(两端ITR完整)AAV病毒在生物活性方面也没有明显差异;D序列对基因组包装很重要,其中一个ITR中的D区域缺失的载体与野生型ITR相比,生物活性会有所降低。ITR缺失对AAV效力的影响见下图Figure5:
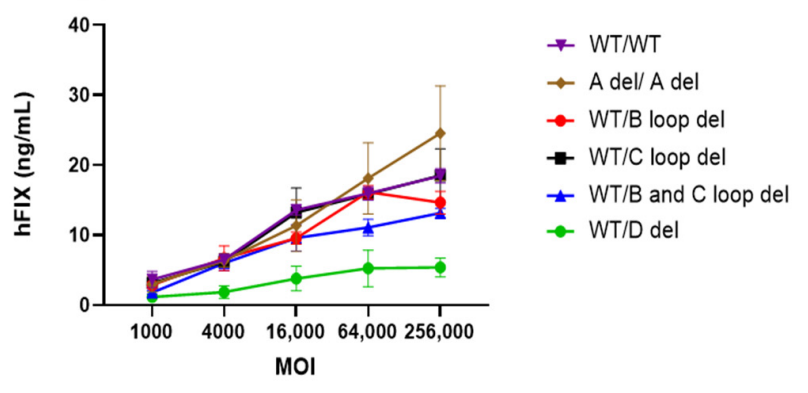
Figure5: Impact of ITR deletion on potency
支持CMC开发及BLA上市的ITR设计
有报道称,虽然145bp的wtAAV2 ITR质粒转化stbl3感受态后,~40%的克隆有出现ITR突变(主要为其中一端ITR的B环或C环缺失),但是在挑选出ITR完整的克隆后,在后继的扩增和发酵过程中没有再出现ITR突变。并且,目前已上市的8款AAV基因治疗产品中有5款是采用HEK293生产体系生产的,这5款产品中有3款产品(LuxturnaUpstazaElevidys)的载体两端ITR均使用了145bp的wtAAV2 ITR,其中1款产品(Zolgensma)的载体ITR为5’:106bp、3’:143bp,另1款产品(Beqvez)的ITR信息不明。可见,大部分HEK293生产体系生产的已上市AAV基因治疗产品选择了145bp的wtAAV2 ITR,说明145bp的wtAAV2 ITR在CMC开发及监管机构上市审评过程中得到了充分论证,可以确保药品安全、有效和质量可控。
派真生物的“派载体”平台采用野生型AAV2 ITR (145bp),以更好地支持客户项目的CMC开发及未来BLA申报上市。同时,我们通过优化载体骨架以及开发高保真E.Coli菌株PBS1,进一步确保ITR完整性以及AAV产品质量。
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。

