您是否也在为AAV载体的空壳率过高而烦恼?
在AAV基因治疗载体的生产过程中,有一个令所有从业者头疼的问题:仅有10-50%的病毒颗粒含有完整的目标基因组,其余大部分是空壳或含有不完整基因组的”废品”。这些杂质不仅影响治疗效果,还可能引发免疫反应,直接影响产品的安全性和有效性。
近期,一项发表在《Molecular Therapy: Methods & Clinical Development》的重磅研究为我们带来了全新的解决思路。研究团队通过巧妙的”填充序列”策略,不仅显著优化了AAV颗粒质量,更揭示了一个惊人发现:填充序列的具体选择比我们想象的更加关键!

研究背景:当前AAV生产的“质量困境“
当前AAV生产面临以下核心挑战:
1. 完整填充率低:只有10-50%的颗粒含有完整基因组;
2. 空壳率高:大量空壳竞争结合位点,降低转导效率;
3. 异质性强:部分填充和过度填充颗粒影响产品一致性;
4. 纯化困难:现有技术难以完全去除产品相关杂质。
FDA和EMA等监管机构已要求治疗性AAV制品必须报告空壳、部分填充和完整填充颗粒的比例,这进一步凸显了解决这一问题的紧迫性。
创新策略:用“填充序列“巧妙调控基因组大小
研究团队提出了一个看似简单却极其巧妙的策略:通过在表达盒的5’或3’位置插入非编码”填充序列”,将基因组大小从2.0kb逐步扩展至5.0kb,从而优化AAV颗粒的填充状态。
1. 为什么这样做?这是因为:
- 小基因组(<2.5kb):容易“装太多”,产生双倍大小的异常颗粒;
- 大基因组(>4.5kb):容易“装不全”,导致基因组截断;
- 最适大小(3.0-3.5kb):获得最佳的完整颗粒比例。
2. 实验方法
- 载体系统:AAV6.2和AAV2(验证血清型通用性);
- 表达盒:CMV-eGFP-poly(A);
- 填充序列:两种不同来源的序列进行对比;
- 检测手段:质量光度法、纳米孔测序、ddPCR等前沿技术。
关键发现:填充序列身份决定成败
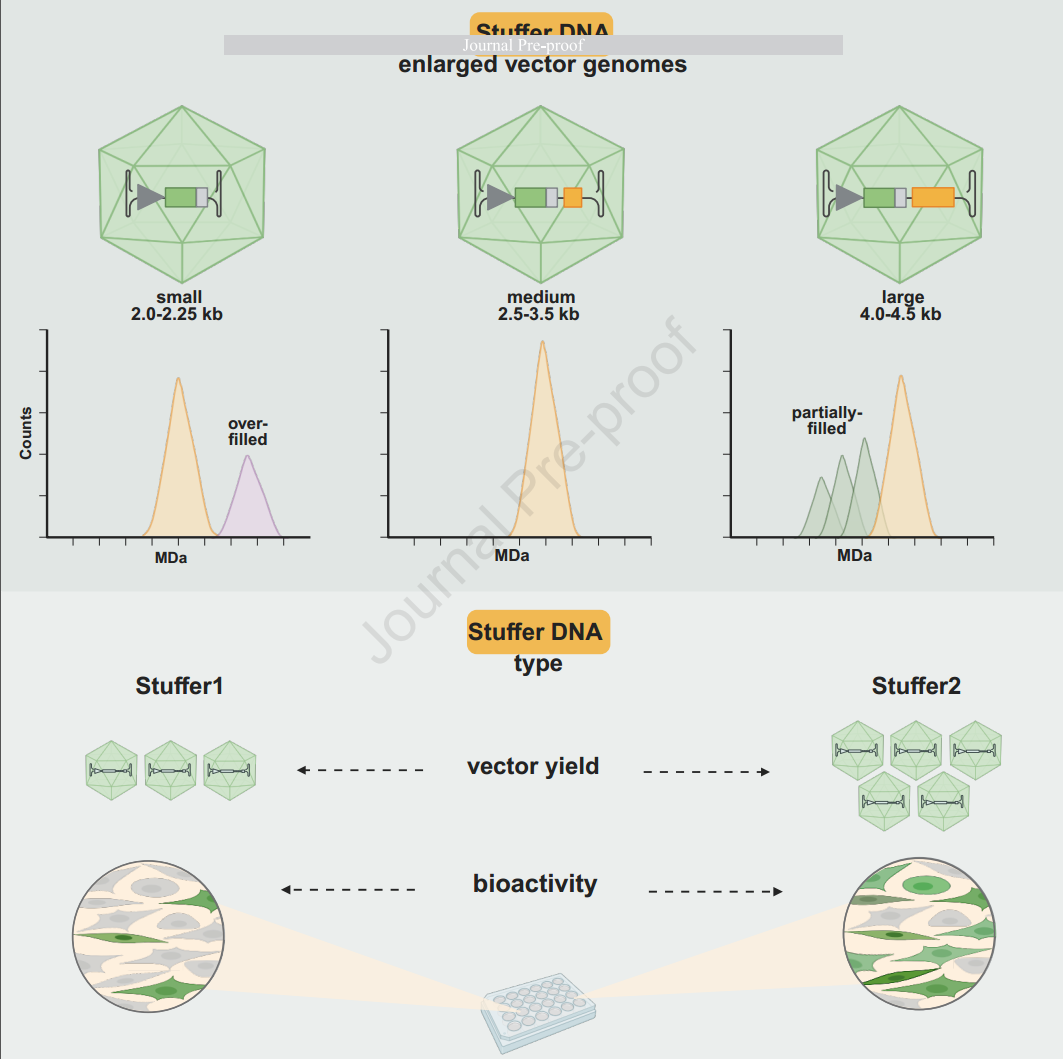
发现一:基因组大小的“最佳区间“
通过系统性分析不同基因组大小的AAV制品,研究发现:
1. 过度填充颗粒比例:
- 2.0-2.25kb基因组:高达20-40%;
- 3.0-3.5kb基因组:降至10-17%;
- 4.5-5.0kb基因组:几乎无过度填充,但部分填充增加至40-60%。
2. 完整颗粒比例最优区间:3.0-3.5kb
发现二:填充序列的“身份“至关重要
研究团队测试了两种填充序列:
填充序列1(Stuffer1):计算机设计的人工序列;随基因组增大,AAV产量持续下降(最高降幅68%);生物活性显著受损(最高降幅82%)。
填充序列2(Stuffer2):来源于天然UBE3A基因的3’UTR;产量基本维持或仅轻微下降;生物活性几乎完全保持。
这一对比结果彻底颠覆了“所有填充序列效果相似“的传统认知!
发现三:机制解析揭示根本原因
进一步的机制研究表明:
1. 转录水平影响:填充序列1在质粒转染水平就显示负面效果,说明影响发生在转录阶段。
2. 序列特性差异:
-
- GC含量:Stuffer1(43.5-44.8%)vs Stuffer2(33.8-34.7%);
- 序列多样性:人工序列重复性高,天然序列多样性丰富;
- 进化优势:天然序列具有数百万年进化筛选的优势。
实用指导:AAV载体设计的最佳实践
本研究对AAV生产的启示:
1. 基因组大小优化:将小于2.5kb的表达盒扩展至3.0-3.5kb;避免设计超过4.5kb的载体;重点关注完整颗粒比例的提升。
2. 填充序列选择策略:优先选择天然来源的非编码序列,避免完全人工设计的序列;优先选择3’UTR区域的序列片段;注意GC含量控制在合理范围。
3. 质量控制要点:
- 建立质粒水平的预筛选体系;
- 使用质量光度法监控颗粒分布;
- 通过生物活性检测验证功能的保持情况。
4. 插入位置建议
5’插入vs 3’插入:根据研究数据,5’插入(启动子上游)的耐受性总体上优于3’插入[poly(A)下游],但具体效果仍需结合填充序列特性综合评估。
监管与未来趋势
1. 监管层面的重要性
虽然当前FDA的CMC指南主要关注启动子、转基因等功能元件,但这项研究清楚表明:非编码区域同样对产品质量具有决定性影响。未来监管要求很可能将扩展到包括填充序列在内的所有载体组成部分。
2. 行业应用前景
- 标准化流程:建立基于天然序列的填充序列库;
- 个性化设计:针对不同的转基因和血清型定制优化方案;
- 质量提升:通过理性设计显著改善AAV制品质量属性;
- 成本优化:减少下游纯化负担,提高生产效率。
总结与展望
这项研究提醒我们:在基因治疗载体的设计中,没有任何一个序列元件是”无关紧要”的。每一个碱基的存在都可能对最终产品产生深远影响。
您的项目是否也面临类似挑战?
- 空壳率过高影响疗效?
- 生产批次间一致性不佳?
- 下游纯化成本居高不下?
我们愿意与您分享更多关于AAV载体优化的专业见解,共同推动基因治疗技术的发展。
派真生物AAV生产的优势与服务升级
基于本研究的结果,我们已着手优化现有的AAV生产服务:
✅载体设计优化:整合最新研究成果,为客户提供个性化的表达盒设计建议;
✅ 质量控制升级:引入质量光度法等先进检测手段,确保产品质量;
✅ 工艺参数调整:基于基因组大小特点优化生产和纯化工艺;
✅ 技术咨询服务:为客户提供专业的载体设计和优化建议。
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。