在基因治疗领域,腺相关病毒(AAV)作为载体已经被广泛应用,但现有的AAV载体在脑部应用时仍面临诸多挑战:
- 转导效率不够高:难以有效地将治疗基因递送到目标细胞;
- 剂量需求大:需要使用高剂量才能达到治疗效果;
- 副作用风险:高剂量可能带来不必要的安全隐患;
- 跨物种差异:在小鼠中有效的载体在大型哺乳动物中可能效果不佳。
2025年5月,来自美国宾夕法尼亚大学和俄亥俄州立大学的研究团队在《Science Translational Medicine》发表了研究成果,通过非人灵长类动物(NHP)筛选,成功开发出AAV-Ep+衣壳变体,在脑部基因递送效率上显著优于现有载体,为神经退行性疾病的基因治疗提供了新的技术选择。

AAV-Ep+的诞生:NHP体内筛选策略
研究团队采用了独特的筛选方法:在非人灵长类动物中直接筛选,而非传统的小鼠模型。通过在AAV衣壳的可变区域插入半随机七肽,生成了包含约680万种衣壳变体的AAV1、AAV2和AAV9文库(其中基于AAV1的衣壳变体约130万种、基于AAV2的衣壳变体约230万种、基于AAV9的衣壳变体约325万种)。将这三种血清型的文库混合后注入成年恒河猴的侧脑室,收集感兴趣的脑区,包括室管膜和大脑皮层,提取病毒DNA,测序,生成第二轮AAV文库。将新制备的AAV文库注入第二只成年恒河猴的侧脑室,从中收集病毒DNA和细胞RNA(图1),通过病毒扩增子高通量测序来鉴定成功富集的衣壳。通过两轮筛选,研究者鉴定出一种名为AAV-Ep+的AAV衣壳,它在转导NHP的室管膜细胞和大脑神经元时表现出显著增强的效力。
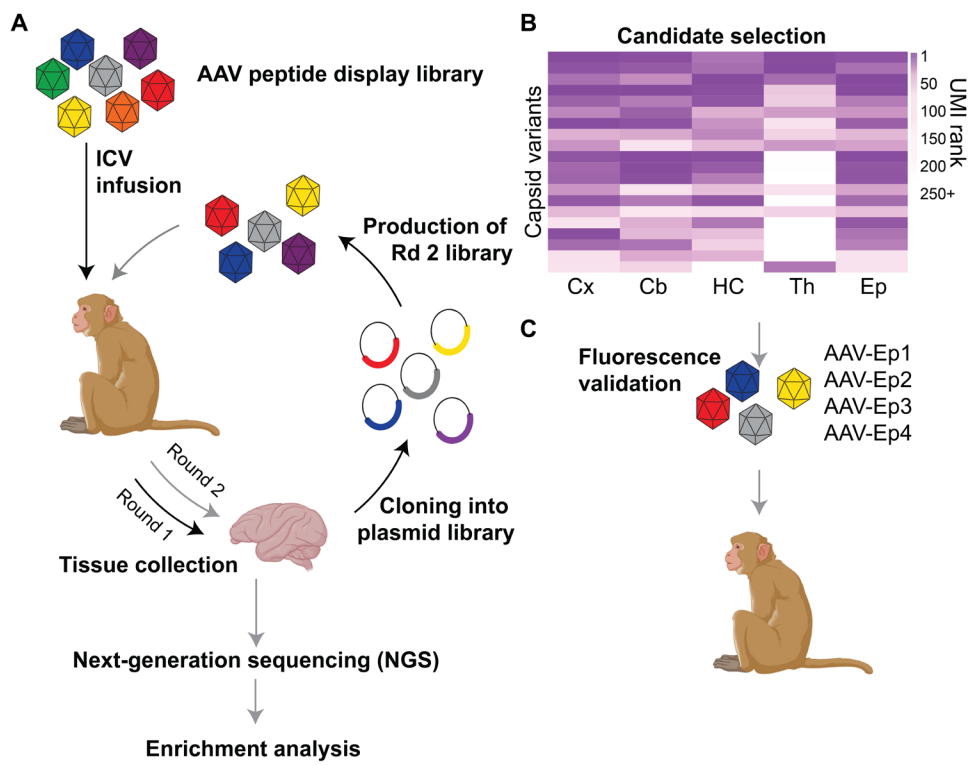
图1. AAV衣壳文库富集和候选者选择
为什么选择非人灵长类?研究发现,在小鼠中筛选出的载体往往无法在大型哺乳动物中重现同样的效果。因此,团队选择在与人类更为相近的非人灵长类动物中进行筛选,大大提高了临床转化的成功率。
AAV-Ep+的四大优势
1. 超强的靶向能力。对室管膜细胞的转导效率比其亲本AAV1高22倍,能够广泛转导大脑皮质神经元和深层脑区,在整个脑室系统中实现均匀分布(图2)。
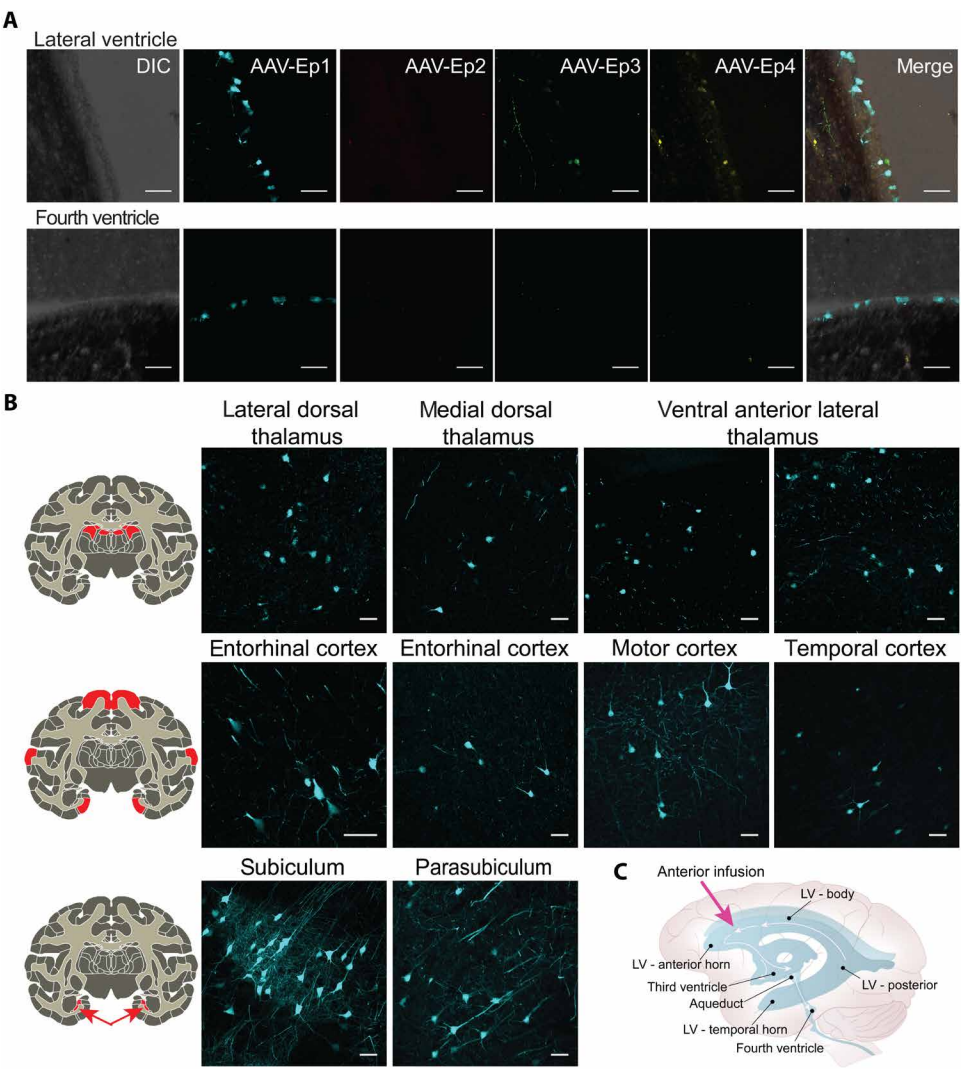
图2. AAV-Ep的报告基因评估结果。
(A)在成年恒河猴的侧脑室(上)和第四脑室(下)中检测荧光报告基因表达,该恒河猴4周前接受了四种候选衣壳的单侧脑室内注射。DIC(差分干涉对比显微镜),AAV-Ep1(AAV1变体;CAG.mTFP1)、AAV-Ep2(AAV2变体;CAG.mRuby3)、AAV-Ep3(AAV2变体;CAG:mNG)和AAV-Ep4(AAV9变体;CAG:mTagBFP)。(B)在(A)中检查的同一动物的额外室管膜区域中AAV-Ep1的荧光报告基因表达。(C)显示了向右侧前侧脑室注射(品红色箭头)的部位。
2. 卓越的跨物种兼容性。AAV-Ep+在多个物种中都展现出优异表现:
- 三种非人灵长类动物(恒河猴、非洲绿猴、食蟹猴);
- 两种小鼠品系(C57BL/6和FVB);
- 人源化诱导多能干细胞(iPSC)衍生神经元。
3. 显著降低剂量需求。在NHP中,AAV-Ep+的使用剂量比以往报道低30倍以上,达到的蛋白表达水平是正常人脑脊液的5-9倍,大幅提升了治疗的安全窗口。
4. 安全性优势。相比传统AAV9载体,AAV-Ep+展现出更好的安全特征:极低的外周组织转导(肝脏、心脏);背根神经节转导率<3.3%,显著降低了毒性风险。
临床应用前景:CLN2疾病的基因治疗
CLN2病是一种罕见的遗传性神经退行性疾病,由TPP1酶缺陷引起。患儿通常在幼年发病,出现严重的神经功能退化,预后极差。
在缺乏TPP1活性的小鼠模型中,研究团队使用AAV-EP+载体递送人TPP1基因,显著改善了震颤症状,延长了生存期,脑组织中酶活性提高了7-27倍(图3A-C)。
在非人灵长类动物中,使用剂量仅为1×10¹²vg(远低于既往研究),脑脊液中TPP1浓度达到正常人的5-9倍(图3D,E)。
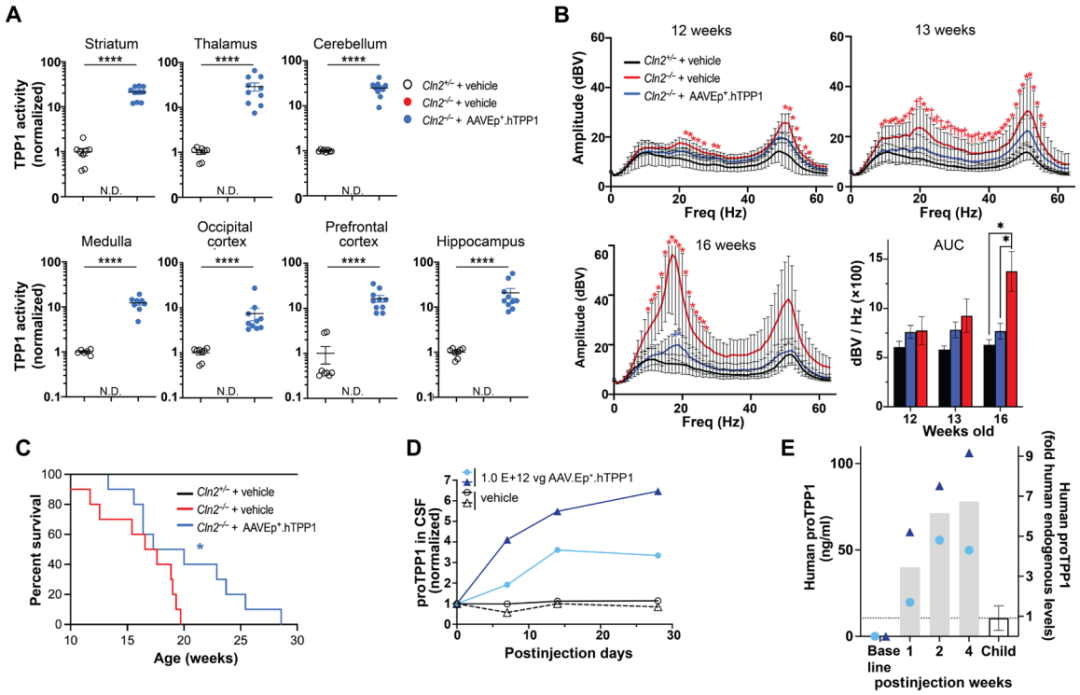
图3. AAV-Ep+.hTPP1治疗对Cln2−/−小鼠的功能校正以及在NHPs中hTPP1的表达情况。(A)在7周龄时接受5×10¹⁰vg AAV-Ep+注射的小鼠组织匀浆中的TPP1酶活性,5周后收集样本。(B)在5分钟记录间隔内,指定频率下的静止性震颤幅度。(C)在7周龄时接受5×10¹⁰vg AAV-Ep+.hTPP1治疗的小鼠的生存曲线。(D)在1、2和4周后,接受AAV-Ep+.hTPP1脑室内注射的食蟹猴脑脊液中Pro-TPP1蛋白的丰度,以每只动物的基线值为基准进行标准化(每半球5×10¹¹ vg AAV-Ep+.hTPP1,总计1×10¹² vg)。(E)接受AAV-Ep+.hTPP1治疗的NHP脑脊液中的人类TPP浓度(ng/mL)与九份人类脑脊液样本中内源性TPP1的比较结果。
总结与展望
本研究通过在NHP中筛选AAV衣壳变体,成功鉴定出AAV-Ep+,为需要在CSF中表达目的蛋白的基因治疗提供了一种潜在的高效载体。
AAV-Ep+在多个物种中的转导效力表明其具有良好的临床转化潜力,其应用不仅限于CLN2疾病,同时也为多种神经系统疾病治疗开辟了新路径:
- 溶酶体贮积症:利用交叉校正机制治疗各类酶缺陷病;
- 帕金森病:递送神经生长因子;
- 阿尔茨海默病:表达治疗性抗体或纳米抗体;
- 肌萎缩侧索硬化症:分泌神经保护因子。
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。