基因治疗已成为治疗多种遗传性疾病的革命性方法,其中腺相关病毒(AAV)载体因其优异的安全性和有效性,已成为体内基因递送的首选工具。然而,预存抗体这一”隐形屏障”限制了约30-60%潜在患者获得AAV基因治疗的机会。
近期发表在 Neurology 的一篇病例报道,记录了两名体内存在高滴度AAV9 抗体(1:800) 的脊髓性肌萎缩症(SMA)双胞胎,如何在治疗窗口(2岁)关闭前,采取血浆置换+利妥昔单抗 “组合拳”降低AAV抗体,却仍在输注onasemnogene abeparvovec(OA,英文商品名Zolgensma,中文商品名“诺健生”)时出现急性过敏反应,导致疗效受限的全过程。这篇案例不仅提供了“成功降低AAV抗体滴度”的可行路径,也暴露了 IgG 之外的免疫盲区。

一、研究方法
- 受试者基本情况:21个月男双胞胎,确诊SMA(SMN1基因零拷贝,SMN2基因3拷贝),A双胞胎能独立坐但不能行走,B双胞胎能行走但有轻度步态异常,Anti‑AAV9 Ab 1:800(OA治疗要求Anti‑AAV9 Ab≤1:50)。
- 目的:在治疗窗口(2岁)关闭前,将抗体滴度 ≤1:50 以满足 OA 说明书要求。
- 治疗方案:研究团队设计了一套综合免疫清除方案:① 使用Spectra Optia血浆分离系统进行血浆置换(TPE),共进行11 次(每次 1×血浆量,白蛋白回输),以去除循环中的抗体;② 利妥昔单抗(rituximab)2 剂(–30 & –23d),靶向清除产生抗体的B细胞;③ OA 输注前 2d开始口服强的松龙(1mg/kg),输注当天静脉给予甲基强的松龙(2mg/kg),抑制总体免疫反应。
- 观测指标:① AAV9 抗体动态;② 输注安全性;③ 运动功能量表(HFMSE、CHOP‑INTEND 等)
二、研究结果
1. 抗体清除效果
A双胞胎:AAV9抗体滴度从1:800降至1:50;B双胞胎:AAV9抗体滴度从1:800降至1:25,成功“达标”(图1)。
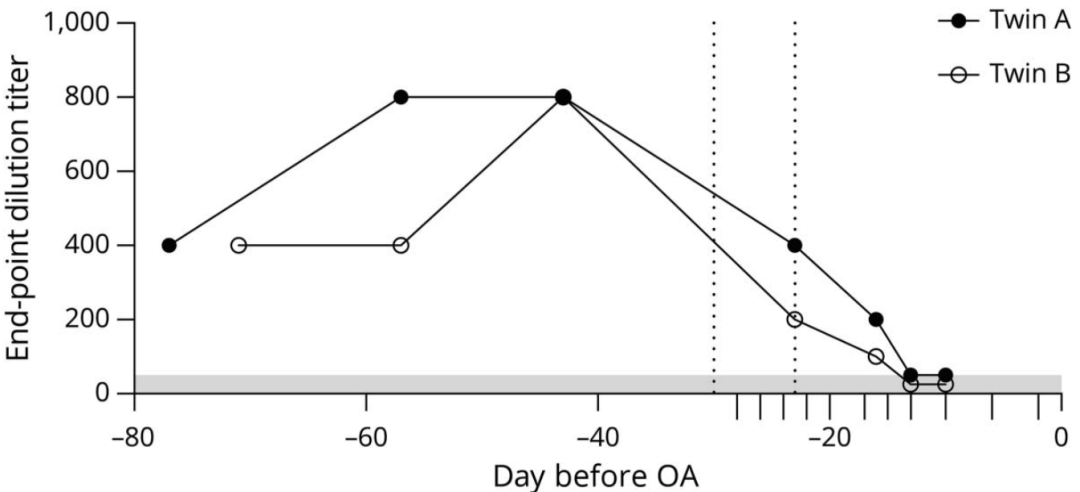
图1. 免疫耗竭干预措施的时间顺序及其相关的AAV抗体滴度变化。灰色区域表示参考范围终点稀释比≤1:50。x轴主要刻度表示血浆置换日期:-28、-26、-24、-22、-20、-17、-15、-13、-10、-6和-2天。虚线表示于-30天和-23天给予利妥昔单抗。OA输注当日(0天)静脉输注甲基强的松龙。
2. 治疗过程中的挑战
急性过敏反应:尽管采取了预防措施,两名患者在开始输注OA约10分钟后仍出现荨麻疹、喘息和胃肠道症状。
治疗中断:由于严重过敏反应,不得不中止给药,并给予肾上腺素治疗。随后给予苯海拉明,并留院观察一晚。
3. 基因治疗前后运动神经元功能的改善情况
由于仅接受了部分剂量的OA,在治疗2个月后(26月龄),双胞胎A未获得治疗益处,双胞胎B可能获得了有限的改善。
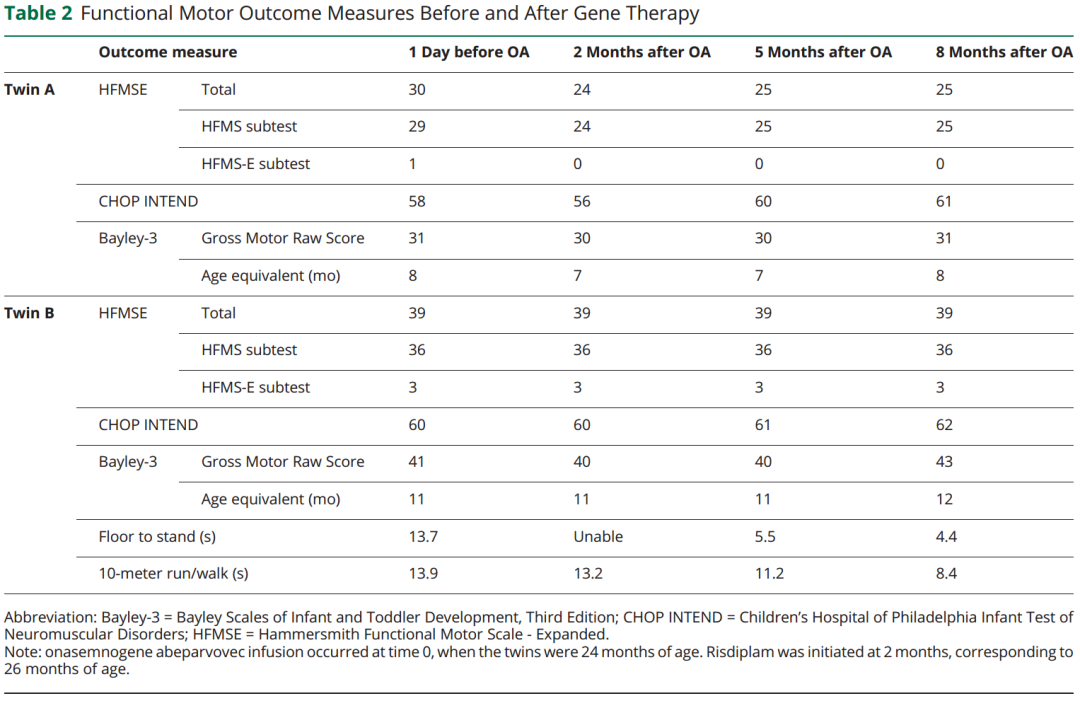
随后,研究团队为患儿启用了利司扑兰(risdiplam)治疗。在利司扑兰治疗3-6个月后,两名患儿的运动功能均有不同程度改善。
三、讨论与总结
1. 技术可行但挑战犹存
该研究证实了通过血浆置换和B细胞清除能够有效降低AAV9抗体滴度,但同时揭示了仅降低抗体水平可能不足以防止输注反应。这表明:抗体滴度只是一部分,IgG抗体水平下降不代表所有免疫记忆被清除。
过敏性休克主要由先前暴露后产生的IgE抗体介导,而IgE抗体主要结合于肥大细胞表面,不易通过血浆置换清除,因此未来可能需要将AAV9的IgE检测纳入安全性检测标准。
与 AAV 输注直接相关的急性过敏性休克极为罕见,目前仅见于治疗血友病的 valoctocogene roxaparvovec 报道,而用于 OA 治疗的案例尚未见报道。本研究中两例患儿出现超敏反应的原因尚不清楚。若在反应发生时检测血清类胰蛋白酶(tryptase)或 IL-6,可能有助于区分肥大细胞脱颗粒与细胞因子释放综合征,但这些指标当时并未测定。
2. AAV载体的优化方向
这项研究也为AAV载体的优化提供了重要启示:
- 未来可通过修饰AAV衣壳以降低其被抗体识别的可能性;
- 在AAV生产过程中,需要控制空壳率,减少制备过程中的空AAV颗粒,降低免疫原性;
- 新型血清型开发:筛选和开发人群中预存抗体较低的新型AAV血清型。
参考资料
Nelson RW, et al. Reduction of Preexisting AAV9 Antibody Titers Before Onasemnogene Abeparvovec Administration in Twins With Spinal Muscular Atrophy. Neurology. 2025;105:e213899.
Day JW, et al. Adeno-associated virus serotype 9 antibody seroprevalence for patients in the United States with spinal muscular atrophy. Mol Ther Methods Clin Dev. 2023;31:101117.
Potter RA, et al. Use of plasmapheresis to lower anti-AAV antibodies in nonhuman primates with pre-existing immunity to AAVrh74. Mol Ther Methods Clin Dev. 2024;32:101195.
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。