耳聋是最常见的感官障碍疾病之一,全球约有4.3亿人受致残性听力障碍困扰,其中2600万为先天性耳聋患者。遗传因素约占先天性耳聋的60%,已知的耳聋基因超过200个,然而目前暂无临床上市的治疗药物。
非综合征型常染色体隐性遗传性耳聋DFNB 111 (Autosomal recessive genetic forms 111)是一种早发性、进行性的轻度至中度感音神经性听力损失,且听力损失在高频更为明显,MPZL2基因突变是该类型耳聋的重要致病因素。近年,一项基于大规模轻度至中度感音神经性听力损失(SNHL)儿童队列的前瞻性研究表明,MPZL2是导致遗传性轻度至中度SNHL的第二常见基因,占17.3%,仅次于STRC基因(55.8%)。值得注意的是,MPZL2中的某些特定突变(如c.220C>T)在东亚人群中具有创始效应(Founder effect),提示其可能为该地区特有的遗传风险因素。
2025年8月5日,复旦大学附属眼耳鼻喉科医院舒易来教授团队与韩国首尔大学医院Sangsu Bae、Sang-Yeon Lee科研团队合作在国际期刊Nature Communications上发表题为“PAM-flexible adenine base editing rescues hearing loss in a humanized MPZL2 mouse model harboring an East Asian founder mutation”的研究论文,利用PAM灵活型腺嘌呤碱基编辑器(ABE8eWQ-SpRY)结合高效的内耳靶向AAV递送,精准修复东亚人群高发的MPZL2 c.220C>T创始突变,在人源化小鼠模型中显著恢复听力,并维持至少20周。这一成果为遗传性耳聋的“一次性”精准治疗提供了全新思路。

研究亮点
1. 基于中韩两国遗传性耳聋病人临床队列研究,发现亚洲高发的MPZL2 c.220C>T突变位点;
2. 发了一个人源化MPZL2突变小鼠模型(hMPZL2Q74X/Q74X),完全模拟了人类该类耳聋的基因与听力表型;
3. 选择了PAM灵活的ABE编辑器,能够在不造成DNA双链断裂的情况下,将致病性A·T碱基精准转化为正常的G·C,避免了传统CRISPR的潜在大规模缺失和安全风险,成功恢复小鼠内耳MPZL2蛋白的表达、内耳结构的完整性以及小鼠听力。
主要研究结果
1. 东亚特异性MPZL2基因突变在DFNB111相关听力损失中的临床意义
研究团队基于临床队列研究,对遗传性耳聋1437例无亲缘关系的耳聋家系进行了系统性病因学分析。筛选出234例表现为对称性、轻中度非综合征型SNHL未成年患者(≤18岁),明确了155例患者的致病基因(66.2%)。其中24例与MPZL2基因突变有关(15.5%),且23例(95.8%)患者携带至少一个c.220C>T等位基因突变。c.220C>T等位基因在东亚人群中频繁出现,提示该突变可能为东亚地区的创始突变。
2. 人源化MPZL2 c.220 C > T小鼠的构建以及表型描述
针对该突变位点,研究团队构建了人源化小鼠模型(hMPZL2Q74X/Q74X),该小鼠模型表现为进行性听力损失,重现了人类MPZL2耳聋病人的听力学表型:渐进性低至中度听力损失,且有着比较明显的内耳毛细胞的丢失(图1)。
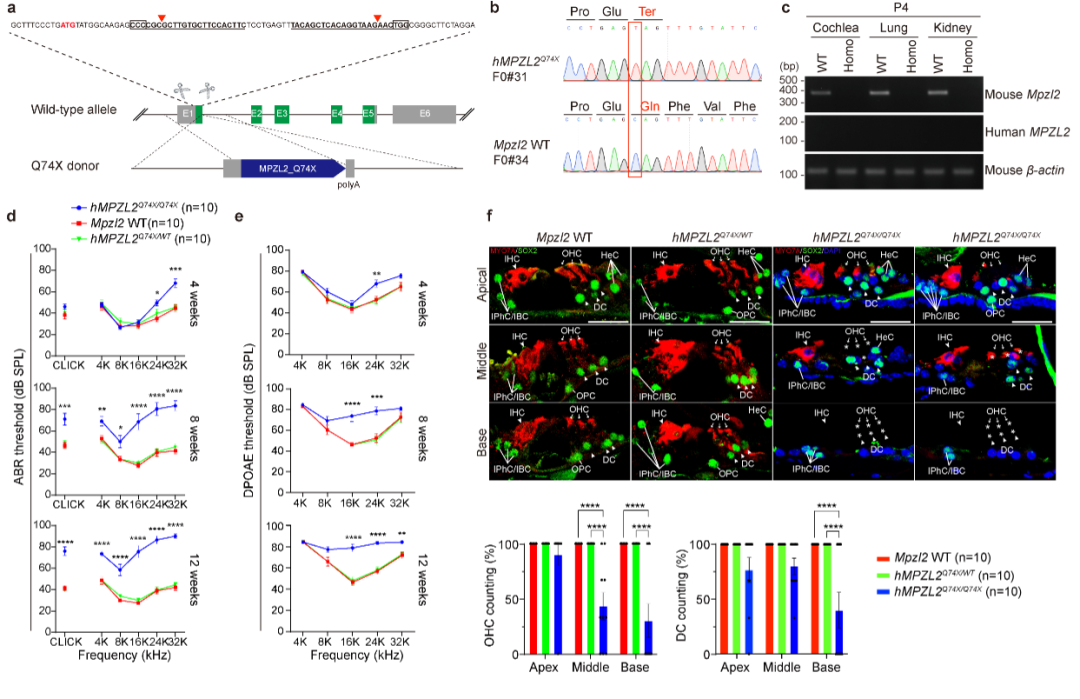
图1. 人源化MPZL2 c.220 C > T小鼠模型的听力学表型及内耳结构的损伤。
图1. 人源化MPZL2 c.220 C > T小鼠模型的听力学表型及内耳结构的损伤。a用CRISPR/Cas9系统构建人源化MPZL2小鼠模型(hMPZL2Q74X)的靶向策略示意图。b 采用Sanger测序对hMPZL2Q74X小鼠和Mpzl2野生型(WT)小鼠的基因序列进行验证。c RT-PCR检测P4时期hMPZL2Q74X/Q74X纯合突变小鼠与Mpzl2 WT小鼠中MPZL2和Mpzl2的表达情况。d、e 4周、8周和12周龄时Mpzl2 WT(红色,n = 10)、hMPZL2Q74X/WT杂合小鼠(绿色,n = 10)和hMPZL2Q74X/Q74X纯合突变小鼠(蓝色,n = 10)的ABR和DPOAE阈值比较。f 12周龄Mpzl2 WT小鼠(n = 1)、hMPZL2Q74X/WT小鼠(n = 1)和hMPZL2Q74X/Q74X小鼠(n = 2)耳蜗柯蒂氏器的代表性切片图(切片厚度10 μm),用肌球蛋白VIIa(毛细胞,红色)和抗Sox2(支持细胞,绿色)进行免疫标记。箭头指示内毛细胞(IHCs)和Deiters细胞(DCs),白色箭头指示外毛细胞(OHCs),白线标示支持细胞(SCs)。星号表示OHCs和DCs的缺失。
3. 基于ABE的基因治疗体系的体外筛选
针对该突变的A·T→G·C精确修复,研究团队评估了14种ABE与sgRNA组合,最终确定PAM几乎无限制的ABE8eWQ-SpRY:sgRNA3为最佳方案,该方案具有较高的体外编辑效率(约50%以上),较低的旁观者编辑和脱靶效应。
4. AAV递送策略、治疗效果及安全性评价
为突破AAV单载体容量限制,研究者采用了split-intein双AAV系统(图2)。通过圆窗膜显微注射,结果显示:
- 听力改善:治疗组在多频段ABR阈值显著下降,8 kHz接近野生型水平,效果可持续20周(图3)。
- 结构恢复:外毛细胞与Deiters细胞数量明显回升,耳蜗结构完整性改善。
- 分子水平:MPZL2 mRNA与蛋白表达恢复,相关细胞黏附与细胞外基质通路基因回归正常水平。
- 安全性:未检测到明显的脱靶效应或耳毒性,非耳蜗组织几乎无病毒分布。
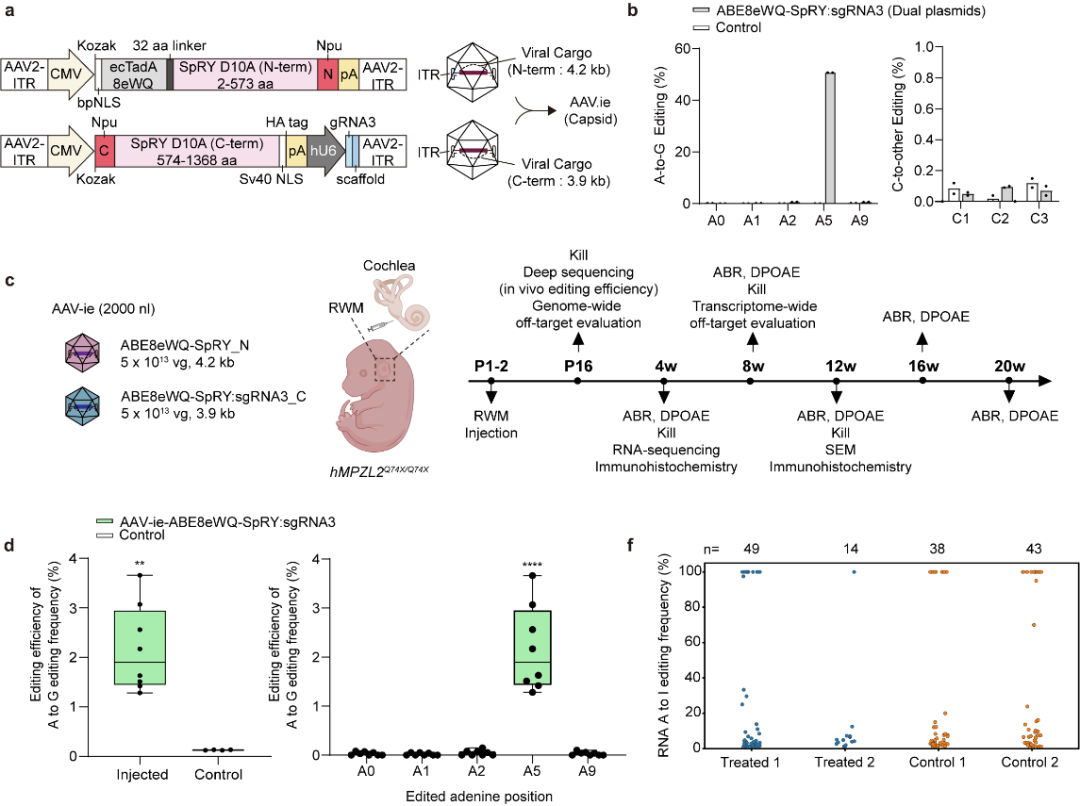
图2. 双 AAV-ie-ABE8eWQ-SpRY:sgRNA3 体内修复 MPZL2 c.220 C>T 突变。
a 用双 AAV 载体及分裂内含肽在体内递送ABE的示意图。b MPZL2靶点腺嘌呤及周围旁观腺嘌呤或胞嘧啶的编辑效率评估(n=2)。c 体内碱基编辑流程概览,将两个AAV病毒重悬至 5.0×10¹³ vg/mL,1:1混合。取2000 nL 注射至P2 期 hMPZL2Q74X/Q74X 小鼠圆窗膜(RWM)。d 柯蒂氏器官 DNA 中靶位点 A·T→G·C 编辑效率及周边核酸旁观效应。e Cas-OFFinder 预测的潜在体内脱靶位点,包含与靶序列 ≤2 bp 错配及/或 ≤1 bp DNA/RNA bulge 的位点。f 双 AAV-ie-ABE8eWQ-SpRY:sgRNA3 注射后 8 周,体内 RNA 脱靶检测。检测结果显示无 RNA 脱靶编辑。
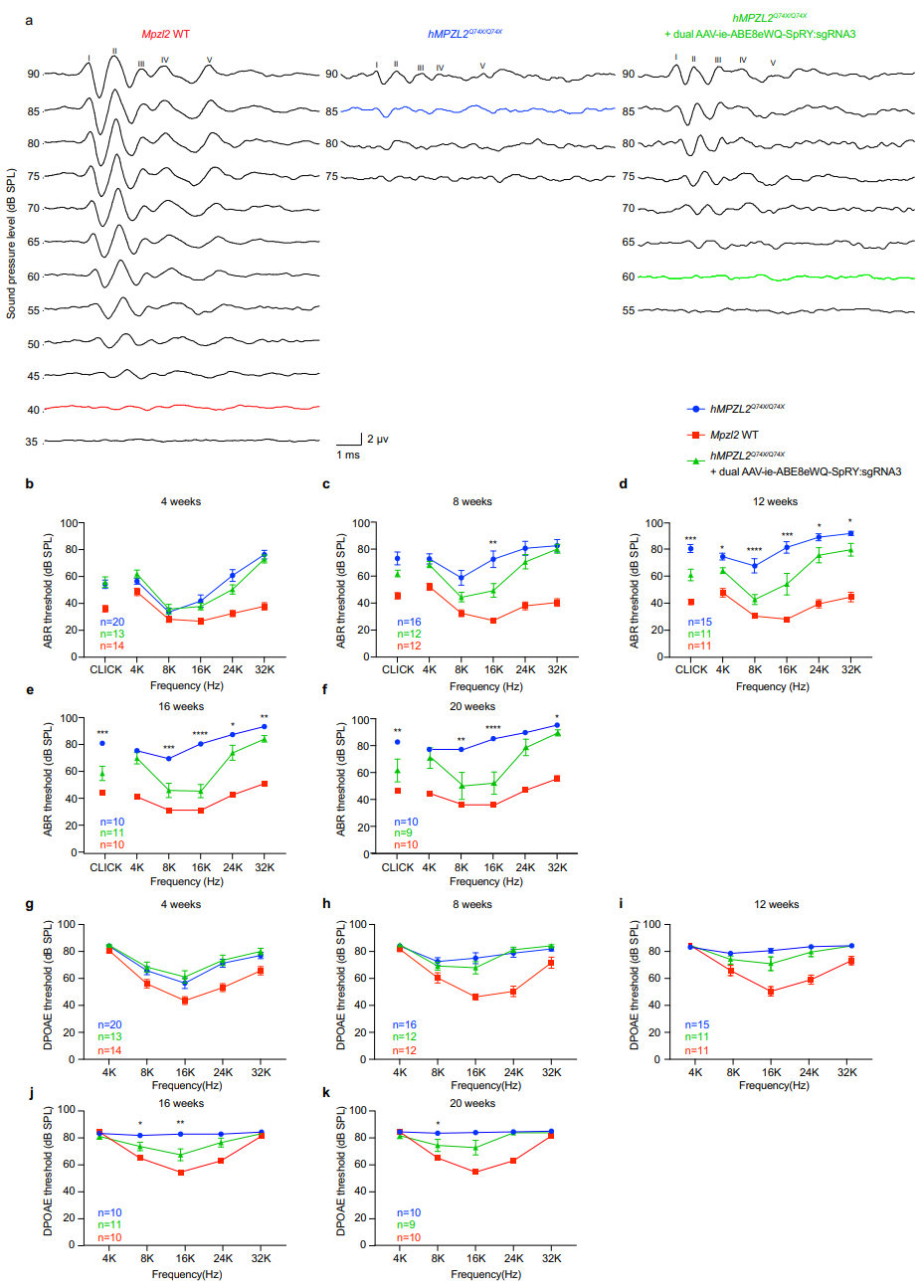
图3. ABE8eWQ SpRY:sgRNA3治疗体系恢复人源化MPZL2 c.220 C > T小鼠听力
a 在注射后第 12 周,对三组小鼠(Mpzl2野生型、hMPZL2Q74X/Q74X及经治疗的 hMPZL2Q74X/Q74X)在点击声刺激下记录的代表性 ABR 波形。每组中的粗线表示阈值。b–f 比较 Mpzl2 野生型(红线)、hMPZL2Q74X/Q74X(蓝线)及经治疗的 hMPZL2Q74X/Q74X(绿线)小鼠在 4 周(b)、8 周(c)、12 周(d)、16 周(e)和 20 周(f)时的 ABR 阈值。g–k 比较 Mpzl2野生型(红线)、hMPZL2Q74X/Q74X(蓝线)及经治疗的 hMPZL2Q74X/Q74X(绿线)小鼠在 4 周(g)、8 周(h)、12 周(i)、16 周(j)和 20 周(k)时的 DPOAE 阈值。
研究意义
1. 首创性:首次针对东亚创始突变实现PAM灵活型ABE体内精准修复。
2. 可推广性:为单一高频突变型遗传病提供“一次性”基因编辑治疗范式。
3. 平台价值:AAV-ie + split-intein递送模式可扩展至更多大基因或复杂突变的治疗。
派真生物有幸为本研究提供了AAV病毒包装服务。
原文链接:https://www.nature.com/articles/s41467-025-62562-8
研究团队简介:该研究由复旦大学附属眼耳鼻喉科医院舒易来教授团队牵头,联合韩国首尔大学医院Sangsu Bae团队以及Sang-Yeon Lee团队共同完成。复旦大学附属眼耳鼻喉科医院胡少伟、蒋罗颖,韩国首尔大学医院的Sohyang Jeong以及Hansol Koo为共同第一作者。
舒易来教授团队长期耕耘于耳聋基因治疗领域,创新性采用双AAV载体递送系统,运用基因置换、基因编辑等前沿技术,在多个耳聋模型上证明了基因治疗的疗效。经过数年刻苦攻关,成功研发出OTOF耳聋基因治疗药物,相关研究结果已发表于顶级医学期刊《柳叶刀》和《自然·医学》等杂志。
派真生物可提供以下内耳研究中用到的血清型和启动子:
靶向内耳的AAV血清型

内耳研究中用到的启动子

此外,派真生物还可提供随机多态展示AAV衣壳变体库、barcode AAV衣壳库等,助力客户筛选获得特异性更好的内耳靶向AAV衣壳。
参考资料
Hu, S.W., Jeong, S., Jiang, L. et al. PAM-flexible adenine base editing rescues hearing loss in a humanized MPZL2 mouse model harboring an East Asian founder mutation. Nat Commun 16, 7186 (2025). https://doi.org/10.1038/s41467-025-62562-8
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。