作为基因治疗领域最炙手可热的“明星载体”,腺相关病毒(AAV)以其低免疫原性、高安全性和持久的基因表达能力,在众多遗传病的治疗中展现出巨大潜力 。然而,在AAV的生产和应用实践中,一个棘手的技术难题日益凸显,那就是AAV基因组的不完整性。
尤其当需要递送的基因(GOI)较大,基因组尺寸超过AAV的“天然装载极限”(约4.7kb)时,我们常常在质量检测中(如毛细管电泳)发现大量的基因组片段,而非我们期望的完整“货物” 。这种不完整的基因组不仅无法在靶细胞内表达出功能蛋白,还可能引发非预期的免疫反应,从而严重影响治疗效果和安全性 。
那么,导致AAV基因组不完整的原因究竟是什么?我们又该如何应对这一挑战呢?
AAV基因组完整性及其检测方法
1. 什么是基因组完整性?
基因组完整性是指AAV基因组的结构完整性与序列准确性。重组AAV(rAAV)基因组主要包含两个关键部分:转基因表达框及其两端的反向末端重复序列(ITRs)。ITRs对病毒基因组的复制、包装乃至整合至关重要;转基因表达框则包含治疗性基因及驱动其表达所需的调控元件。任何AAV基因组的缺失、突变或重排(图1)都可能削弱载体功能,降低治疗效果,甚至带来安全性隐患。
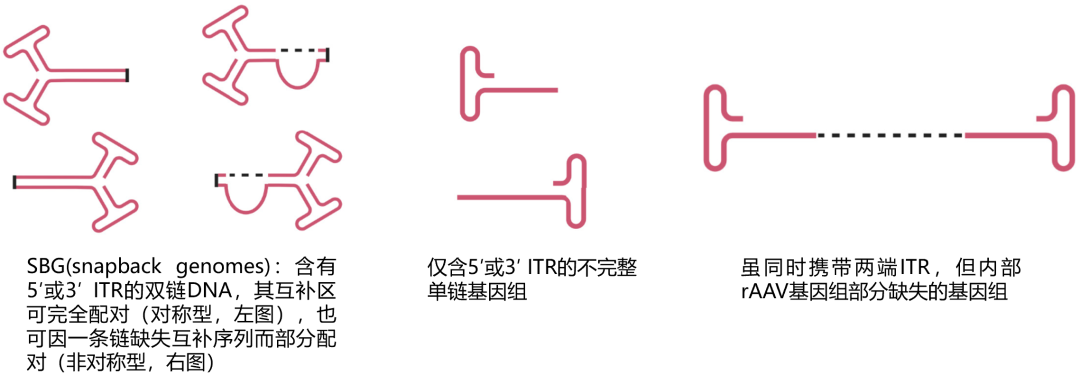
图1 rAAV内包装的不完整基因组DNA的种类示意图
2. AAV基因组完整性的检测方法主要有哪些?
变性琼脂糖凝胶电泳:成本低廉、操作简单,可在变性条件下直观观察 AAV 基因组,但精度有限,难以用于精细分析。
毛细管电泳(CE):是检测AAV基因组完整性的主要方法之一。其原理是通过电泳迁移时间区分不同大小的核酸分子,具有分辨率高、快速(<5分钟)、样品需求量小的优势,能够准确区分完整基因组和截断片段,提供定量信息。
定量PCR(qPCR)与微滴式数字 PCR(ddPCR):qPCR和ddPCR常用于特异性定量 AAV 基因组序列,滴度测定灵敏且准确,但无法提供基因组长度信息,也不能发现缺失目标序列的截短或重排基因组。
纳米孔测序:可实时、低成本、长读长分析 AAV 基因组,揭示全长结构与群体异质性,且价格亲民,不足之处是碱基识别准确性和一致性还有待提高。
PacBio 测序:单分子实时(SMRT)测序,读长超长,适合分析全长 AAV 基因组,可精准鉴定结构变异、截短与重排,但成本较高。
派真生物拥有全面的AAV质量分析平台,可提供60+种AAV相关检测方法。针对AAV基因组完整性评估,我们重点提供基于毛细管电泳的高通量检测服务,日通量最高可达 5×96 个样品,高效支持同一先导序列下不同候选载体的优化筛选。同时,我们还提供多种互补方法,包括碱性琼脂糖凝胶电泳、qPCR、ddPCR、Nanopore 测序等,以满足多样化的分析需求。
AAV基因组为何会“缺斤少两”?
1.“塞翁失马”——包装超大基因组的代价
AAV的衣壳如同一个大小有限的“快递箱”,其理论上的最大装载量约为4.7kb。当我们试图“硬塞”一个超过此大小的基因组时,包装过程可能会在基因组完全进入衣壳之前就提前终止。这种“强制包装”策略虽然在某些情况下能够实现超大基因的递送,但代价就是产生大量被截短的、不完整的基因组 。
2. 包装序列的长度和二级结构
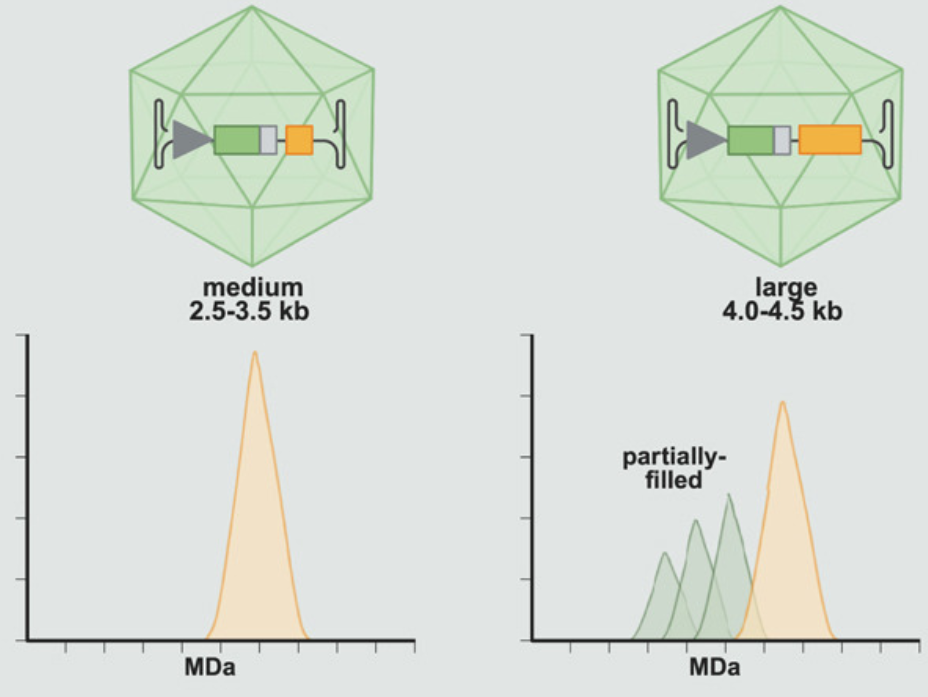
DNA分子在长度增加时,其柔性和拓扑结构变得更加复杂。Blahetek等的研究发现,基因组大小与AAV颗粒异质性之间存在明显关联:较小的AAV基因组(2.0–2.25 kb)容易发生过度填充,而较大的AAV基因组(4.5–5.0 kb)则更容易发生截断。
已有的研究表明,在 CMV 增强子、CB 启动子及 EGFP 基因等二级结构丰富的区域有“截断热点”(图2),表明序列结构是基因组断裂的关键诱因。
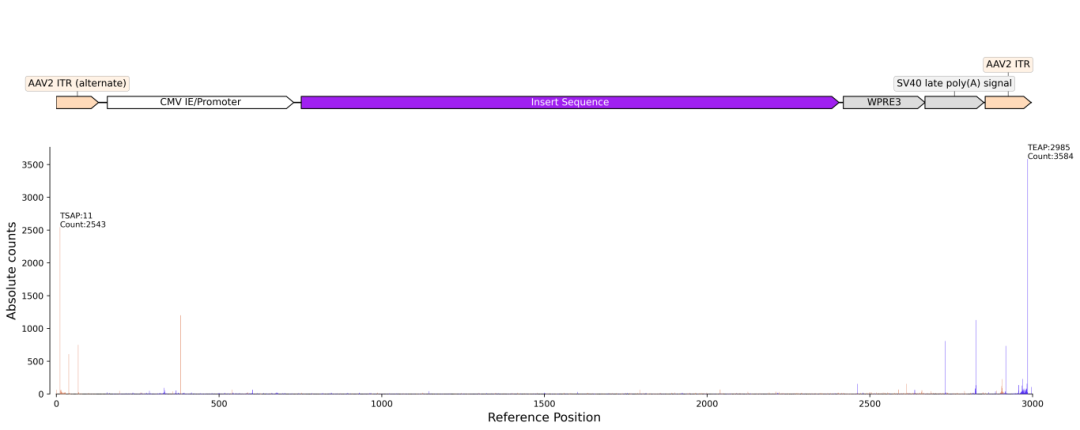
图2 Nanopore测序分析AAV基因组内的“截断热点”。横轴表示序列位置,纵轴为reads数量。TSAP:最高比对起始位置;TEAP:最高比对终止位置;Counts:比对序列数目(图片来源于派真生物)
Tran等研究发现,当两个sgRNA表达盒以尾对尾(tail-to-tail)方式排列时,会形成长回文结构,导致高频基因组截短,功能载体产量显著下降,而头对尾(tail-to-head)排列则未出现类似问题(图3)。
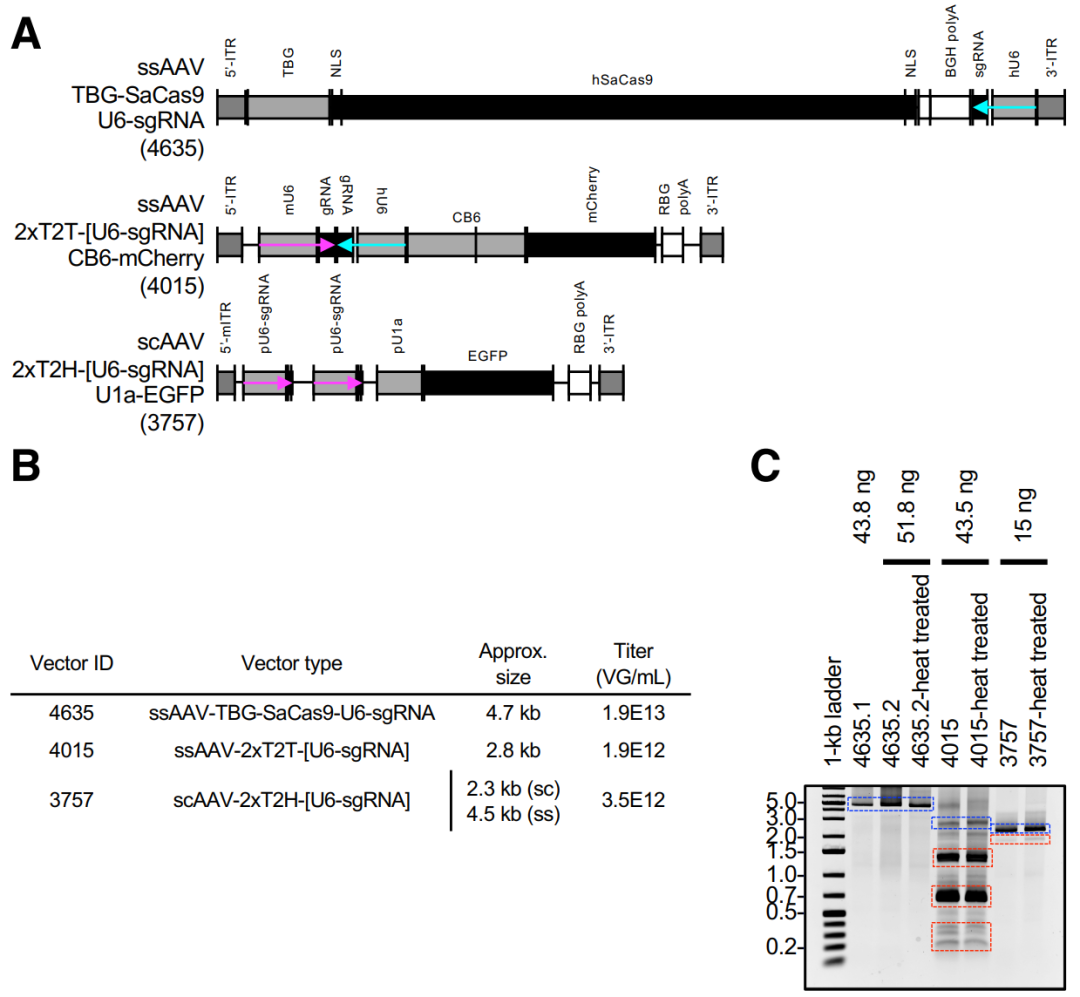
图3 sgRNA表达盒尾对尾设计对AAV基因组完整性的影响3。(A)载体基因组从ITR到ITR的示意图。箭头表示U6驱动的sgRNA的方向(正向,品红色;反向,青色)。(B) 载体信息表。自互补(sc)载体3757有两种预期大小:一种是sc形式(2.4 kb),另一种是单链(ss)形式,其大小约为前者的两倍(4.5 kb,mITR未加倍)。(C) 三种载体DNA提取后的代表性琼脂糖凝胶图,用于评估整体完整性。蓝色框表示迁移至与全长基因组大小一致的条带。红色框表示迁移至截短基因组大小的主要条带。
3. 包装信号和复制机制相关因素
- ITR结构完整性:ITR是AAV基因组复制和包装的“起点”和“终点”,其结构的完整性至关重要。然而,ITR区域富含G/C碱基,呈现高度复杂的二级结构,这使得它在质粒扩增和病毒复制过程中极易发生突变或缺失 。不完整的ITR会严重干扰AAV基因组的正常复制和包装,好比是发车信号出了故障,自然无法保证运输任务的顺利完成。
- Rep蛋白与DNA相互作用:研究表明,Rep蛋白中的同义突变可以通过影响Rep-DNA相互作用来增强AAV基因组包装。当基因组过大时,Rep蛋白对DNA的识别、切割和包装效率受到影响,导致提前终止包装过程。
如何打赢这场AAV基因组“保卫战”?
面对AAV基因组完整性这一挑战,全球的科学家们正在从多个角度探索解决方案,力求让每一颗AAV病毒都“满载而归”。
1. 优化基因盒设计——从源头减少错误
- 优化载体序列:加入设计合理的间隔序列,将启动子、Kozak序列、目的基因开放阅读框(ORF)以及polyA信号等元件进行物理分离,一方面可以为转录和翻译 machinery 提供更优的结合环境,另一方面可以减少形成稳定发夹结构或其他二级结构的可能性。为最大化AAV的有效包装空间,可以使用更小的启动子和调控元件,为更大的目的基因腾出空间。
- 避免使用易形成二级结构的设计(如尾对尾双sgRNA),以提高载体产量和功能完整性。
2. 升级生产工艺
- 优化质粒生产:采用特殊的宿主菌株和培养条件,可以有效减少ITR序列在质粒扩增阶段的突变和重组 。
- 改进病毒生产体系:无论是基于贴壁细胞还是悬浮细胞的生产系统,通过优化转染条件、收获时间以及纯化流程,都能在一定程度上减少不完整基因组的产生 。
3. 突破包装极限——递送“超大号”基因的策略
4. 精准的质量控制——用“火眼金睛”筛选出“正品”
除了传统碱性琼脂糖凝胶电泳和CE分析,新一代测序技术,特别是长读长测序技术(如Nanopore测序),为我们提供了前所未有的精确度,能够全面、深入地分析AAV产品中基因组的完整性、异质性以及杂质情况 。这为我们优化生产工艺、筛选出高质量的AAV产品提供了有力的武器。
总 结
AAV基因组的不完整性是基因治疗领域必须正视并解决的重要挑战。随着我们对基因组不完整原因的认识不断深入,通过全链条的改进,包括基因盒设计、生产工艺优化与质量控制,我们有理由相信,生产的AAV产品将具备更高的基因组完整性和更好的均一性,从而为遗传病患者带来更安全、疗效更佳的基因治疗药物。
作为专业的基因治疗服务提供商,我们深刻理解AAV基因组完整性的挑战。我们团队拥有丰富的AAV载体设计和优化经验,可以为各种规模的基因提供定制化的解决方案,帮助您克服包装限制,实现高效、安全的基因递送。无论是载体设计优化,还是生产工艺的调整,我们都能提供全流程技术支持,确保您的基因治疗项目成功实施。
参考文献
1. Brimble, Mark A. et al. (2023). Stowaways in the cargo: Contaminating nucleic acids in rAAV preparations for gene therapy. Molecular Therapy, 31(10): 2826 – 2838. https://doi.org/10.1016/j.ymthe.2023.07.025
2. Blahetek G., et al. (2025). AAV yield, bioactivity, and particle heterogeneity are influenced by genome size. Molecular Therapy Methods & Clinical Development, 33(3):101499. https://doi.org/10.1016/j.omtm.2025.101499
3. Tran NT., et al. (2020). AAV-Genome Population Sequencing of Vectors packaging CRISPR components reveals design-influenced heterogeneity. Molecular Therapy Methods & Clinical Development, 18: 639-651
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。