研究概述
2026年1月27日,中国科学院深圳先进技术研究院路中华研究员团队在Cell期刊在线发表题为“AAVLINK:ApotentDNA-recombinationmethodforlargecargodeliveryingene therapy”的研究论文。本研究提出了一种新型AAV大载荷递送策略AAVLINK,通过Cre/lox介导的分子间DNA重组,突破了传统AAV载量限制,实现了大基因及CRISPR工具的高效重建与表达。
研究表明,AAVLINK相较现有拼接策略具有更高的重建效率和更少的截短副产物,并在Shank3和SCN1A小鼠模型中显著改善行为缺陷和癫痫表型。此外,团队进一步开发了Cre表达显著降低的AAVLINK2.0,并系统构建验证了涵盖近200个大基因的递送资源库,为大基因缺失相关疾病的基因治疗提供了通用且具转化潜力的平台。

导读
尽管取得了上述进展,rAAV载体在基因治疗中的应用仍面临挑战,其中最主要的限制之一是其较小的包装容量(通常小于5kb),这显著限制了其对大基因的递送能力。为解决这一问题,研究者提出了多种策略。由于两种不同的rAAV载体可以共同转导同一靶细胞,大基因可被拆分为较小片段,分别由两个甚至三个载体递送;在共转导后,这些片段可在细胞内重组为全长基因或蛋白。目前用于AAV载荷重组的策略主要分为三类:DNA转剪接、RNA转剪接以及蛋白转剪接。然而,DNA和RNA层面的策略通常仅表现出中等或较低的重建效率;而蛋白转剪接则高度依赖正确的蛋白折叠和特定的拆分位点,同时未连接的蛋白片段持续存在,可能引发显性负效应。
在本研究中,研究团队开发了一种名为AAV with translocation linkage(AAVLINK)的方法,用于利用AAV递送超大基因载荷。该方法具有极高的重建效率、对多种拆分位点的优异灵活性,并且几乎不产生截短蛋白。研究团队利用AAVLINK成功挽救了Shank3和Scn1a突变小鼠的疾病表型。此外,AAVLINK还实现了多种基于CRISPR-Cas9工具的高效递送。为降低Cre潜在的毒性风险,本研究进一步构建了带有降解标签Cre的AAVLINK2.0系统。最后,研究团队建立了一个资源库,涵盖193个与遗传性疾病相关的大基因以及5种CRISPR工具。
研究结果
1. AAVLINK的设计与优化
为提高rAAV基因组重组效率,本研究利用位点特异性的Cre-loxP系统,实现rAAV基因组之间的精确分子间重组。双载体体系中,一个载体包含启动子、目标基因(GOI)5′端、剪接供体(SD)及lox位点;另一个载体包含启动子、Cre、嵌入人工内含子的lox位点、GOI 3′端及poly(A)信号。当两载体共同进入靶细胞后,首先产生Cre(步骤1),随后Cre介导重组将“GOI 5′端-SD”与“剪接受体(SA)-GOI 3′端”连接,并使Cre表达盒与SA及3′poly(A)分离,从而限制其后续表达(步骤2);最终经内含子剪接实现全长GOI的重建与表达(步骤3)(图1A)。
为降低Cre介导易位的可逆性,研究采用左右臂带突变的不对称lox位点(LE与RE)。LE与RE之间的重组会产生一个野生型loxP位点以及一个双臂突变的lox位点,使该结构不再被Cre识别,从而使易位在原则上不可逆(图1A、1B)。多组突变lox位点比较显示,loxJT15(LE)与loxJTZ17(RE)的组合具有最高的重组效率(图1B),并被用于后续AAVLINK设计。

图1. AAVLINK的设计与优化。
在AAVLINK体系中,GOI 5′端mRNA含未剪接SD且缺乏poly(A),而GOI 3′端作为Cre编码序列后的非翻译区转录,从而显著降低截短蛋白产生。实验结果显示,未检测到截短EYFP;EYFP表达在约60 h达到峰值并保持稳定,而Cre表达随后迅速下降至基础水平(图1C、1D)。进一步研究表明,拆分的EYFP经双AAVLINK载体递送后,仅在两载体共存且Cre存在时,才能在体外细胞和小鼠大脑皮层中观察到荧光信号;在食蟹猴大脑中亦获得一致结果(图1E–1G)。综上,这些结果表明AAVLINK能够在体内外高效重建被拆分的基因,并具备DNA重组高效、精准且副产物极少等优势。
2. AAVLINK实现三载体基因载荷的成功递送
为适配超出双载体容量限制的更大基因,本研究评估了三载体AAVLINK体系的有效性。该体系需要两对lox位点来组装被拆分的目标基因(GOI):第一对lox位点介导GOI 5′端与主体序列之间的重组;第二对lox位点在loxJT15和loxJTZ17臂突变的基础上引入lox2272间隔区突变,用于将GOI 3′端易位至主体序列下游,从而避免与携带野生型间隔区的lox位点发生交叉反应(图2A、2B)。
为验证该策略,研究团队将TagRFP基因拆分为三段并分别装载至AAVLINK载体中(图2C)。在HEK293T细胞中共转导后,重组DNA及其mRNA的测序结果证实全长TagRFP基因被精确重建;Western blot分析显示全长TagRFP蛋白高效表达,且未检测到截短产物(图2D)。随后,将三段TagRFP分别封装进三种rAAV并转导哺乳动物细胞,仅在三载体同时存在且Cre活性完整时检测到TagRFP信号(图2E)。体内实验同样表明,TagRFP可在小鼠及食蟹猴大脑皮层中被高效重建(图2F、2G)。
这些结果凸显了AAVLINK在递送超大基因方面的能力。单个rAAV基因组容量约为4.7 kb,在去除反向末端重复序列(ITR)、Cre及调控元件(如启动子、内含子和poly(A))后,三载体AAVLINK体系可递送约11 kb的遗传物质,覆盖了大多数与人类遗传性疾病相关的基因。
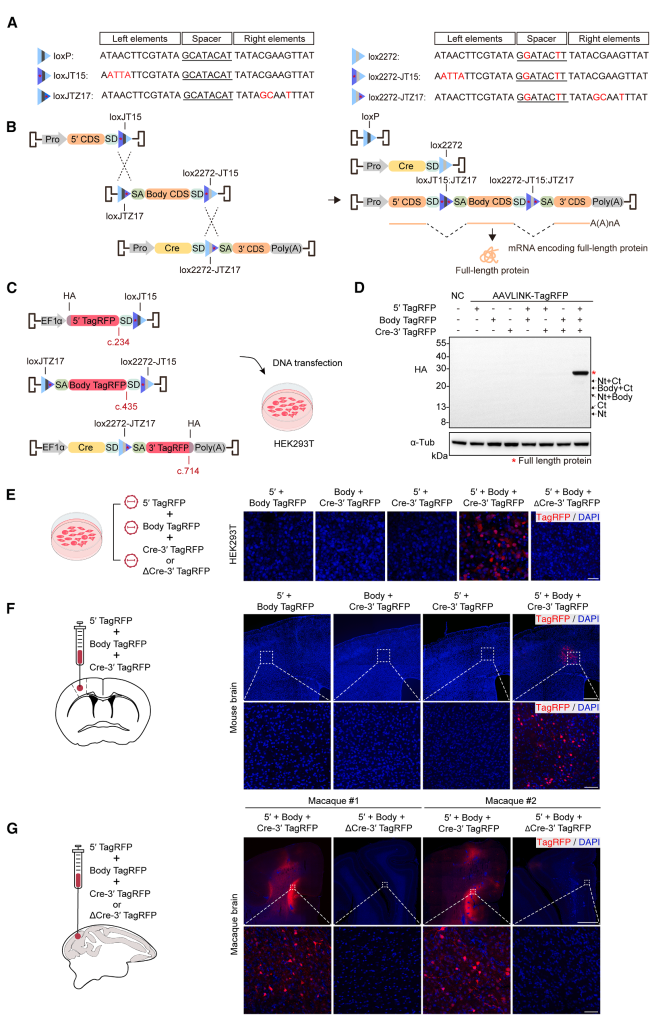
图2. AAVLINK介导的三载体基因载荷递送。
3. AAVLINK在蛋白重建效率上优于intein方法
研究团队将AAVLINK与常用的intein蛋白重建策略进行了系统比较。蛋白转剪接对拆分位点附近序列高度敏感,而AAVLINK对连接位点要求更为灵活,通常仅需一个共识外显子AG/G位点,且可通过同义突变进一步优化。
以荧光素酶为报告基因,在双载体体系中对10个拆分位点进行比较(图3A),AAVLINK在所有位点上均表现出更高效率,其最高信号较intein方法提高23.3±1.3倍,整体提高25.8±10.5倍(图3B、3C)。进一步分析表明,DNA重组效率随拆分位点变化,而RNA剪接对多数位点具有耐受性,二者共同决定了AAVLINK的蛋白产量。
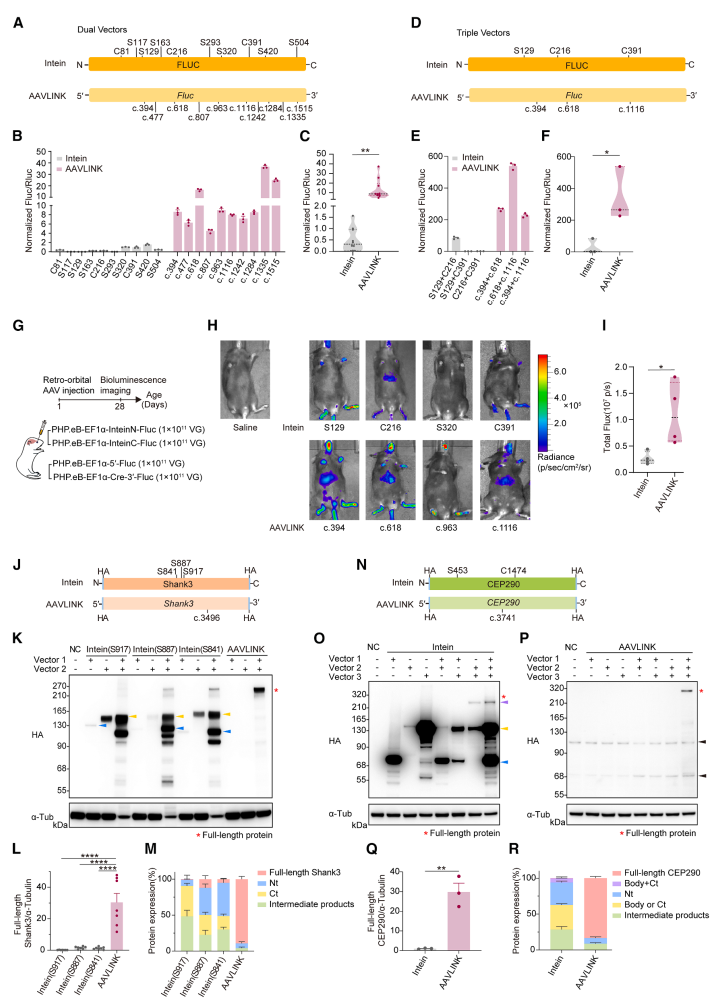
图3. AAVLINK与基于intein的蛋白重建方法对比评估。
在三载体体系中,AAVLINK同样显著优于intein方法。无论拆分设计如何,AAVLINK均实现更高的荧光素酶重建效率,平均生物发光信号提高245.5±156.7倍(图3D–3F),且全长蛋白比例更高、截短产物极少(图2D)。体内实验进一步验证了这一优势。采用相同拆分位点将携带拆分荧光素酶的rAAV注射至小鼠体内,4周后AAVLINK的整体效率约为intein方法的4.5±1.4倍(图3G–3I)。
在疾病相关大基因验证中,针对Shank3(5.4 kb),AAVLINK的重建效率较intein方法提高36.6±22.1倍,且几乎不产生截短产物(图3J–3M)。对于更大的CEP290(7.4 kb),三载体AAVLINK递送获得的全长蛋白占比达83.4%±2.4%,而intein方法仅为0.2%±0.1%(图3N–3R)。综上,这些结果表明,与intein策略相比,AAVLINK在大基因递送中具有显著更高的效率和更少的副产物,是一种高度有效的大基因递送方法。
4. AAVLINK介导的全长Shank3递送改善Shank3突变小鼠行为缺陷
为评估治疗潜力,研究团队首先利用AAVLINK在突变小鼠中表达Shank3。Shank3基因缺失会导致突触功能障碍和自闭样行为,而其重新表达可改善相关表型。
鉴于SHANK3基因体积较大,研究将其在c.3496位点拆分并分别封装至AAVLINK载体中(图4A),随后注射至4周龄Shank3*InsG3680+/+小鼠的纹状体(图4B)。4周后,检测到稳定的全长Shank3蛋白表达,并通过免疫染色确认其N端和C端完整性(图4C、4D)。功能上,接受治疗的小鼠刻板行为和运动能力缺陷显著改善(图4E、4F)。
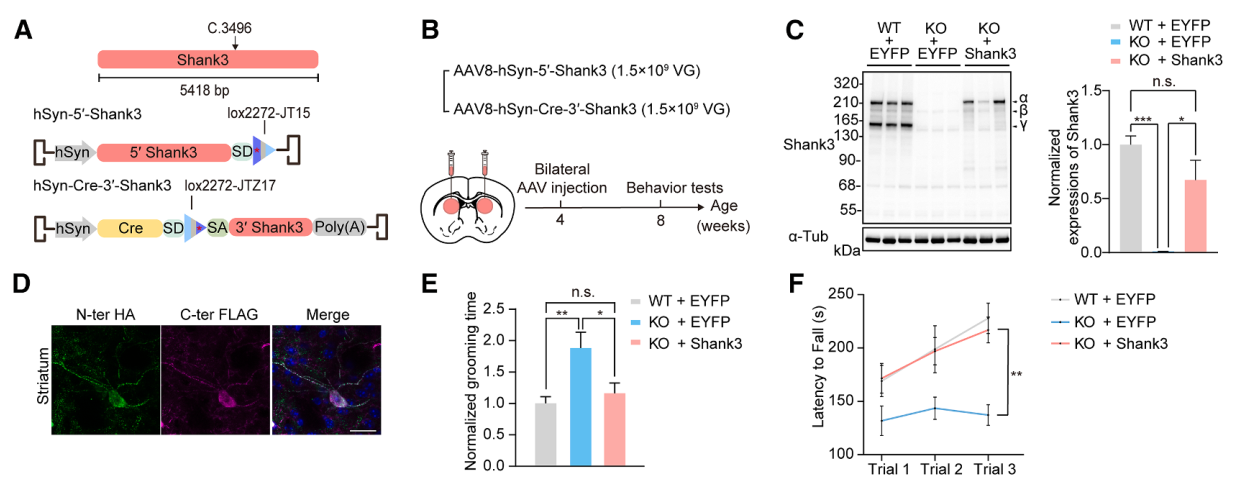
图4. AAVLINK介导的基因替代治疗在PMS和Dravet综合征小鼠模型中的应用。
5. AAVLINK介导的SCN1A替代缓解Dravet综合征小鼠癫痫表型
Dravet综合征主要由SCN1A半量不足引起。尽管SCN1A编码序列约6 kb,超过AAV载荷上限,但其单基因致病特性适合基因替代治疗。
本研究构建了Scn1a功能缺失小鼠模型,并观察到稳定的高热诱导癫痫和显著缩短的生存期。随后,将分别携带SCN1A 5′端或3′端的rAAV-PHP.eB通过眶后注射共同递送至Scn1a+/−小鼠(图4G、4H)。结果显示,Nav1.1蛋白在脑内被高效重建(图4I、4J),小鼠生存率提高,对高热诱导癫痫的耐受性增强(图4K)。进一步电生理分析表明,SCN1A替代可纠正海马锥体神经元的高兴奋性,恢复快速放电中间神经元功能,并显著减弱癫痫相关脑电活动(图4L–4P)。
总体而言,这些结果表明AAVLINK能够在体内稳健递送大尺寸治疗基因。尽管系统给药后脑内共转导效率相对有限,AAVLINK仍可实现足够的基因重建,从而产生明确的治疗获益。
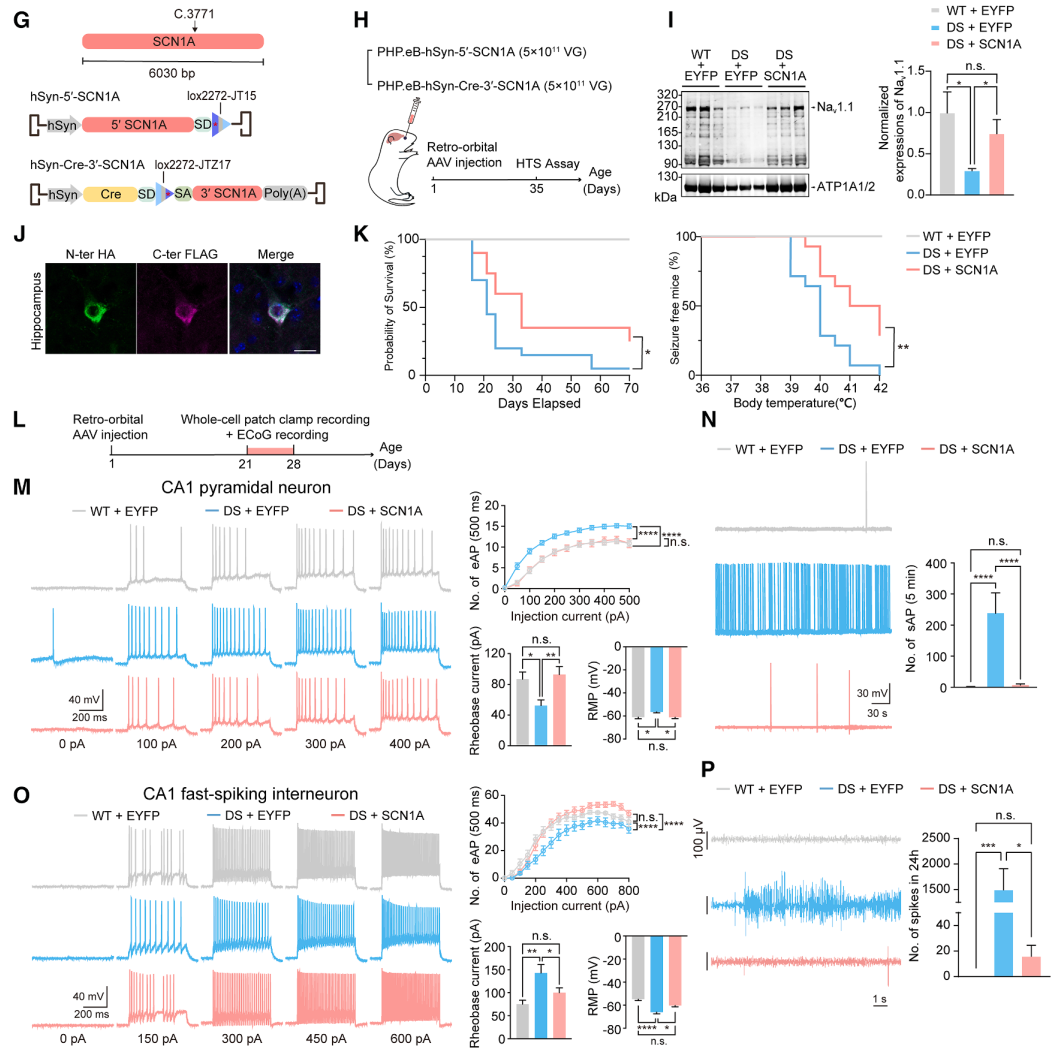
图4. AAVLINK介导的基因替代治疗在PMS和Dravet综合征小鼠模型中的应用。
6. AAVLINK促进CRISPR-Cas工具的高效递送
CRISPR-Cas技术在基因治疗中的体内应用受限于其相关基因体积较大,常超过单个AAV的包装容量。研究团队评估了AAVLINK递送多种CRISPR-Cas工具的能力。针对长度约4.3 kb的SpCas9,研究将其在c.2682位点拆分并装载至双AAVLINK载体中(图5A),在COS-7细胞中成功重建SpCas9,并实现了PSEN1基因片段的精确删除(图5B、5C)。
进一步地,研究利用AAVLINK递送两种大体积碱基编辑器ABE8e和YE1-BE4max,分别在c.2964和c.3540位点拆分并递送。在HEK293T细胞中,二者均实现高效蛋白重建,并在多个位点产生显著的A-to-G或C-to-T编辑,最高编辑效率可达80%(图5D–5F)。此外,AAVLINK还可递送基于失活Cas9的转录调控工具。拆分递送的CRISPRoff-V2显著抑制多种靶基因的表达,而dSpCas9-VPH则有效激活相关基因的转录(图5G–5I)。
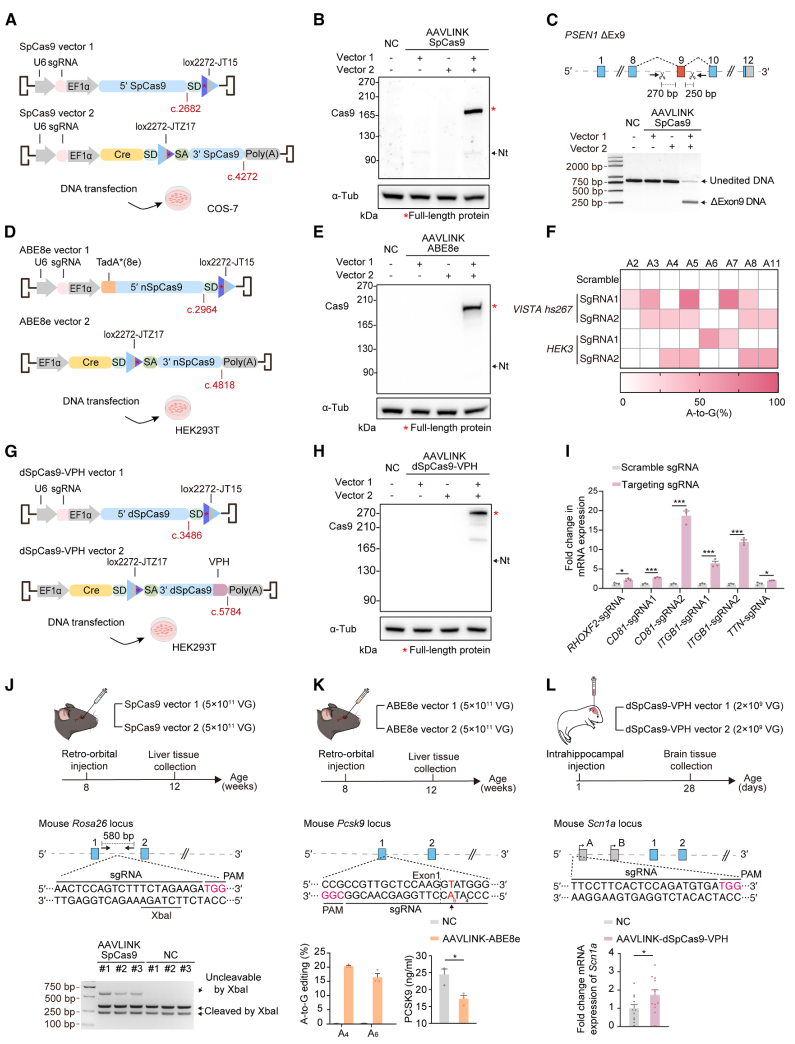
图5. AAVLINK介导的CRISPR工具递送。
在体内实验中,AAVLINK介导的SpCas9在小鼠肝脏Rosa26位点成功诱导双链断裂,验证了其体内重建能力(图5J)。同时,AAVLINK递送靶向Pcsk9的ABE8e在小鼠体内实现约16%的A-to-G编辑并降低Pcsk9表达;递送dSpCas9-VPH至海马区则上调Scn1a表达(图5K、5L)。总体而言,这些结果表明AAVLINK可在体内高效递送多种大型CRISPR工具,具有广泛的应用潜力。
7. AAVLINK2.0的开发以最小化Cre表达
外源性Cre表达在治疗应用中可能带来生物安全性风险。为进一步降低Cre水平,本研究在原有AAVLINK体系基础上引入多重优化策略(图6A)。首先,在HEK293T细胞中比较了6种不同强度的Cre驱动启动子,结果显示SCP1启动子在维持EYFP高效重建的同时,仅产生极低水平的Cre表达(图6B–6D),据此构建了AAVLINK1.1。
随后,研究通过缩短Cre蛋白半衰期进一步增强其瞬时性,在Cre C端融合不稳定化标签UDeg3a,使Cre在各检测时间点几乎不可检测,且不影响目标基因的重建效率(图6E–6G)。采用弱启动子SCP1并结合不稳定化Cre的体系被定义为AAVLINK2.0(图6A)。
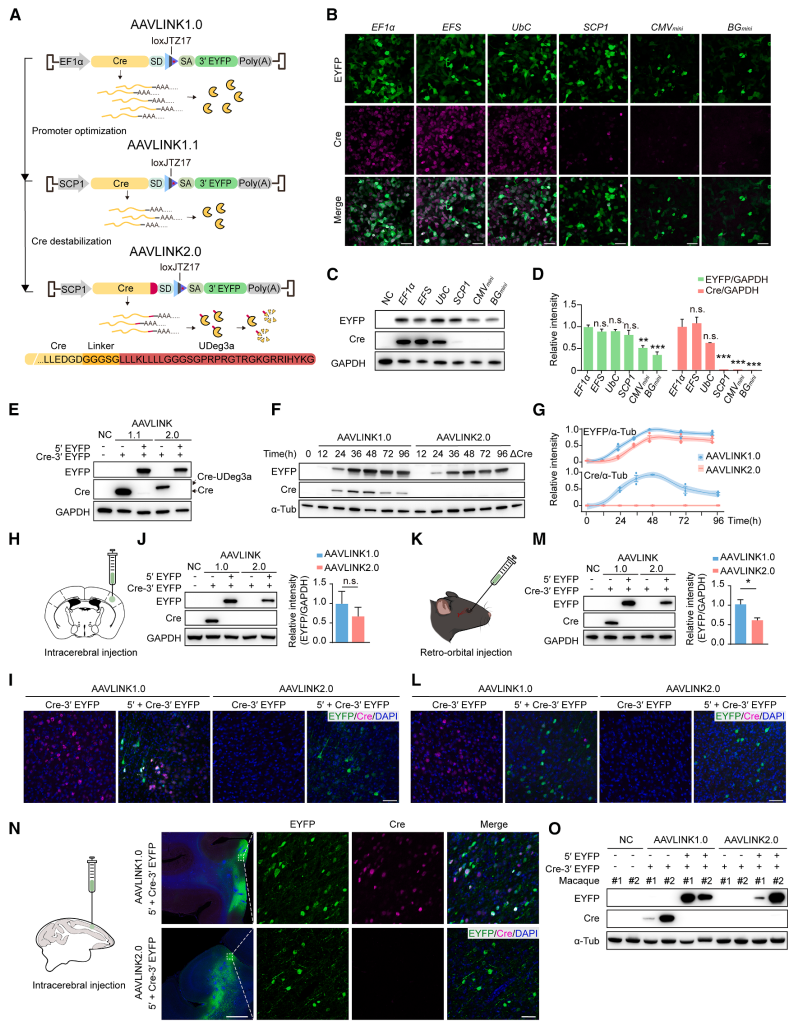
图6. AAVLINK2.0中Cre表达的最小化。
体内实验表明,经脑内或静脉递送后,AAVLINK1.0中Cre在IHC中仅呈弱信号而在WB中不可检测;而AAVLINK2.0在IHC和WB中均未检测到Cre表达,同时两种体系均可实现稳健的目标基因表达(图6H–6M)。类似结果亦在食蟹猴大脑中得到验证(图6N、6O)。
综上,这些发现凸显了AAVLINK2.0在生物安全性方面的显著优势,有效缓解了Cre表达相关的潜在风险,尤其提升了其在非人灵长类和临床转化中的应用前景。
8. 基于AAVLINK的大基因递送资源库构建
为进一步提升AAVLINK在大基因递送中的应用价值,本研究构建了一个面向遗传性疾病相关大基因的系统性资源库,重点聚焦自闭症谱系障碍(ASD)风险基因。之所以选择ASD相关基因,主要基于以下原因:(1)ASD具有显著的遗传学基础,且目前缺乏有效治疗手段;(2)多数单基因ASD病例由功能缺失(LoF)突变引起,适合开展基因替代治疗;(3)相当一部分ASD风险基因的编码序列长度超过4 kb。
研究团队系统检索了SFARI Gene数据库,克隆了所有长度大于4 kb的ASD相关基因,并同时纳入了27个与其他遗传性疾病相关的重要基因。其中包括AGL、ATP7A和OTOF,这些基因的LoF突变分别可导致糖原贮积症III型、Menkes综合征和感音神经性耳聋。根据基因长度,这些基因被拆分并分别装载至双载体或三载体AAVLINK体系中,随后在培养细胞中验证其在DNA和蛋白水平上的重建效果。
研究共将198个基因(其中193个为疾病相关基因,5个为CRISPR工具基因)克隆入AAVLINK1.0载体,随后全部升级为AAVLINK2.0格式以增强治疗适用性。Sanger测序证实,198个基因在HEK293T细胞中均实现了成功的DNA重组;其中192个基因的全长蛋白表达进一步通过Western blot得到验证(图7)。值得注意的是,大多数基因仅需单一拆分方案即可实现成功重建,体现了AAVLINK体系的稳健性。但不同拆分策略间的重建效率仍存在差异,这一现象与荧光素酶实验中的结果一致,提示对于部分基因,筛选最优拆分位点可能有助于获得最佳性能。
该资源库的总体信息,包括基因名称、基因长度及验证状态,总结见图7L和表S1。此外,研究团队还建立了专门的网站(http://AAVLINK.com/),以便研究者便捷获取相关详细信息。
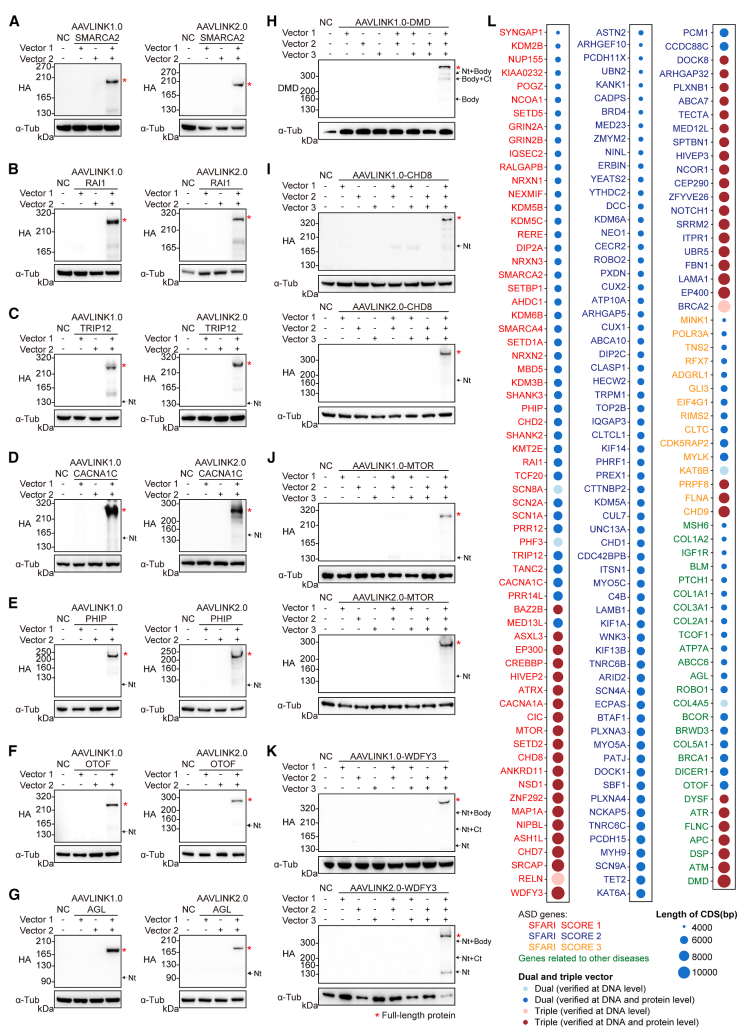
图7. 用于遗传性疾病相关大基因递送的AAVLINK资源库。
讨论
利用AAV载体递送超大基因是基因治疗领域中的一个关键研究方向。尽管已有多种策略被提出以应对这一挑战,但其在体内的成功率仍然有限,效果并不理想。在本研究中,研究团队提出了一种名为AAVLINK的策略,使AAV能够以高效且高度兼容的方式递送大载荷基因。AAVLINK的主要优势包括:(1)相较于基于intein的蛋白重建方法和StitchR策略,具有更高的重建效率;(2)截短副产物极少;(3)在拆分位点选择上具有更高的灵活性。此外,研究发现AAVLINK可在非人灵长类动物中高效重建被拆分的基因,显示出较强的转化应用潜力。
然而,AAVLINK在治疗应用中的一个关键限制在于Cre的表达。尽管Cre在载体间重组后可实现自我失活,但在未发生重组的Cre载体中仍可能出现一定程度的累积。为解决这一问题,研究团队开发了AAVLINK2.0,在保持稳健重建效率的同时,将Cre表达降低至Western blot不可检测水平,并在灵长类动物中验证了其改进后的生物安全性,进一步增强了其临床转化潜力。此外,研究还在培养细胞中验证了AAVLINK1.0和AAVLINK2.0对198个大基因的广泛适用性,其中大多数基因与ASD等半量不足性疾病或隐性单基因疾病密切相关。AAVLINK对这些基因的高效递送为相关疾病的基因治疗提供了新的可能。
AAVLINK递送全长Shank3和SCN1A基因分别挽救了Phelan-McDermid综合征(PMS)和Dravet综合征(DS)小鼠模型中的行为和癫痫表型。尤其是,纹状体中Shank3的替代治疗同时改善了刻板行为和运动障碍;而全长SCN1A的递送则显著降低了Scn1a突变小鼠的癫痫发作频率。AAVLINK对全长Shank3和SCN1A的成功递送,代表了PMS和DS基因治疗策略中的重要进展。其在多种CRISPR-Cas工具递送中的优异表现,也进一步凸显了该体系在临床转化中的应用潜力。
大基因的功能缺失突变是多种神经发育障碍的重要致病机制。对SFARI Gene数据库的分析显示,与ASD密切相关的功能缺失突变基因中,有37.5%的编码序列长度超过4 kb。基于此,研究团队构建了一个AAVLINK资源库,涵盖193个与疾病相关的大基因(其中166个为ASD候选基因,27个与其他遗传病相关)以及5种CRISPR工具,并验证了每个基因的DNA重组成功性,其中192个基因的全长蛋白表达也得到了确认。这一结果充分体现了AAVLINK在促进不同DNA分子重组方面的稳健性。
综上所述,本研究开发了AAVLINK这一高效的大基因递送方法,其有效性已通过数百个疾病相关基因和CRISPR工具的成功递送得到充分验证。
研究局限性
AAVLINK的效果仍有进一步提升空间。首先,所有拆分基因重建策略均依赖AAV的共转导,而在灵长类动物中经系统给药后的共转导效率相对较低。其次,基因拆分位点会影响AAVLINK的重建效率,其内在机制尚待深入研究。第三,AAVLINK1.0中用于疾病相关基因和CRISPRoff-V2的3′ CDS载体均采用pCALM1启动子以实现神经元特异性表达;若需要非神经元表达,可使用具有广泛表达特性的AAVLINK2.0(SCP1启动子),或根据需要引入自定义启动子。最后,对于需要细胞类型特异性表达或精确调控目标基因表达水平的应用,还需优化5′ CDS启动子的选择,因为该启动子在重建后是唯一发挥作用的转录调控元件。
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。