CAR-T细胞疗法自问世以来,已在血液肿瘤治疗领域取得了令人瞩目的成就。然而,随着该领域的不断发展,如何更安全、更高效地将CAR基因导入T细胞,成为制约行业进一步突破的关键瓶颈。
长期以来,慢病毒载体(Lentiviral Vector, LVV) 因其较高的转导效率和稳定表达能力,占据了CAR-T制造的主流地位。但随着技术的迭代演进,腺相关病毒(Adeno-Associated Virus, AAV) 在CAR-T领域的应用价值正逐渐被重新审视与发掘。
一、AAV应用于CAR-T细胞制备的优势
1. 安全性:更低的插入致癌风险
这可能是AAV最为核心的优势之一。慢病毒载体作为整合型载体,会将外源基因随机整合到宿主基因组中。这种随机整合有可能激活原癌基因或破坏抑癌基因,从而带来插入突变(Insertional Mutagenesis) 的风险,造成继发性恶性肿瘤的隐患。2024年10月,发表于《新英格兰医学》上的一篇文章表示,接受蓝鸟基因疗法eli-cel(商品名:Skysona)的67名患儿中,有7名患儿不幸患上血癌[1]。
野生型AAV主要以游离体(Episomal)形式存在,整合至宿主基因组的频率极低,从根本上规避了随机插入带来的致瘤风险。在经典的AAV-based CAR-T研究中,AAV更多被用作同源重组定向整合的供体模板(HDR donor template),配合CRISPR/Cas9等基因编辑工具,实现基因的定点精准插入 ,这种策略不仅避免了随机整合的风险,更能将CAR基因精准导入特定基因座(如TRAC位点),实现基因表达的生理性调控[2]。
此外,在监管角度方面,AAV已经在体内基因治疗领域已积累了大量的临床安全数据,监管机构对其安全性有着相对成熟的认知。
2. AAV的生产工艺和行业标准已相对成熟
在生物安全性方面,慢病毒载体的生产通常需要BSL-2+级别的生物安全设施,并对操作人员及环境防护有严格要求。AAV的生产虽然同样有规范要求,但其生物安全风险相对更可控(野生型AAV不致病,不能自主复制),更容易在现有GMP平台上进行整合。
在规模化生产方面,得益于过去十余年体内基因治疗产品(如Luxturna、Zolgensma)的推动,AAV的上游培养工艺(如HEK293悬浮体系等)、下游纯化工艺(如亲和层析+超滤等)、质量分析体系(如滴度、空满壳比、纯度检测等)均已建立起相对成熟的行业标准,可复用于CAR-T制备场景,加快产品开发节奏。
高质量的AAV载体是CAR-T制备成功的关键。作为专业的基因治疗服务商,派真生物深耕AAV制造领域,提供从科研级、小试中试到临床级(GMP)的AAV包装与生产服务。
我们拥有成熟的贴壁/悬浮细胞培养体系与超离/层析纯化平台,严格把控滴度、空壳率及内毒素等核心质控指标。无论您是进行早期靶点验证,还是推进IND申报,我们都能为您提供高滴度、高纯度、高安全性的AAV载体,助您大幅缩短CAR-T管线的研发周期!欢迎后台留言或联系销售经理获取定制化报价。
二、AAV在CAR-T领域的应用
1、通用型CAR-T(Allogeneic CAR-T)
目前市场上已获批的CAR-T产品(如Kymriah、Yescarta)均为自体CAR-T,存在制备周期长、成本高、患者等待风险大等固有局限。通用型(Allo)CAR-T 被视为下一代CAR-T的重要方向。
在工业界,通用型CAR-T最前沿的制造工艺正在从慢病毒随机插入向定点精准整合演进。这其中的标杆企业包括 CRISPR Therapeutics(如CTX110管线) 和 Caribou Biosciences(如CB-010管线)。其标准工艺路线是:使用电穿孔导入CRISPR/Cas系统进行基因座切割,同时使用AAV6作为高效率的递送载体,将CAR基因模板精准送入细胞核,实现TRAC位点的定点整合(图1)。 这证明了AAV(特别是AAV6)不仅在体内基因治疗中大放异彩,在Ex vivo的通用细胞工厂制备中,也是不可或缺的核心工具载体。
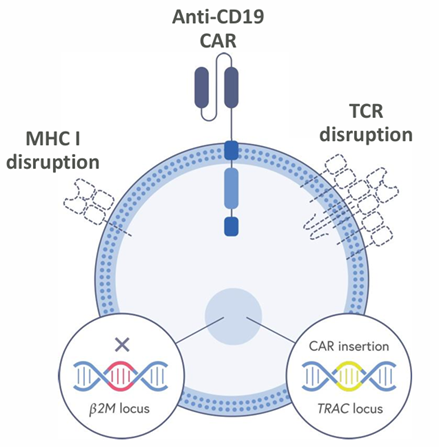
图1 CRISPR Therapeutics 公司的CTX110 同种异体抗CD19 CAR-T细胞疗法示意图。CTX110是一种”现货型”(off-the-shelf)同种异体CAR-T细胞产品,通过CRISPR/Cas9双基因敲除(TRAC和β2M)来降低免疫排斥和GvHD风险,同时利用AAV载体将CAR基因定点整合至TRAC位点,实现精准的基因工程改造。图片来源:https://ir.crisprtx.com/static-files/c1419057-b161-4335-a003-41ff46a44bdb
补充知识:通用型CAR-T制备时为什么不用价格更便宜的质粒(Plasmid)或裸露的线性 dsDNA来递送CAR基因?
要实现CAR基因的定点精准插入,光有CRISPR这把”剪刀”还不够——还必须同时提供一张写有CAR基因内容的”修复模板”,细胞才能按照模板把CAR基因精准抄写到指定位置。这个过程在分子生物学上叫做同源重组修复(HDR)。
最直觉的想法是:用实验室里便宜易得的质粒或裸露的线性DNA片段来充当这张”修复模板”。但这条路在原代T细胞上几乎走不通,原因有两个:第一,T细胞会把它当病毒来打。 T细胞是免疫系统里最警觉的”士兵”。当大量裸露的外源双链DNA被强行塞进T细胞时,细胞质里一套叫做cGAS-STING的天然”病毒探测器”会立即拉响警报,T细胞误以为被病毒入侵,随即启动自我毁灭程序,导致大量T细胞死亡,生产损耗极大。第二,就算侥幸存活,效率也极低。 为了减少毒性而降低质粒用量,进入细胞核的模板就不够用,定点整合的成功率通常不到10%,远不足以支撑GMP级别的规模化生产。
而AAV则完美绕开了这两个陷阱。AAV将单链DNA模板包裹在蛋白质外壳内,通过细胞表面受体”温和进入”T细胞,到达细胞核附近才释放模板,全程不触发任何免疫警报。因此,T细胞存活率可维持在80–90%以上,而定点整合效率也能飙升至40–70%。有文献报道,由于AAV携带的是单链DNA,其用于同源重组的效率比线性双链DNA高50倍以上[3]。这正是CRISPR Therapeutics(CTX110)和Caribou Biosciences(CB-010)等头部企业选择”CRISPR剪刀 + AAV6模板”黄金组合的根本原因。
2、In vivo CAR-T
如果说前文所述的AAV在通用型CAR-T中的应用,是对现有制造流程的”优化迭代”,那么AAV介导的in vivo CAR-T(体内直接生成CAR-T细胞),则代表着一场真正意义上的范式革命。
什么是 in vivo CAR-T?传统CAR-T的制备逻辑是:先把T细胞”请出”患者体内 → 在体外进行基因改造 → 再”送回”患者体内。这一流程复杂、昂贵、耗时,且高度依赖个体化定制。
In vivo CAR-T的逻辑则完全颠覆了这一范式:将CAR载体直接注射入患者体内,由体内的T细胞自主”接受改造”,就地变身为CAR-T细胞,直接发挥抗肿瘤或免疫调节功能。 这使其不再是”个性化细胞疗法”,而真正成为一种可规模化供应的”现货型基因治疗产品”。
为何AAV是 in vivo CAR-T的理想载体之一呢?与慢病毒、脂质纳米颗粒(LNP)等竞争平台相比,AAV在In vivo CAR-T中拥有几项独特的优势:
(1)临床安全记录成熟:目前全球已有9款FDA批准的AAV基因治疗产品(Luxturna、Zolgensma、Hemgenix等),监管机构对其安全性档案有充分认知,这为其进入In Vivo CAR-T的临床开发提供了显著的监管先发优势。
(2)能够递送大片段DNA模板:LNP善于递送mRNA,但对大片段基因组DNA模板(HDR供体)的核内递送能力有限;AAV则天然擅长将单链DNA模板精准送入细胞核,非常适合为CRISPR提供定点整合所需的供体序列。
(3)可进行衣壳工程改造,实现T细胞靶向:通过定向进化或理性设计,可将AAV衣壳精准改造为对T细胞(尤其是CD8⁺ T细胞)具有高度亲和力和特异性的靶向载体,从根本上解决野生型AAV嗜肝性带来的脱靶问题。
2023–2026年AAV在 in vivo CAR-T领域的关键进展:三项里程碑式研究
研究一:Ark313& Ark312——专为T细胞进化而来的AAV变体
来自美国UCSF的Eyquem 团队的 Ark313 系列工作与 Ark312 专利共同构成了在体内直接对 T 细胞进行基因工程的完整路线图。2023 年 ,其团队发表在Cell杂志的研究通过在 AAV6 衣壳可变区IV(VR-IV)进行7个氨基酸的随机插入,构建多样性文库,经三轮在原代小鼠 T 细胞上的定向进化,筛出 Ark313(图2),实现对小鼠T 细胞的高效转导与可控基因编辑,并揭示入胞机制依赖于非经典 MHC-I 分子 QA2(H2-Q7)及相关膜蛋白[4]。
![图2 ark313的筛选和验证过程示意图[4]](https://www.packgene.cn/wp-content/uploads/2026/03/图2-Ark313的筛选和验证过程示意图4.png)
图2 Ark313的筛选和验证过程示意图[4]
随后在 2025 年 Immunity 的工作中,单次静脉注射Ark313,在Ai9荧光报告小鼠中实现了最高22.9% T细胞的永久性遗传修饰,并揭示了关键机制差异:在体内静息naïve T细胞中,HITI策略的整合效率显著高于HDR(与体外激活T细胞中HDR优于HITI的结论相反)(图3),这一发现对于临床场景中靶向静息T细胞的策略设计具有重要指导意义[5]。
![图3 体内t细胞中大片段dna的靶向整合[5]](https://www.packgene.cn/wp-content/uploads/2026/03/图3-体内T细胞中大片段DNA的靶向整合5.png)
图3 体内T细胞中大片段DNA的靶向整合[5]。(A) HITI设计示意图,用于将mCherry报告基因靶向整合至Trac外显子1上游的内含子区域。报告基因两侧为剪接受体(SA)和牛生长激素(BGH)多聚腺苷酸化序列。在该系统中,mCherry表达仅在T细胞中发生整合时启动。(B) 使用HDR模板或HITI模板进行体内mCherry报告基因靶向整合的实验示意图。Cas9表达小鼠经尾静脉注射1×10¹² vg/只的Ark313(携带任一模板)或PBS。小鼠于注射后10天安乐处死,收集脾脏。(C) 注射PBS、Ark313-HDR或Ark313-HITI的小鼠脾脏中mCherry⁺ T细胞总数。mCherry表达通过流式细胞术检测。图中显示每组5只小鼠(n=5)的平均值±标准误。 (D) 注射PBS、Ark313-HDR或Ark313-HITI的小鼠脾脏mCherry⁺ T细胞中的T细胞记忆亚群。CD44和CD62L表达通过流式细胞术检测。CM,中央记忆型;EM,效应记忆型。 (E) Cas9小鼠注射PBS、Ark313-HDR或Ark313-HITI后,脾脏T细胞mCherry表达的流式细胞术检测结果。
作为对这一路线的扩展,Eyquem 团队在专利 WO2025179057 中提出 Ark312——在 ex vivo 进化得到的变体,专门设计以减少对造血干细胞等非靶组织的摄取、显著降低肝脏去靶向性,并与 enveloped delivery vehicles (EDVs) 相结合,将 Cas9/sgRNA 与 HDRT/整合模板一并高效、选择性地递送到人类 T 细胞(图4)。
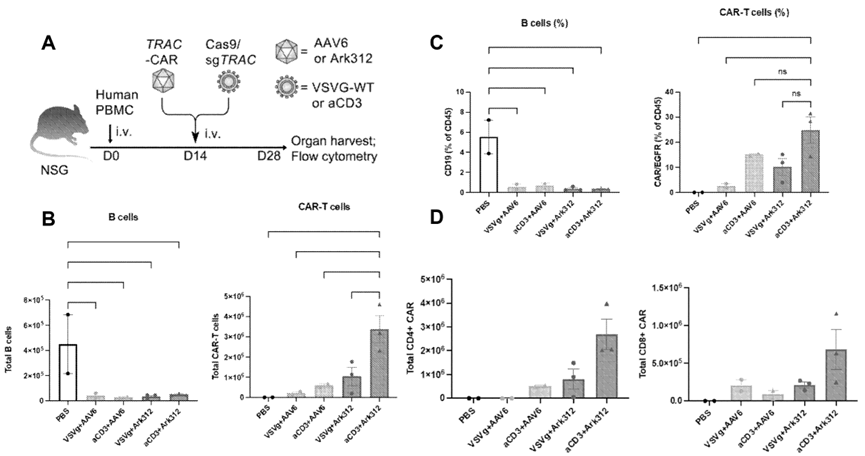
图4 EDV和AAV组合在体内生成TRAC靶向CAR T细胞的能力评估。使用人源化小鼠模型,在人PBMC移植14天后,小鼠接受了EDV和AAV组合或PBS(对照)的静脉注射,两周后,采集治疗小鼠的脾脏并通过流式细胞术进行分析。在所有四种EDV和AAV组合中均检测到CAR+ T细胞。WT-VSVG EDV和AAV6产生了约2×10⁵个CAR T细胞,而VSVGm-aCD3 EDV和Ark312产生了约3×10⁶个CAR T细胞(B)。虽然(1) VSVGm-aCD3 EDV和AAV6以及(2) WT-VSVG和Ark312两种组合产生的CAR T细胞数量均多于WT-VSVG EDV和AAV6组合(B),但VSVGm-aCD3 EDV和Ark312联合使用的改善效果超过了简单相加,提示两种载体联合使用时存在协同效应。这一观察结果在CD4和CD8 T细胞中均得到证实(D)。所有EDV和AAV组合均导致B细胞再生障碍(B-C)。这些结果证明了体内T细胞基因组编辑可产生能够杀伤靶细胞的CAR T细胞。
专利显示,Ark312 能在体外/体内实现对人 T 细胞的定向载荷递送、大载荷定点整合以及 TRAC-CAR、HIT、TRAC-TCR 等的体内/体外敲入,且在人体 PBMC 及人源模型中呈现出潜在的应用前景。
综合来看,Eyquem 团队的工作呈现了从体外筛选、到体内验证、再到人体应用的平台化发展路径,为体内直接改造 T 细胞、推动免疫治疗新范式提供了关键工具与策略。
研究二:DART-AAV——理性设计赋予CD8⁺ T细胞高度特异性
与Eyquem 团队的定向进化策略不同,来自德国Paul-Ehrlich-Institut 的 Christian J. Buchholz 团队的工作采用了理性设计(rational design)路线——将靶向人类或小鼠 CD8 的设计锚蛋白重复蛋白(DARPin)插入 AAV2 或 AAV6 衣壳蛋白 VP1 的 GH2/GH3 环(氨基酸 453–459),同时通过突变(AAV2:R585A/R588A;AAV6:V473D/K531E)消除原有受体结合位点(HSPG/唾液酸),将原有宽谱嗜性”致盲”,从而将病毒嗜性重新引导至 CD8+ T 细胞,开发出人鼠通用的CD8靶向DART-AAV平台[6]。
在复杂细胞混合物(人供者全血)中,CD8-AAV 较未改造 AAV2/AAV6 展现出大幅提升的 CD8+ T 细胞选择性,脱靶细胞中几乎无有效转导。在激活 T 细胞的人源化小鼠模型中,hCD8-AAV2 单次静脉注射后,血液中约 40% 的人 CD8+ T 细胞被转导,且特异性接近绝对(>99% 转导细胞为 CD8+)。在非激活 T 细胞的人源化小鼠模型中,未激活条件下转导率显著下降,但加入 IL-2/OKT3 激活T细胞后,脾脏中人 CD8+ T 细胞转导率可恢复至最高 80%。
在免疫完整鼠模型中,mCD8-AAV单独注射时转导率极低(<1%),经 IL-2+抗 CD3 激活T细胞后,mCD8-AAV6 在血液中转导率升至平均 16.4%,脾脏 8.8%,且对 CD8+ T 细胞的靶向特异性高达 >90%。与 AAV2/AAV6 相比,DART-AAV在肝脏的荧光信号大幅降低,实现了对肝脏的显著去靶向(图5)。
![图5 免疫健全小鼠中cd8特异性体内基因转移[6]](https://www.packgene.cn/wp-content/uploads/2026/03/图5-免疫健全小鼠中CD8特异性体内基因转移6.png)
图5 免疫健全小鼠中CD8特异性体内基因转移[6]。(A) Cre编码转移载体的基因结构(上图),以及Ai9 Cre报告小鼠基因组中loxP盒在重组前(中图)和重组后(下图)诱导tdTomato(tdt)表达的结构。(B-E) 雌性Ai9小鼠通过尾静脉注射接受1.7×10¹¹ vg/只的AAV2或mCD8-AAV2lL。第三组动物接受PBS作为对照。动物在注射后14天被安乐死(n = 6只/组)。肝脏的整体器官荧光通过IVIS测定(B)。(C) 显示了用AAV2或mCD8-AAV2lL处理的单只小鼠血液中tdT与CD8信号的代表性流式细胞术图。CD8+细胞中的转导效率以CD8+细胞中tdT阳性细胞的百分比确定(D),转导特异性以tdT+细胞中CD8+细胞的百分比确定(E)。(F-H) T细胞刺激后基因递送增加。雄性Ai9小鼠被分为五组。三组同时接受抗小鼠CD3和小鼠IL-2复合物,并通过尾静脉注射2×10¹¹ vg/只的AAV6(n = 4)、mCD8-AAV2lL(n = 4)或mCD8-AAV6lL(n = 4)。第四组接受PBS作为对照(n = 2)。第五组接受mCD8-AAV6lL但不进行体内T细胞刺激(mCD8-AAV6lL无[ w/o ]预处理)(n = 4)。(F) 显示了第2天血液中CD8+细胞tdT表达的代表性流式细胞术图。显示了血液中CD8+细胞的转导效率(以CD8+细胞中tdT阳性细胞的百分比确定)(G)以及血液和脾脏中转导特异性(以tdT+细胞中CD8+细胞的百分比确定)的图表(H)。BM,骨髓。
关键洞察: T细胞活化状态对体内转导效率有显著影响——活化的T细胞转导效率远高于静息T细胞。这提示未来临床方案中体内T细胞预处理(in vivo conditioning)策略的设计至关重要。
在实际生产中,DART-AAV的产量低(数据来源于PackGene科研生产中心),产量问题可能会成为阻碍DART-AAV临床应用的瓶颈。
研究三:AAV6-M2——首次在人源化小鼠中实现功能性in vivo CAR-T
这是目前最具临床转化里程碑意义的一项研究。2026年2月,来自西湖大学马丽佳和南京大学李颜联合团队的工作,首次证明了一种工程化AAV6变体AAV6-M2可通过全身注射在人源化免疫系统(HIS)小鼠模型中生成功能性人CAR-T细胞,并在自身免疫性疾病模型中展示出治疗效果[7]。
该研究的核心技术路线是在 AAV6 衣壳蛋白 VP3 的 VR VIII 区(氨基酸 A581–T593) 中随机插入来自公共数据库的功能性肽段(6–12 个氨基酸),构建了一个包含约 48 万种变体的多样性衣壳文库,随后以人类原代 T 细胞的转导效率为筛选指标,从中鉴定出顶级候选变体 AAV6-M1 和 AAV6-M2。
在体外验证阶段,AAV6-M2 对激活的人类 T 细胞展示出显著更高的转导效率,在 MOI 为 1×10³ 的条件下,EGFP⁺细胞比例达到 80.2%,与 AAV6 野生型在 10 倍更高 MOI 下的效果相当,且 3 升生物反应器中的规模化制备实验证实 AAV6-M2 的包装效率与野生型相当,具备临床制备的可扩展性。
为揭示 AAV6-M2 高效转导 T 细胞的分子机制,研究团队在 Jurkat-Cas9 细胞中开展了三个相互验证的全基因组 CRISPR KO 筛选,结合靶向基因敲除实验、冷冻电镜(cryo-EM)结构解析以及分子对接分析,共同确认 CD62L(L-selectin,naïve 和早期记忆 T 细胞的表面标志物)是介导 AAV6-M2 增强转导的关键宿主受体。CD62L 敲除细胞中 AAV6-M2 的转导效率显著下降,而这一缺陷在 CD62L 过表达后得到恢复。这一机制意味着 AAV6-M2 能在无需预激活的条件下直接转导静息 T 细胞,克服了此前其他工程化 AAV 变体普遍依赖 T 细胞预激活的局限性。
在体内功能验证方面,研究团队以 HIS-NCGX-IL15 人源化免疫系统小鼠为模型,通过静脉注射 3×10¹³ vg/kg 的 AAV6-M2-CD19CAR,在第 2、4、6 周持续检测外周血及多个器官中 CAR⁺ T 细胞的比例。结果显示,注射后 6 周,外周血及脾脏、骨髓、肺脏等多个器官中,人 CD8⁺ T 细胞中 CAR 阳性比例最高可达 77.5%,且 AAV6-M2 转导的细胞几乎全部局限于 T 细胞群体,对单核细胞、NK 细胞等其他免疫细胞群几乎无转导信号。在表型分析中,CAR⁺ T 细胞以效应记忆 T 细胞(TEM)为主,进一步支持 CD62L 在靶向 less-differentiated T 细胞中的核心作用。
在系统性红斑狼疮(SLE)模型 HIS 小鼠中,单次注射 AAV6-M2-CD19CAR 可有效清除外周血及组织中的人类 B 细胞(包括 Transitional B、Naïve B、Plasmablast 及 Memory B 各亚群),并显著改善狼疮相关病理表现,证实了体内生成的 CAR-T 细胞具有真实的功能性杀伤活性(图6)。安全性评估方面,与 AAV6 野生型及 AAV9 相比,AAV6-M2 在小鼠各器官中的病毒基因组拷贝数检测(qPCR)显示肝脏中的病毒累积水平降低超过两个数量级。
![图6 aav6 m2体内car t疗法在人源化狼疮模型中消除b细胞并改善sle症状[7]](https://www.packgene.cn/wp-content/uploads/2026/03/图6-AAV6-M2体内CAR-T疗法在人源化狼疮模型中消除B细胞并改善SLE症状7.png)
图6 AAV6-M2体内CAR-T疗法在人源化狼疮模型中消除B细胞并改善SLE症状[7]。a 实验设计。人源化HIS-HCG-M小鼠经R848处理诱导SLE样症状后,注射AAV6-M2-CAR。注射后8周收集组织。b 外周血中人B细胞随时间的定量分析。c、d 骨髓(c)和脾脏(d)中总B细胞计数。e 代表性肾脏免疫荧光图像显示SLE组和SLE+AAV组中的人IgG沉积(粉色)。下图提供对应上图中黄色方框标记区域的放大视图。f、g 血清抗dsDNA(f)和抗Smith(Sm)自身抗体(g)水平。h、i 肾脏损伤标志物BUN(h)和CREA(i)水平。j 代表性肺组织学显示SLE中的肺泡炎症及其经AAV6-M2治疗后的减轻。
在食蟹猴(cynomolgus macaque)的体内分布实验中(通过 NGS 定量),同样观察到肝脏病毒拷贝数比野生型 AAV 低约 100 倍,进一步验证了 AAV6-M2 的肝脏去靶向特性及其向非人灵长类动物应用的安全性基础。此外,研究还验证了 AAV6-M2 与携带 enAsCas12f/sgRNA 的第二个 AAV 载体组成的双 AAV 系统,可在体外实现 TRAC 位点的定向整合,为未来在同一步骤中完成基因组编辑与 CAR 敲入提供了技术路径。
研究意义: 据作者团队所知,这是目前已知首次证明单一AAV注射即可在体内产生持久、功能性人CAR-T细胞的研究,并成功将AAV-based CAR-T的应用范围从肿瘤延伸至自身免疫性疾病,极大扩展了该技术的治疗潜力。
派真生物不仅拥有强大的常规AAV生产能力,更提供专业的AAV血清型筛选与优化服务。我们可以协助客户进行新型AAV衣壳文库的构建、高通量筛选验证以及难包装血清型的工艺摸索。从序列设计到高滴度产出,我们为您攻克新型AAV的“量产”难关,让您的创新In Vivo CAR-T管线赢在起跑线上。
三、AAV应用于CAR-T领域尚待解决的关键科学问题
1. 重复给药:AAV预存抗体及注射后产生的中和抗体如何管理?免疫调节联合给药策略正在积极探索中。
2. 非整合的持久性:AAV基因组以游离体形式存在,随T细胞增殖而稀释,CAR表达的持久性仍是核心挑战;AAV+CRISPR双载体定点整合策略是重要解决方向。
3. 人源T细胞靶向的通用性:Ark313依赖鼠特异性QA2,开发对人T细胞具有广谱靶向能力的新变体(如AAV6-M2、DART-AAV)仍是核心工程任务。
4. 制造工艺的规模化:高剂量(10¹³ vg/kg量级)对AAV生产工艺提出了极高要求。
结语
AAV并非要全面”取代”慢病毒在CAR-T领域的地位,两者各有其适用场景。但随着精准医学和通用型CAR-T需求的持续增长,AAV——尤其是作为CRISPR基因编辑的供体递送工具——正在成为下一代CAR-T制造平台中不可或缺的核心组件。其在安全性、定点整合精准性、通用型产品适配性等维度的独特优势,使其具备了支撑CAR-T疗法从”个体化定制”走向”规模化货架产品”的巨大潜力。
参考资料
1. Duncan CN, et al.Hematologic Cancer after Gene Therapy for Cerebral Adrenoleukodystrophy. N Engl J Med 2024;391:1287-301.
2. Eyquem J, et al. Targeting a CAR to the TRAC locus with CRISPR/Cas9 enhances tumour rejection. Nature. 2017;543:113–117.
4. Nyberg WA, et al. An evolved AAV variant enables efficient genetic engineering of murine T cells. Cell. 2023;186:446-460.e19.
5. Nyberg WA, Wang CH, Ark J, et al. In vivo engineering of murine T cells using the evolved adeno-associated virus variant Ark313. Immunity. 2025;58:499–512.
6. Demircan MB, Zinser LJ, Michels A, et al. T-cell specific in vivo gene delivery with DART-AAVs targeted to CD8. Molecular Therapy. 2024;32:3470–3484.
7. Lu Z*, Ni K*, Liu W*, et al. An AAV variant enables human T cell engineering in vivo. Vitae. 2026. https://doi.org/10.15302/vita.2026.01.0008
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。