全球约有4.3亿人受致残性听力障碍困扰,其中2600万为先天性耳聋患者。遗传性因素约占先天性耳聋的60%。以助听器和人工耳蜗为代表的传统干预手段仅能”补偿”功能,而腺相关病毒(adeno-associated virus, AAV)介导的基因治疗正在将”治愈”变为可能。本文系统梳理AAV内耳应用的核心要素,涵盖靶细胞生物学、血清型选择、启动子策略、给药途径及代表性临床转化案例,旨在为内耳基因治疗研究者提供切实可行的实验决策参考。
一、精密的“声音处理器”:内耳结构与靶细胞生物学
1.1 内耳的解剖结构
耳朵分为外耳、中耳和内耳三部分(图1)。外耳包括耳廓和耳道,负责搜集声音。中耳由鼓膜、鼓室及听小骨组成,负责放大声音。内耳位于颞骨岩部深处,由感知声音的耳蜗(cochlea)和感知运动/重力的前庭系统(vestibular system,包括椭圆囊、球囊和三个半规管)组成。耳蜗呈蜗牛状螺旋结构,内部由骨螺旋板和蜗轴分隔为三个充满淋巴液的腔隙:
前庭阶(Scala vestibuli):充满外淋巴(perilymph),与镫骨底板相接
鼓阶(Scala tympani):充满外淋巴,终止于圆窗膜
蜗管(Scala media / Cochlear duct):充满内淋巴(endolymph),K⁺浓度高达150 mM,维持约+80 mV的内淋巴电位(endocochlear potential, EP)
⚠️ 注意:外淋巴与内淋巴的离子成分截然不同。经圆窗膜注射的AAV载体进入外淋巴腔(鼓阶),需穿越螺旋板才能进入蜗管并接触毛细胞的顶面。这一屏障结构是影响内毛细胞转导效率的重要物理限制因素,在实验设计时不可忽视。
1.2 核心靶细胞
基因治疗的靶向精准性取决于对内耳细胞类型的深入理解。
毛细胞(Hair Cells, HCs) 是感音的核心效应细胞,分为两类:
- 内毛细胞(Inner Hair Cells, IHCs):沿耳蜗走行单排排列,约3,500个/人。通过机械-电转导将声音振动转化为神经递质(谷氨酸)释放,驱动螺旋神经节神经元放电,是声音信号传入神经系统的唯一通道。DFNB9型耳聋(OTOF基因突变)即因IHC突触功能障碍所致。
- 外毛细胞(Outer Hair Cells, OHCs):沿耳蜗走行三排排列,约12,000个/人。通过prestin蛋白(由SLC26A5编码)驱动的电致运动(electromotility)对声音信号进行主动放大,是耳蜗灵敏度和频率分辨率的关键。OHCs对噪声、耳毒性药物及遗传缺陷极为敏感。SLC26A5突变所致OHC功能障碍是感音神经性耳聋的重要原因之一。
关键点:哺乳动物(包括人类)的毛细胞终生不可再生。一旦损伤,即造成永久性听力损失。这正是基因治疗——尤其是在细胞死亡发生之前介入——具有不可替代价值的根本原因。
支持细胞(Supporting Cells, SCs) 包围并支持毛细胞,维持内耳微环境稳态。其功能远不止”支撑”:
- 柱细胞(Pillar cells)和指细胞(Deiters’ cells)构成柯蒂氏器的机械骨架
- Hensen细胞、Claudius细胞参与内淋巴离子稳态维护
GJB2(编码Connexin 26)主要在支持细胞中表达,其突变是全球最常见的遗传性耳聋原因(约占隐性遗传性耳聋的50%)。支持细胞也是毛细胞再生研究中关键的”前体细胞”靶标(通过Atoh1等转录因子的转分化策略)。
血管纹(Stria vascularis) 位于耳蜗侧壁,由边缘细胞、中间细胞和基底细胞构成,负责将K⁺分泌入内淋巴,维持内淋巴电位。KCNQ1/KCNE1、KCNQ4等离子通道基因在血管纹细胞中高表达,其功能障碍可导致内淋巴积水型耳聋。
螺旋神经节神经元(Spiral Ganglion Neurons, SGNs) 是初级听觉传入神经元,分为Ⅰ型(占95%,与IHC形成突触)和Ⅱ型(占5%,与OHC形成突触)。SGN在耳蜗退变、人工耳蜗植入及听神经病(auditory neuropathy)等病理过程中具有中心地位,也是神经保护性基因治疗的重要靶点。
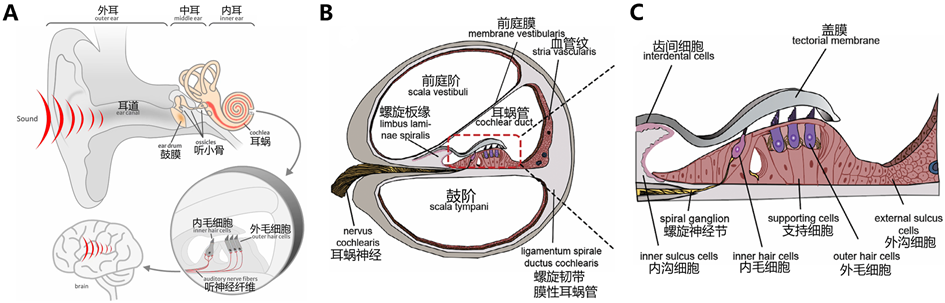
图1. 耳的结构。A) 声音在耳内的传导过程。B) 耳蜗的解剖结构。C) 柯蒂器(organ of Corti)结构的放大示意图。图片来源:https://www.audiocure.com/how-we-hear/;https://doi.org/10.1002/advs.202402166
二、选择“导航车”:AAV血清型的内耳靶向性
选择合适的AAV血清型是实现高效、特异性基因递送的第一步。不同的血清型对内耳不同细胞的亲和力差异显著,且存在明显的年龄依赖性和物种差异性。以下表格综合了近年文献数据,提供AAV血清型选择参考(数据主要来源于小鼠模型)。

AAV血清型选择的决策流程
选择时需系统考量以下维度:
① 确定靶细胞类型
感觉毛细胞(IHC+OHC)广泛转导 → Anc80L65(新生)或 AAV2.7m8(跨年龄)
仅IHC → AAV-ie(新生/临床转化)或 AAV9/AAV-PHP.eB(年龄依赖)
支持细胞 → AAV-ie 或 AAV-KP1
SGN → Anc80L65 或 AAV-PHP.eB(限小鼠)
血管纹/侧壁 → AAV8BP2
② 明确动物模型与年龄
新生小鼠(P0–P5)→ Anc80L65、AAV-ie、AAV2.7m8均可
成年小鼠 → AAV2.7m8 或 AAV-ie;
非人灵长类 → AAV-S;
③ 评估临床转化需求
已有临床数据 → AAV2.7m8(AAV2变体,眼科临床试验NCT03326336)
人源组织验证 → AAV-ie
已进入临床耳科试验 → AAV1(DFNB9研究,见案例二)
④ 结合启动子策略 → 详见第三节
三、安装“精准开关”:启动子与调控元件的选择策略
血清型决定”能进哪扇门”,启动子决定”进门后在哪里开灯”。为实现基因在特定细胞中的精准、高效表达,启动子与增强子的选择至关重要,同时需兼顾AAV的包装容量限制(~4.7 kb,含ITR)。
3.1 主要启动子及其特性

3.2 增强子工程:突破传统启动子的局限
天然启动子在”特异性”与”表达强度”之间往往存在矛盾——广谱强启动子(CAG)表达高效但脱靶严重,细胞特异性启动子(如天然Myo15a)精准但表达强度往往不足。增强子工程提供了新的解决方案(详见案例二):通过解析内源性调控元件(conserved non-coding elements, CNEs)并进行模块化重组,可以构建兼具高特异性和高表达强度的合成增强子(如B8增强子),从而超越单一启动子的局限。
3.3 启动子选择建议
- 追求强力广泛表达(基础研究/概念验证):CBA或EF1α
- 毛细胞特异性靶向(治疗应用):Myo15a(包装容量充足时)或截短Myo15a(容量受限时)
- 支持细胞靶向(毛细胞再生):GFAP
- SGN靶向:Syn1
- 精准OHC特异性高效表达:考虑增强子工程策略(如B8类合成增强子)
⚠️ 包装容量警示:AAV的有效包装容量约为4.7 kb(含两端ITR各0.145 kb,实际可用约4.4 kb)。若目标基因较大(如OTOF 5.9 kb、MYO15A ~11 kb),必须使用双AAV载体系统并优先选用截短/小型启动子。过大的包装物会显著降低AAV产量和感染效率。
四、打通“最后屏障”:内耳给药途径与操作规范
内耳的给药途径直接影响AAV载体的分布和转导效率。由于内耳解剖位置深邃、体积微小且结构脆弱,给药方式的选择须兼顾有效性、安全性和临床转化潜力。
4.1 主要给药途径对比
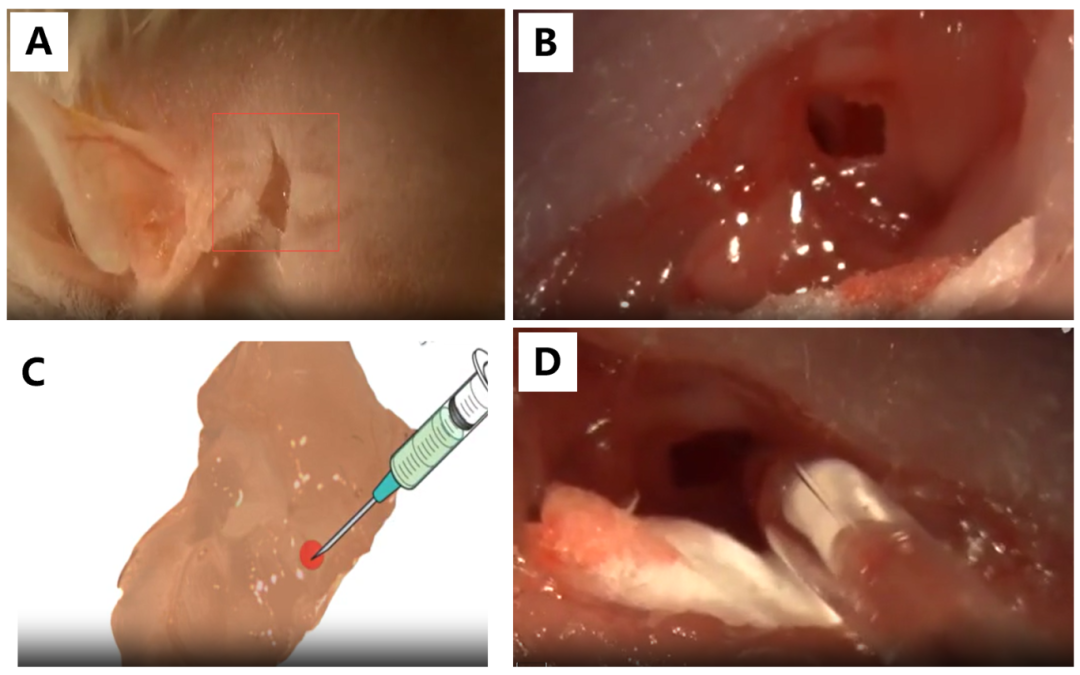
小鼠圆窗膜注射。在耳廓后方做一切口,暴露胸锁乳突肌,向两侧分离,暴露颞骨;用硼硅酸盐玻璃微管轻柔穿刺圆窗膜中心。图片来源于文献:Akil O, et al.( 2015). Surgical Method for Virally Mediated Gene Delivery to the Mouse Inner Ear through the Round Window Membrane. J Vis Exp. 16;(97):52187. doi: 10.3791/52187.
注射.png)
新生鼠后半规管(PSCC)注射。图中展示的是左耳。黑色虚线表示后半规管。图片来源于文献:Isgrig K & Chien WW. (2018). Posterior Semicircular Canal Approach for Inner Ear Gene Delivery in Neonatal Mouse. J Vis Exp. 2;(133):56648. doi: 10.3791/56648.
4.2 参考剂量与注射体积
以下数据是基于文献报道的有效范围,正式实验前必须通过预实验(pilot study)进行个体优化:
注射体积:
- 新生/幼年小鼠(P0-P7): 0.5 – 1.5 µL/耳
- 成年小鼠(>P21): 1.0 – 2.0 µL/耳
病毒剂量:
- 基础研究(报告基因):1×10¹⁰ – 1×10¹¹ vg/耳
- 基因治疗(功能恢复):5×10¹⁰ – 5×10¹¹ vg/耳(参见案例一、二的剂量数据)
临床试验参考(人):
DFNB9双侧治疗:1.5×10¹² vg/耳,体积50 µL,注射速率120 nL/min(案例二)
⚠️ 剂量安全警示:过高的AAV剂量或注射体积可能直接损伤毛细胞,导致听力下降和ABR阈值升高。这一效应与AAV毒性、注射压力(引起内淋巴液压骤变)均有关。建议梯度剂量预实验,并以ABR/DPOAE监测听力功能变化作为安全终点。
4.3 操作规范要点
- 所有内耳注射操作须在严格无菌条件和精确麻醉深度下进行
- 新生小鼠(P0–P3)建议低温麻醉(冰板冷却);P4以上可使用异氟烷
- 注射速率建议控制在50–150 nL/min,避免压力性损伤
- 术后需给予镇痛(如布洛芬)和抗炎(皮质激素视需要)处理
- 术后3–7天密切监测动物体重、行为(前庭功能:转圈、偏头等)
- ABR和DPOAE评估应在手术前(基线)、注射后2–4周(早期)和4–8周(稳态表达)分别进行
五、代表性应用案例
案例一:遗传性耳聋的基因治疗
2025年8月5日,复旦大学附属眼耳鼻喉科医院舒易来教授团队与韩国首尔大学医院Sangsu Bae、Sang-Yeon Lee科研团队合作在国际期刊Nature Communications上发表题为“PAM-flexible adenine base editing rescues hearing loss in a humanized MPZL2 mouse model harboring an East Asian founder mutation”的研究论文,利用PAM灵活型腺嘌呤碱基编辑器(ABE8eWQ-SpRY)结合高效的内耳靶向AAV递送,精准修复东亚人群高发的MPZL2 c.220C>T创始突变,在人源化小鼠模型中显著恢复听力,并维持至少20周。

该研究的主要研究结果:
1. 东亚特异性MPZL2基因突变在DFNB111相关听力损失中的临床意义
研究团队基于临床队列研究,对遗传性耳聋1437例无亲缘关系的耳聋家系进行了系统性病因学分析。筛选出234例表现为对称性、轻中度非综合征型SNHL未成年患者(≤18岁),明确了155例患者的致病基因(66.2%)。其中24例与MPZL2基因突变有关(15.5%),且23例(95.8%)患者携带至少一个c.220C>T等位基因突变。c.220C>T等位基因在东亚人群中频繁出现,提示该突变可能为东亚地区的创始突变。
2. 人源化MPZL2 c.220 C > T小鼠的构建以及表型描述
针对该突变位点,研究团队构建了人源化小鼠模型(hMPZL2Q74X/Q74X),该小鼠模型表现为进行性听力损失,重现了人类MPZL2耳聋病人的听力学表型:渐进性低至中度听力损失,且有着比较明显的内耳毛细胞的丢失。
3. 基于ABE的基因治疗体系的体外筛选
针对该突变的A·T→G·C精确修复,研究团队评估了14种ABE与sgRNA组合,最终确定PAM几乎无限制的ABE8eWQ-SpRY:sgRNA3为最佳方案,该方案具有较高的体外编辑效率(约50%以上),较低的旁观者编辑和脱靶效应。
4. AAV递送策略、治疗效果及安全性评价
为突破AAV单载体容量限制,研究者采用了split-intein双AAV系统(图2)。通过圆窗膜显微注射,结果显示:
- 听力改善:治疗组在多频段ABR阈值显著下降,8 kHz接近野生型水平,效果可持续20周
- 结构恢复:外毛细胞与Deiters细胞数量明显回升,耳蜗结构完整性改善。
- 分子水平:MPZL2 mRNA与蛋白表达恢复,相关细胞黏附与细胞外基质通路基因回归正常水平。
- 安全性:未检测到明显的脱靶效应或耳毒性,非耳蜗组织几乎无病毒分布。
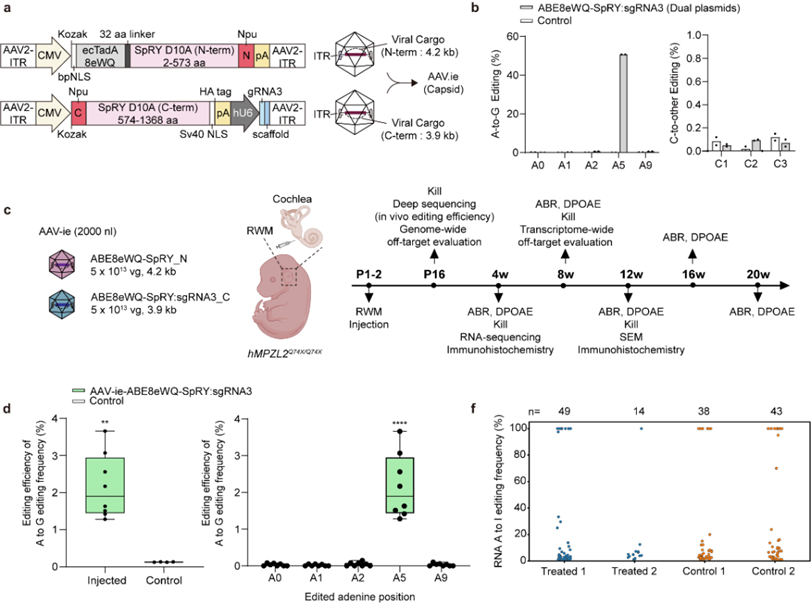
图2. 双 AAV-ie-ABE8eWQ-SpRY:sgRNA3 体内修复 MPZL2 c.220 C>T 突变。a 用双 AAV 载体及分裂内含肽在体内递送ABE的示意图。b MPZL2靶点腺嘌呤及周围旁观腺嘌呤或胞嘧啶的编辑效率评估(n=2)。c 体内碱基编辑流程概览,将两个AAV-ie病毒重悬至 5.0×10¹³ vg/mL,1:1混合。取2000 nL 注射至P2 期 hMPZL2Q74X/Q74X 小鼠圆窗膜(RWM)。d 柯蒂氏器官 DNA 中靶位点 A·T→G·C 编辑效率及周边核酸旁观效应。e Cas-OFFinder 预测的潜在体内脱靶位点,包含与靶序列 ≤2 bp 错配及/或 ≤1 bp DNA/RNA bulge 的位点。f 双 AAV-ie-ABE8eWQ-SpRY:sgRNA3 注射后 8 周,体内 RNA 脱靶检测。检测结果显示无 RNA 脱靶编辑。

案例二: 增强子工程:AAV内耳递送的表达效率与特异性优化策略
2025年4月21日,上海科技大学钟桂生研究团队在Neuron发表题为“Deciphering enhancers of hearing loss genes for efficient and targeted gene therapy of hereditary deafness”的研究成果。该研究创新性建立了基于AAV报告载体的体内转录增强子重构(ARBITER)技术平台,系统解析了调控听损基因Slc26a5表达的功能性保守非编码元件(CNEs),并证实这些增强子通过协同作用介导Slc26a5的精准时空表达。

文章的背景与核心问题:遗传性耳聋基因治疗面临双重矛盾,广谱强启动子(如CAG)表达效率高,但脱靶表达(在IHC、前庭细胞、脑组织中异位表达)带来安全隐患;天然细胞特异性启动子精准但表达强度不足,无法驱动足够的蛋白水平以恢复功能。能否在不牺牲特异性的前提下,通过解析和工程化改造内源调控元件来显著提升基因治疗效率?
实验设计拆解:
1. 开发核心研究工具:ARBITER平台
研究团队针对内耳细胞数量极少(全耳仅~15,000个毛细胞)、传统ChIP-seq/ATAC-seq所需细胞量难以满足的瓶颈,开发了ARBITER(AAV-Reporter-Based In vivo Transcriptional Enhancer Reconstruction)平台:基于已发表的ATAC-seq/ChIP-seq数据及跨物种保守性分析(CNEs),识别目标基因座附近的潜在调控元件。将候选序列克隆至含最小启动子和报告基因(mNeonGreen)的AAV载体,经圆窗膜注射至新生小鼠耳蜗,2周内完成荧光成像定量,评估转导效率、细胞特异性和表达强度(图3)。
2. 鉴定并验证关键增强子:以Slc26a5为例
SLC26A5编码OHC特异性马达蛋白prestin,其敲除导致OHC电致运动丧失和严重听力损失(~50 dB阈值升高)。
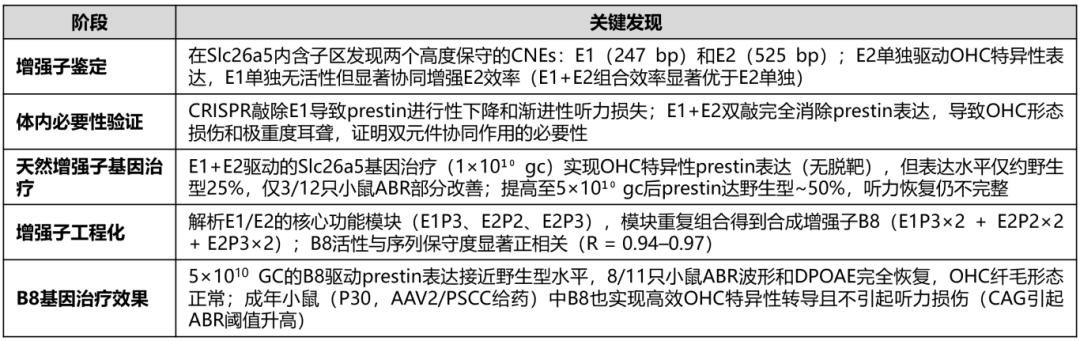
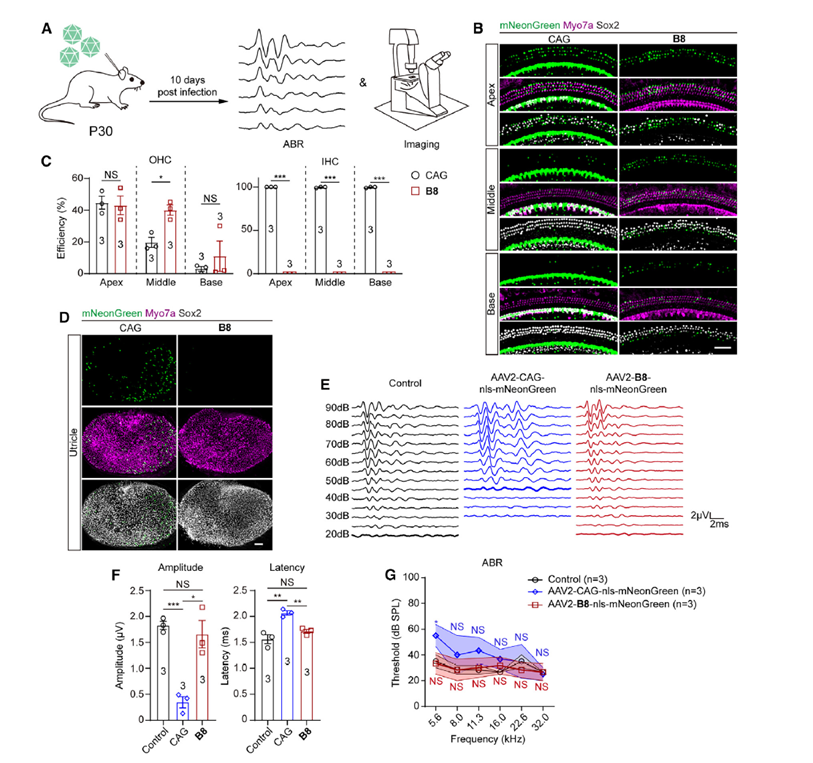
图3. B8增强子对成年小鼠OHCs的安全特异性转导
对AAV内耳研究的启示
案例三:双耳聆听的曙光:AAV基因治疗成功恢复DFNB9儿童双侧听力
2024年6月5日,复旦大学附属眼耳鼻喉科医院舒易来和王武庆团队在国际期刊Nature Medicine上发表了题为Bilateral gene therapy in children with autosomal recessive deafness 9: single-arm trial results的研究论文。该研究的核心问题是:评估一次性地通过双侧耳蜗注射基因治疗药物AAV1-hOTOF,在患有常染色体隐性遗传性耳聋9型(DFNB9)的儿童患者中的安全性和有效性。

疾病背景:DFNB9型耳聋(常染色体隐性遗传性耳聋9型)由OTOF基因双等位基因突变所致,导致耳铁蛋白(otoferlin)功能缺陷。Otoferlin是IHC突触囊泡胞吐(exocytosis)的关键钙感受器,其缺失导致IHC突触功能完全丧失,表现为听神经病(auditory neuropathy spectrum disorder)——耳蜗毛细胞形态相对正常,但神经传导功能丧失,ABR无法引出。DFNB9约占遗传性耳聋的2–8%,目前除助听器和人工耳蜗外无有效治疗手段。
临床试验设计
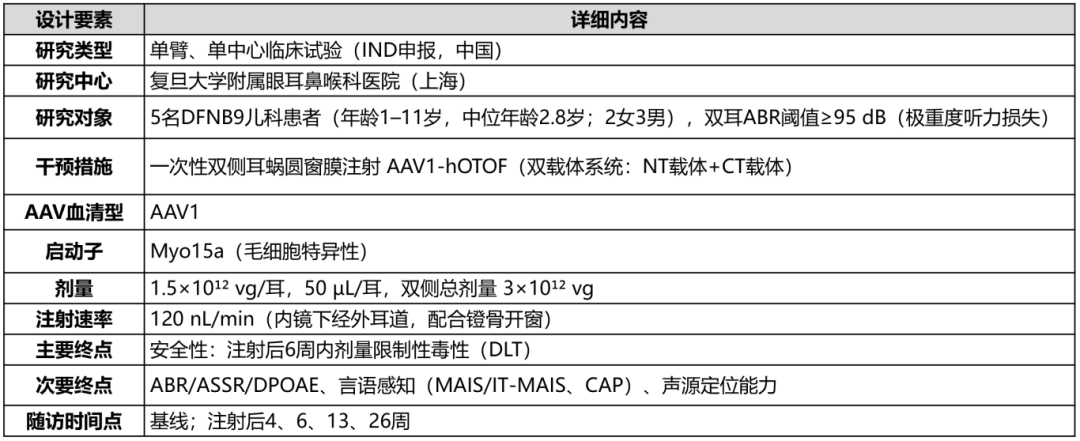
载体工程设计要点:双AAV策略
OTOF基因全长cDNA约5.9 kb,远超AAV单载体约4.4 kb的有效包装容量。研究团队采用经过临床前验证的双载体重叠重组策略:
AAV1-hOTOF-NT:携带基因5’端(N端序列)及重叠重组序列(源自F1噬菌体的AK序列)
AAV1-hOTOF-CT:携带基因3’端(C端序列)及重叠重组序列
两载体同时进入同一细胞后,通过同源重组在细胞内拼接为完整功能性OTOF mRNA
工程化亮点:Myo15a启动子确保otoferlin仅在毛细胞中表达,在实现容量突破的同时维持靶向精准性。这一”分而治之+精准靶向”的组合策略,为所有编码序列超出AAV容量的大基因疾病提供了重要参考(如DMD、USH2A等)。
主要结果
1. 安全性结果
- 无剂量限制性毒性(DLT),无严重不良事件(SAEs)。
- 共发生36次不良事件,均为1级或2级(轻度至中度)。最常见的是淋巴细胞计数增加(6/36)和胆固醇水平升高(6/36),所有不良事件均得到缓解。
- 治疗后6周,所有患者均检测到抗AAV1中和抗体(滴度1:1215),但针对AAV1衣壳的T细胞免疫反应(IFN-γ ELISpot)均为阴性。治疗后7天,血液中未检测到载体DNA。
- 计算机断层扫描(CT)和磁共振成像(MRI)显示,注射后患者耳部结构正常,无异常变化。
2. 有效性结果
- 听觉功能显著恢复
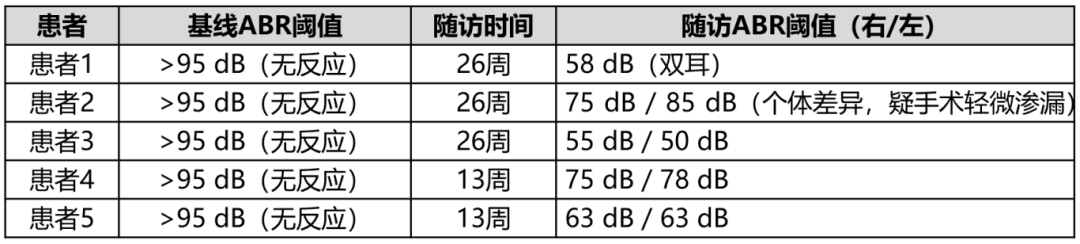
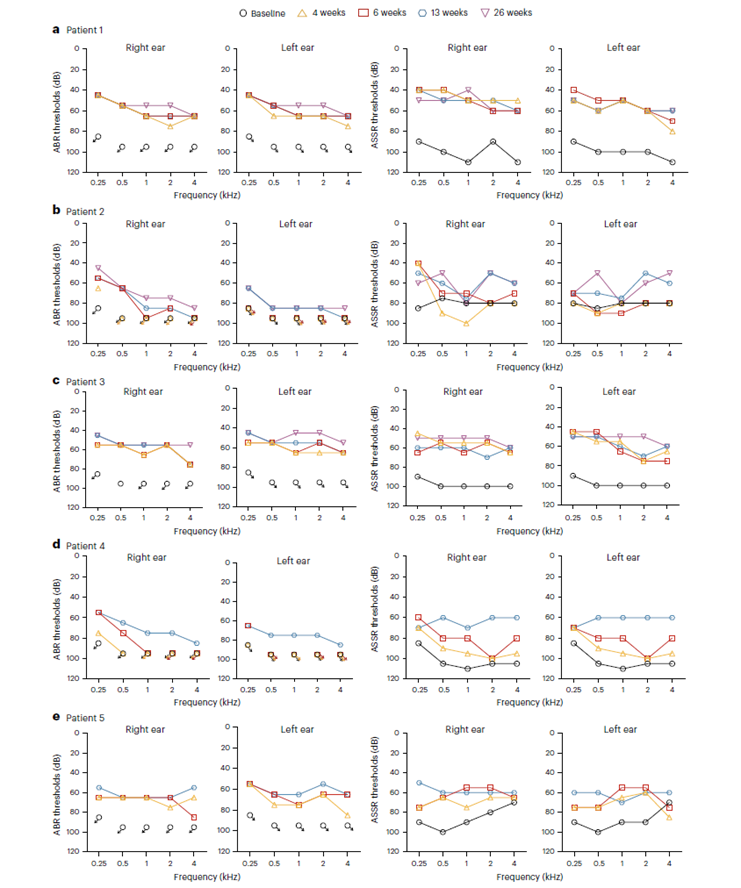
图4. 听力测试a–e,患者1(a)、2(b)、3(c)、4(d)和5(e)的听性脑干反应(ABR)和听性稳态反应(ASSR)阈值。箭头表示即使在最大声强级下也无反应。箭头向左下指为右耳;箭头向右下指为左耳。
- 言语感知和能力提升
所有患者在MAIS/IT-MAIS(有意义听觉整合量表)、CAP(听觉表现类别)等问卷评分上均有显著提高。例如,患者1的MAIS分数从基线1分提升至26周28分(满分40),CAP从0分提升至4分。
- 声源定位能力恢复(双侧治疗的关键优势)
这是单侧治疗无法实现的功能。通过SSQ-P问卷和声源定位测试评估,所有患者均恢复了声源定位能力。
例如,患者1的双侧均方根误差(RMSE)从基线时的92.8°显著改善至26周时的40.0°。当遮住一只耳朵时,误差增大,证明其依赖双耳听觉进行定位。
关键策略与临床转化启示
1)免疫原性的”前瞻性规避”:研究预见到分次注射将导致第二次给药时AAV中和抗体屏障,因此设计为一次性双侧同步注射,将免疫挑战从”时间维度”转化为”空间维度”。这一策略对所有需要多靶点/多器官治疗的基因治疗方案均具有参考价值
2)内耳免疫特权的合理利用:内耳属于免疫特权部位(immune-privileged site),局部注射引发的全身T细胞免疫反应较轻,为AAV内耳治疗的安全窗口提供了生物学基础
3)双侧治疗的额外收益超越预期:声源定位能力的恢复不仅是功能指标,也是人工耳蜗(单侧)无法实现的优势,为双侧基因治疗提供了强有力的临床依据
六、内耳AAV应用快速决策指南

3. 注射手术质量是最大变量来源:内耳注射的实验间重复性高度依赖操作者经验,建议设置阳性对照(已知转导效率的标准血清型+CAG-GFP)和统一的ABR基线筛查流程。
4. 免疫反应需纳入评估体系:局部注射后1–2周应检测外周血抗AAV中和抗体,排除预存免疫对实验结果的干扰。
七、常见问题
Q1:IHC转导不错但OHC几乎无表达,或支持细胞转导差?
A: 可能原因为血清型与目标细胞不匹配,建议区分年龄、物种和靶细胞。如果目标为毛细胞:可优先试用Anc80L65、AAV2.7m8;成年动物可考虑配合PSCC途径。如果目标为支持细胞:优先试用AAV-ie及其优化变体(如ie-K558R)。以“目标细胞—年龄段—物种”为主轴,先做小规模预实验筛型。
Q2: AAV包装效率低,滴度低,表达不稳定。
A:ITR之间的序列不能超过4.7kb,最佳序列长度为3.0-3.5kb [https://doi.org/10.1016/j.omtm.2025.101499]。对于大基因,建议将基因片段拆分,用双/三AAV递送,或采用功能性截短版本。重要元件建议采用经验证的序列,构建后全长测序确认。
Q3: AAV介导的转基因表达在初期达到峰值后逐渐下降。
A: 选择稳定的启动子,如EF1α,或经过优化的细胞特异性启动子,避免使用易被沉默的启动子(如某些病毒启动子在某些细胞中会被甲基化)。优化载体设计,加入增强子元件或绝缘子序列(如cHS4),防止启动子沉默。
Q4: 新生期有效,成年期失效,同血清型不同日龄效果差异大?
A:新生期(P0–P7)RWM对HCs常更有效;成年期OHC可考虑PSCC。需要关注目标疾病的病理进展,尽量“早干预”;若已退化,建议转向再生策略(支持细胞转分化)。设计跨时间点的时序实验,绘制“效率-日龄”曲线。
- https://news.qq.com/rain/a/20250723A05TIS00
- https://www.bksv.com/zh/knowledge/blog/sound/cochlea-function
- Zhao, Y., Zhang, L., Wang, D., Chen, B., & Shu, Y. (2022). Approaches and Vectors for Efficient Cochlear Gene Transfer in Adult Mouse Models. Biomolecules, 13(1), 38.
- Zhang, L., Wang, H., Xun, M., Tang, H., Wang, J., Lv, J., … Shu, Y. (2023). Preclinical evaluation of the efficacy and safety of AAV1-hOTOF in mice and nonhuman primates. Molecular Therapy Methods & Clinical Development, 33(3), 101575.
- Lv, J., Wang, H., Cheng, X., Chen, Y., Wang, D., Zhang, L., … Shu, Y. (2024). AAV1-hOTOF gene therapy for autosomal recessive deafness 9: a single-arm trial. The Lancet, 403(10441).
- Iranfar, S., Cornille, M., Roldan, M. S., Plion, B., Lecomte, M.-J., Safieddine, S., & Lahlou, G. (2025). Cell tropism of adeno-associated viruses within the mouse inner ear in vivo: from embryonic to adult stages. Scientific Reports, 15(1).
- Ballana, E., Wang, J., Venail, F., Estivill, X., Puel, J.-L., Arbonès, M. L., & Bosch, A. (2008). Efficient and specific transduction of cochlear supporting cells by adeno-associated virus serotype 5. Neuroscience Letters, 442(2).
- Emptoz, A., Michel, V., Lelli, A., Akil, O., Boutet de Monvel, J., Lahlou, G., … Safieddine, S. (2017). Local gene therapy durably restores vestibular function in a mouse model of Usher syndrome type 1G. Proceedings of the National Academy of Sciences, 114(36).
- Isgrig, K., Ishibashi, Y., Lee, H. J., Zhu, J., Grati, M., Bennett, J., … Chien, W. W. (2022). AAV8BP2 and AAV8 transduce the mammalian cochlear lateral wall and endolymphatic sac with high efficiency. Molecular Therapy – Methods & Clinical Development, 26.
- Han, S., Xu, Z., Wang, S., Tang, H., Hu, S., Wang, H., … Shu, Y. (2024). Distributional comparison of different AAV vectors after unilateral cochlear administration. Gene Therapy, 31(3–4).
- Han, S., Xu, Z., Wang, S., Tang, H., Hu, S., Wang, H., … Shu, Y. (2024). Distributional comparison of different AAV vectors after unilateral cochlear administration. Gene Therapy, 31(3–4).
- Isgrig, K., McDougald, D. S., Zhu, J., Wang, H. J., Bennett, J., & Chien, W. W. (2019). AAV2.7m8 is a powerful viral vector for inner ear gene therapy. Nature Communications, 10(1).
- György, B., Meijer, E. J., Ivanchenko, M. V., Tenneson, K., Emond, F., Hanlon, K. S., … Corey, D. P. (2019). Gene Transfer with AAV9-PHP.B Rescues Hearing in a Mouse Model of Usher Syndrome 3A and Transduces Hair Cells in a Non-human Primate. Molecular Therapy – Methods & Clinical Development, 13.
- György, B., Meijer, E. J., Ivanchenko, M. V., Tenneson, K., Emond, F., Hanlon, K. S., … Corey, D. P. (2019). Gene Transfer with AAV9-PHP.B Rescues Hearing in a Mouse Model of Usher Syndrome 3A and Transduces Hair Cells in a Non-human Primate. Molecular Therapy – Methods & Clinical Development, 13.
- Tao, Y., Liu, X., Yang, L., Chu, C., Tan, F., Yu, Z., … Wu, H. (2022). AAV-ie-K558R mediated cochlear gene therapy and hair cell regeneration. Signal Transduction and Targeted Therapy, 7(1).
- Ivanchenko, M. V., Hanlon, K. S., Hathaway, D. M., Klein, A. J., Peters, C. W., Li, Y., … Corey, D. P. (2021). AAV-S: A versatile capsid variant for transduction of mouse and primate inner ear. Molecular Therapy – Methods & Clinical Development, 21.
- Kim, M.-A., Ryu, N., Kim, H.-M., Kim, Y.-R., Lee, B., Kwon, T.-J., … Kim, U.-K. (2019). Targeted Gene Delivery into the Mammalian Inner Ear Using Synthetic Serotypes of Adeno-Associated Virus Vectors. Molecular Therapy – Methods & Clinical Development, 13.
- Aaron, K. A., Pekrun, K., Atkinson, P. J., Billings, S. E., Abitbol, J. M., Lee, I. A., … Cheng, A. G. (2023). Selection of viral capsids and promoters affects the efficacy of rescue of Tmprss3-deficient cochlea. Molecular Therapy – Methods & Clinical Development, 30.
- Shubina-Oleinik, O., Nist-Lund, C., French, C., Rockowitz, S., Shearer, A. E., & Holt, J. R. (2021). Dual-vector gene therapy restores cochlear amplification and auditory sensitivity in a mouse model of DFNB16 hearing loss. Science Advances, 7(51).
- Akil, O., Dyka, F., Calvet, C., Emptoz, A., Lahlou, G., Nouaille, S., … Lustig, L. R. (2019). Dual AAV-mediated gene therapy restores hearing in a DFNB9 mouse model. Proceedings of the National Academy of Sciences, 116(10).
- Al‐Moyed, H., Cepeda, A. P., Jung, S., Moser, T., Kügler, S., & Reisinger, E. (2019). A dual‐AAV approach restores fast exocytosis and partially rescues auditory function in deaf otoferlin knock‐out mice. EMBO Molecular Medicine, 11(1).
- US 2021/0388045A1
- Hu, S. W., Lv, J., Wang, Z., Tang, H., Wang, H., Wang, F., … Li, H. (2024). Engineering of the AAV-Compatible Hair Cell-Specific Small-Size Myo15 Promoter for Gene Therapy in the Inner Ear. Research, 7.
- Rio, C., Dikkes, P., Liberman, M. C., & Corfas, G. (2002). Glial fibrillary acidic protein expression and promoter activity in the inner ear of developing and adult mice. Journal of Comparative Neurology, 442(2).
- Keppeler, D., Merino, R. M., Lopez de la Morena, D., Bali, B., Huet, A. T., Gehrt, A., … Moser, T. (2018). Ultrafast optogenetic stimulation of the auditory pathway by targeting‐optimized Chronos. The EMBO Journal, 37(24).
- Gene Therapy vs Cochlear Implantation in Restoring Hearing Function and Speech Perception for Individuals With Congenital Deafness. JAMA Neurol. Published online July 21, 2025. doi:10.1001/jamaneurol.2025.2053
- Hu, S. W., Jeong, S., Jiang, L., Koo, H., Wang, Z., Choi, W. H., … Shu, Y. (2025). PAM-flexible adenine base editing rescues hearing loss in a humanized MPZL2 mouse model harboring an East Asian founder mutation. Nature Communications, 16(1).
- Zhao, S., Yang, Q., Yu, Z., Chu, C., Dai, S., Li, H., … Zhong, G. (2025). Deciphering enhancers of hearing loss genes for efficient and targeted gene therapy of hereditary deafness. Neuron, 113(10). https://doi.org/10.1016/j.neuron.2025.03.02
- Wang, H., Chen, Y., Lv, J., Cheng, X., Cao, Q., Wang, D., … Shu, Y. (2024). Bilateral gene therapy in children with autosomal recessive deafness 9: single-arm trial results. Nature Medicine, 30(7).
- Akil O, et al.( 2015). Surgical Method for Virally Mediated Gene Delivery to the Mouse Inner Ear through the Round Window Membrane. J Vis Exp. 16;(97):52187. doi: 10.3791/52187.
- Isgrig K & Chien WW. (2018). Posterior Semicircular Canal Approach for Inner Ear Gene Delivery in Neonatal Mouse. J Vis Exp. 2;(133):56648. doi: 10.3791/56648.
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。