腺相关病毒(AAV)是目前基因治疗领域应用最广泛的病毒载体之一。凭借其低免疫原性、高转导效率以及在多种组织中实现长期稳定表达的能力,AAV已在基础研究和临床转化中取得了令人瞩目的进展——从早期获批的 AAV 基因治疗药物Glybera,到 Luxturna、Zolgensma 等里程碑式产品,AAV 的临床价值正在被不断验证。
然而,AAV 有一个几乎无法回避的物理限制——约 4.7 kb 的基因组包装容量。这一上限需要容纳目的基因编码序列(CDS)、启动子、增强子、poly(A) 信号序列以及病毒包装必需的反向末端重复序列(ITR,约 145 bp × 2)。当目的基因的 CDS 本身接近甚至大幅超过 4 kb 时,单个 AAV 载体便力不从心。
这并非小概率问题——许多重要遗传疾病的致病基因恰恰”超标”。以杜氏肌营养不良(DMD)为例,其 DMD 基因全长 cDNA 约 11 kb;DFNB9 型耳聋的致病基因 OTOF 约 6 kb;Stargardt 病的 ABCA4 基因约 6.8 kb。容量瓶颈,直接将这些疾病挡在了 AAV 基因治疗的”门外”。
面对这一挑战,研究者们开发出了一系列将大基因”化整为零、再聚为一”的双载体(或多载体)递送策略。本文将为您系统梳理这些策略的设计原理,各自的优缺点,并结合经典的应用案例,为您提供一份详尽的AAV大基因递送实战参考指南。
一、破“限”之道:大基因拆分与重组的核心技术策略
面对“超载”的基因货物,科学家们开发了多种巧妙的“拆分-重组”策略,其核心思想是将一个大基因拆分成两个或多个片段,分别包装进不同的AAV病毒中,在共感染目标细胞后,通过DNA重组、mRNA反式剪接或蛋白质内含肽剪接三种不同层面的分子机制,将这些基因片段重新拼接成一个完整的、具有功能的表达单元。
这是最早被开发也是最经典的双载体策略之一。
设计原理:将大基因从中间拆分为两部分,上游载体包含启动子和基因 5′ 片段,下游载体包含基因 3′ 片段和 poly(A)信号,分别构建到两个AAV载体上。关键在于,这两个载体的拆分区存在一段几百bp的同源重叠序列(overlapping sequence)。
重组机制:当这两个AAV载体共感染同一个细胞并进入细胞核后,细胞会利用自身的同源重组修复机制,以重叠序列为模板,将两条AAV基因组拼接成一个完整的、可转录的DNA分子(图1)。
优点:
- 概念简单,易于设计,无需引入额外的外源功能元件。
- 重组后的产物是完整的DNA,可以实现长期稳定的表达。
挑战:
- 重组效率偏低:依赖于细胞内源的同源重组,其效率在不同组织和细胞类型中差异很大,且通常不高。
- 副产物问题:可能产生非同源末端连接(NHEJ)介导的副产物或单体截短蛋白,可能引发细胞毒性或免疫反应。
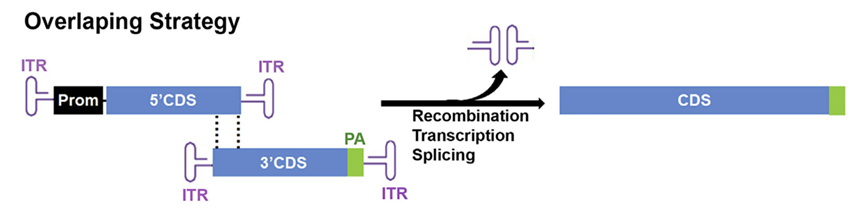
图1 重叠法(Overlapping)双AAV载体递送策略[1]
2. 经典 dual-AAV trans-splicing:先重建载体,再重建转录本[1,3]
为了克服同源重组效率低下的问题,研究者们将目光投向了更为高效的mRNA剪接过程。
设计原理:将过大的基因表达盒拆分为两个独立的AAV载体。
- 5’端载体(上游载体):携带启动子(Promoter)、5’端编码序列(5′ CDS)以及位于3’端的剪接供体位点(Splice Donor, SD)。
- 3’端载体(下游载体):携带剪接受体位点(Splice Acceptor, SA)、3’端编码序列(3′ CDS)以及多聚腺苷酸信号(PolyA)。
两个载体通过ITR(反向末端重复序列)介导的分子间重组进行头尾相连(head-to-tail concatemerization),形成完整的转录单元(图2)。
重组机制:两个AAV基因组的ITR序列通过分子间重组实现头尾相连,连接后,SD和SA信号识别并剪切除去中间的重组ITR序列,剪接后产生包含完整编码序列的单一mRNA分子,随后翻译成全长蛋白(图2)。
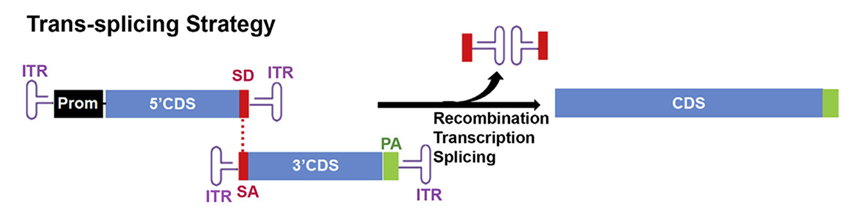
图2 反式剪接(Trans-splicing)双AAV载体递送策略[1]
优点:
- 明确的分子机制:相比重叠法的策略,dual-AAV trans-splicing具有更明确的分子机制,通过工程化的剪接信号精确控制重组过程。
- 广泛适用性:不依赖于基因内部的同源序列,可适用于各种大型基因。
- 背景表达低:单个载体表达的将是无功能的截短蛋白,降低了背景信号和潜在毒性。
挑战:
- 方向性依赖:需要两个载体以特定的头尾方向连接,随机连接效率低。
- 剪接效率问题:需要精确的剪接信号匹配,剪接效率可能影响最终蛋白产量。
- 共转导要求:需要目标细胞同时被两个载体感染,对共转导效率要求高。
- 组织/细胞类型差异:不同组织的DNA修复和剪接机制差异可能影响效率。
3. REVeRT:真正意义上的 mRNA反式剪接(trans-splicing)[4-5]
REVeRT (Reconstitution via mRNA Trans-splicing):通过 mRNA反式剪接在转录本层面重建完整大基因或大型编辑工具。该体系已被用于重建报告基因、CRISPRa、prime editor 以及大基因 ABCA4,并在细胞、类器官和小鼠体内得到验证 (图3) 。
设计原理:将过大的基因表达盒拆分为两个独立AAV载体,但与传统依赖DNA层面连接的双AAV不同,REVeRT的核心在于RNA层面的重建。
- 5’端载体(上游载体):携带启动子、5’端编码序列、剪接供体位点(SDS)、互补结合域(binding domain)以及polyA等元件。
- 3’端载体(下游载体):携带启动子、互补结合域、剪接受体位点(SAS)、3’端编码序列以及polyA信号。
两个载体进入同一细胞后,分别转录形成两段RNA,这两段RNA借助互补结合域靠近,再在SDS和SAS的介导下发生真正的mRNA反式剪接,生成完整成熟mRNA,最终翻译出全长蛋白。
重组机制:
REVeRT的重组过程主要发生在两条独立mRNA之间,而不是先在AAV基因组的DNA层面完成重组。具体来说,两个AAV分别转录产生5’片段RNA和3’片段RNA,这两条RNA在互补结合域的作用下相互配对并靠近,随后由细胞剪接机制识别剪接供体位点(SDS)和剪接受体位点(SAS),切除中间非编码序列并完成反式剪接,最终形成包含完整编码序列的成熟mRNA,再进一步翻译生成全长蛋白。
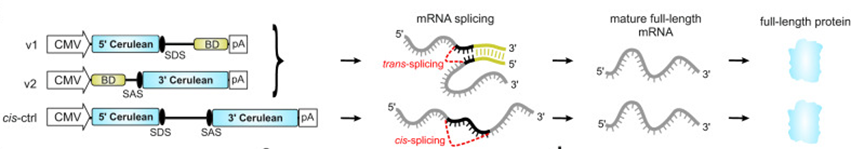
图3 REVeRT法双AAV载体递送策略[4]
优点:
- 不依赖DNA同源重组,机制更直接:REVeRT主要依赖mRNA反式剪接完成重建,而不是依赖效率有限的DNA层面重组,因此在原理上绕开了传统DNA trans-splicing效率不稳定的问题。
- 应用范围广:该体系不仅能重建报告蛋白,还能用于 CRISPRa、prime editing、体内多重编辑(同时激活和敲除)以及大基因补充治疗。
- 体内外均具有可观重建效率。
挑战:
- 仍然依赖双载体共转导:REVeRT必须要求同一目标细胞同时获得两个AAV载体,之后两条RNA才能发生trans-splicing。因此在体内尤其是系统给药条件下,共转导效率仍然是限制因素。
- 重建效率仍未达到单载体全长表达水平:虽然REVeRT能实现功能性恢复,但其效率通常仍低于全长单载体对照,例如luciferase在体内和类器官中的恢复都只是部分比例,提示该系统仍需进一步优化。
- 系统对剪接元件设计较敏感:SAS对效率影响尤其显著,不同SAS之间差异很大;互补结合域、是否保留polyA、split site选择等也都会影响结果。这说明REVeRT虽然灵活,但并不是完全“即插即用”,仍需针对不同目标进行工程优化。
4. Hybrid AK:把“重组”和“剪接”组合起来[1]
将”大基因递送”从传统依赖ITR随机串联的低效重组,升级为依赖外源性高重组原性序列(AK)介导的高效同源重组的”定向拼接”。
设计原理:
Hybrid AK的核心设计是把完整表达盒拆成两个携带互补AK重组臂的AAV载体(图4):
- AAV-5’载体:携带启动子与目标基因(GOI)5’端片段,并在末端依次连接剪接供体位点(SD)与AK重组序列(F1噬菌体来源,77bp), flank以ITR,形成”重组臂+剪接信号”的双重功能模块。
- AAV-3’载体:携带AK重组序列(与5’载体互补)、剪接受体位点(SA)、GOI 3’端片段和poly(A)信号,AK-SA-GOI-3’序列位于ITR之间,确保重组后形成完整转录单元。
- 关键设计:AK序列作为外源性重组原性区域,不依赖GOI内部序列同源性,使拆分位点选择更灵活;SD/SA信号嵌套于AK序列两侧,确保DNA重组后通过顺式剪接精确去除重叠区。
重组机制
该双AAV载体系统通过共感染实现目标基因(GOI)的高效重建(图4):
- AK序列启动重组:共感染后,两个载体通过AK序列介导的分子间同源重组,将5’载体的”Promoter-GOI-5′-SD-AK”与3’载体的”AK-SA-GOI-3′-poly(A)”精确拼接,形成单一连续DNA分子。
- mRNA成熟与翻译:重组后的DNA转录为pre-mRNA,包含SD-AK-SA内含子结构,经顺式剪接去除AK序列及连接区,生成可翻译的成熟GOI转录本。
- 方向性控制:AK重组序列显著提高头尾串联(head-to-tail)正确方向的比例,减少错误串联导致的表达失败。
优点
- 重组效率更高、方向性更强:AK序列的高重组原性显著优于单纯ITR介导的随机串联。
- 适用范围更广:不依赖GOI内部同源序列,可通用化设计。
挑战
- 共感染门槛仍在:双载体系统本质上依赖同一细胞同时获得两个AAV;组织/血清型/剂量分布不均会限制总体有效细胞比例。
- 组织特异性差异:不同细胞的DNA修复通路活性影响重组效率。
- 血清型组合优化:AAV血清型与靶组织的匹配对共转导效率影响显著。
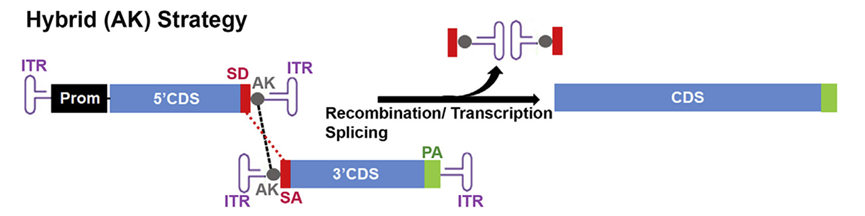
图4 AK法双AAV载体递送策略[1]
5. Split intein:在蛋白层面完成“无缝拼接”[6]
如果说前两种策略依赖的是细胞自身的“剪刀加浆糊”,那么内含肽策略则是为蛋白片段引入了能“自我重组”的智能模块。
设计原理:内含肽(Intein)是一类特殊的蛋白质序列,能够从一个前体蛋白中自我“剪切”出去,并同时将两侧的“外源蛋白”(Extein)通过标准的肽键连接起来。分裂内含肽(Split-Intein)则是将一个内含肽拆分成N端(IntN)和C端(IntC)两部分。我们将大蛋白拆分成两半,分别与IntN和IntC融合,并由两个AAV载体递送(图5)。
重组机制:当两个融合蛋白在细胞内相遇时,IntN和IntC会自动识别、折叠并缔合,恢复内含肽的完整功能,然后催化自身切除,并将两侧的目标蛋白片段无痕地连接在一起,形成全长功能蛋白。
优点:
- 反应快速、效率高:蛋白质剪接过程非常迅速,例如常用的Npu DnaE和 Rma DnaB 内含肽,其反应半衰期可达秒级。
- 绕开转录和剪接:直接在蛋白质层面操作,不受转录效率、mRNA稳定性等因素影响。
- “无痕”连接:理想情况下,连接处不引入任何额外的氨基酸。
挑战:
- 剪接效率:部分内含肽系统存在不完全剪接的问题,可能与蛋白折叠、聚集有关。
- 拆分位点选择:拆分位点的选择对目标蛋白的折叠和功能至关重要,需要仔细评估。
- 免疫原性:内含肽作为外源蛋白,存在引发免疫反应的潜在风险。

图5 内含肽双AAV载体递送策略[6]
6. AAVLINK技术: 新近出现的位点特异性重组路线[7]
将“大基因递送”从传统依赖同源重叠的 DNA自发拼接,升级为依赖 Cre/lox 位点特异性重组的“强制拼接”。
设计原理:
AAVLINK 的核心设计是把完整表达盒拆成两个彼此“单独不完整、合在一起才完整”的 AAV(图6):
- AAV-5’载体:携带启动子与目标基因(GOI)5’端片段,并在末端加入剪接供体位点(SD)与一个 lox 位点,同时刻意不提供有效 poly(A),使其单独进入细胞时难以形成稳定表达。
- AAV-3’载体:放入启动子驱动的 Cre 重组酶表达框,并在一个人工内含子里嵌入另一个 lox 位点,在其后依次连接剪接受体位点(SA)、GOI 3’端片段和 poly(A),其中一个关键技巧是把 GOI 的 3’片段“隐藏”在 Cre 的 3’UTR/内含子结构之后,让重组前更像非完整表达盒。
- AAVLINK系统还可扩展至三载体配置,进一步突破载体容量限制。通过合理设计多个lox位点和剪接位点的组合(图7),三载体AAVLINK系统能够递送高达11kb的遗传物质,这几乎涵盖了大多数与人类遗传疾病相关的大基因。在三载体系统中,基因被分割成三个片段分别装载,通过Cre介导重组和剪接过程,最终重建完整的功能基因表达单元。
- 为进一步降低重组的可逆性,系统通常采用左右臂突变的非对称 lox(LE/RE)配对,使重组后生成难以再次被 Cre 识别的双突变位点,从而让拼接更趋于不可逆。
重组机制:
该双AAV载体系统(或三载体系统)通过共感染实现目标基因(GOI)的条件性表达(图6-7):
Cre酶启动重组:共感染后,3’载体首先表达Cre重组酶。
分子间基因重建:Cre酶识别并介导载体间loxP位点的分子间重组,将各载体携带的基因片段精确拼接,形成一个完整的转录单元。
mRNA成熟与翻译:重组后的DNA转录为前体mRNA,随后通过SD/SA介导的剪接反应去除人工内含子,生成可翻译的成熟GOI转录本。
自我失活的安全开关:重组过程会使Cre编码序列与其表达所必需的SA/poly(A)元件分离,导致Cre在完成重组任务后表达迅速终止。这种瞬时表达策略,显著降低了长期表达可能带来的脱靶或免疫风险。
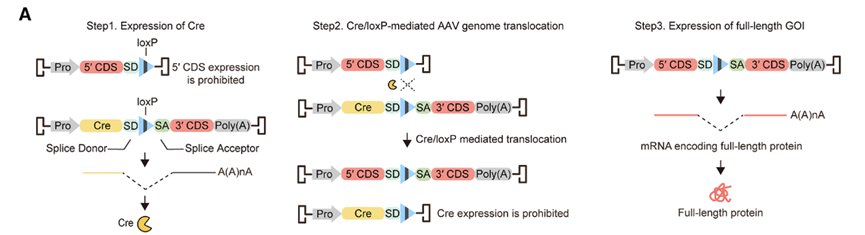
图6 AAVLINK系统示意图。对于双AAV载体方案,其中一条载体携带GOI的5′端部分,并在其末端加入SD(剪接供体)等元件,但缺乏poly(A)信号;另一条载体包含Cre重组酶表达框及相关UTR,并将GOI的3′端片段(连同SA,剪接受体)布置在Cre转录单元的下游/非完整表达盒结构中。重组发生前,只有Cre因具备完整表达盒而更易被表达[7]。
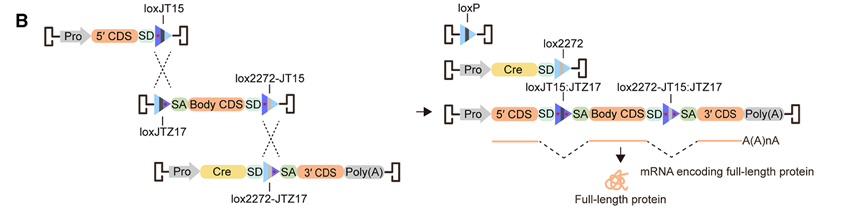
图7 AAVLINK介导的三载体递送示意图。在三载体(tripartite)方案中,需要使用两对lox位点来组装被分段拆分的GOI。第一对lox位点(loxJT15 与 loxJTZ17)介导GOI 5′端片段与GOI主体(body)片段之间的重组;随后,GOI的3′端片段通过另一对间隔/突变型lox位点(lox2272-JT15 与 lox2272-JTZ17)发生重组,从而被转位并连接到GOI主体片段的下游[7]。
优点:
- 重组效率更高、可控性更强:由Cre/lox驱动的位点特异性重组通常比细胞内源同源重组更稳定、更高效。
- 副产物更少:通过“5’端无poly(A)+带SD抑制成熟”“3’端把GOI-3’放在Cre之后且需经重组+剪接才变成表达盒”,能显著降低传统双AAV常见的截短蛋白/错误拼接产物。
- 拆分位点更灵活:不再强依赖几百bp同源重叠序列,拆分策略可围绕剪接与载体容量做更灵活优化。
- 载体容量突破:三载体系统可递送高达11kb的遗传物质,覆盖绝大多数大基因治疗需求。
- 表达更干净、Cre更短暂:重组后GOI是“完整DNA表达盒”,可获得较长期表达;同时Cre在完成重组后被“自我关停/显著衰减”,有利于安全性。
挑战:
- 共感染门槛仍在:多载体系统本质上依赖同一细胞同时获得所有AAV载体,组织/剂量/血清型分布不均会限制总体有效细胞比例。
- Cre相关安全性与免疫风险:Cre属于外源蛋白,存在潜在毒性或免疫原性;也可能在极端情况下带来非预期重组风险,因此文章中进一步提出了 AAVLINK2.0(如用降解标签使Cre更易降解)来缓解生物安全顾虑。
- 工艺与质控复杂度增加:需要多种载体分别生产、定量、配比与一致性控制;临床级放大时对批间差异更敏感。
7. 其他创新策略
三 AAV 载体系统(Triple AAV) 是一种面向超大基因的容量扩展策略:如果把单个 AAV 理解成一个“快递盒”,那它最大的难题就是空间太小:很多真正关键的疾病基因,根本装不进去。像 DMD 这样的超大基因,全长编码序列超过 11 kb,单 AAV 不够,双 AAV 也往往很吃力,这时候就需要 Triple AAV 出场了。它的核心思路并不是简单“多加一个载体”,而是把同一套表达信息拆成 3 段,分别装进 3 个 AAV,再让它们在同一个目标细胞里重新拼回完整产物。这个“拼回去”的过程,既可以发生在 DNA/RNA 层面,也可以发生在蛋白层面,所以三 AAV 更准确地说是一种容量扩展框架,而不是某一种固定技术。它真正厉害的地方在于,把过去几乎不可能的“全长大基因递送”拉回到了可验证、可优化的现实范围;当然,代价也很明确:3 个载体必须同时进入同一个细胞,后续组装还要足够高效、足够准确,整体工艺难度也会明显上升。
典型设计是利用两对正交的分裂内含肽,将目的蛋白拆分为三段,由三个 AAV 分别递送:
(1)中间片段两端各融合一对内含肽(IntC₁ + IntN₂);(2)N 端片段融合 IntN₁;(3)C 端片段融合 IntC₂。三个片段在细胞内共表达后,依次发生两步蛋白反式剪接,最终组装出全长蛋白(图8)[9]。
这一策略已在mdx小鼠模型中得到验证[6],成功表达了全长427 kDa抗肌萎缩蛋白(dystrophin),并显示出优于micro-dystrophin的功能恢复效果。该研究为超大基因的体内递送提供了可行方案,但其在大型动物模型(如猪、狗、羊等)中的验证仍需进一步研究。
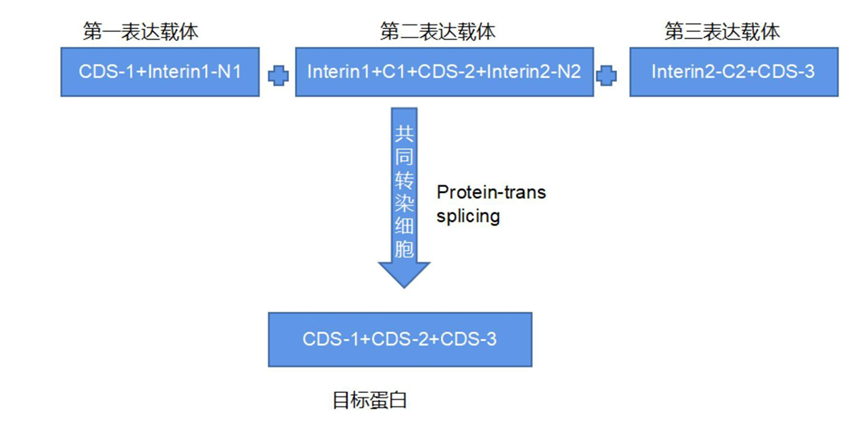
图8 两组正交的内含肽三AAV载体递送策略[9]
策略对比总览
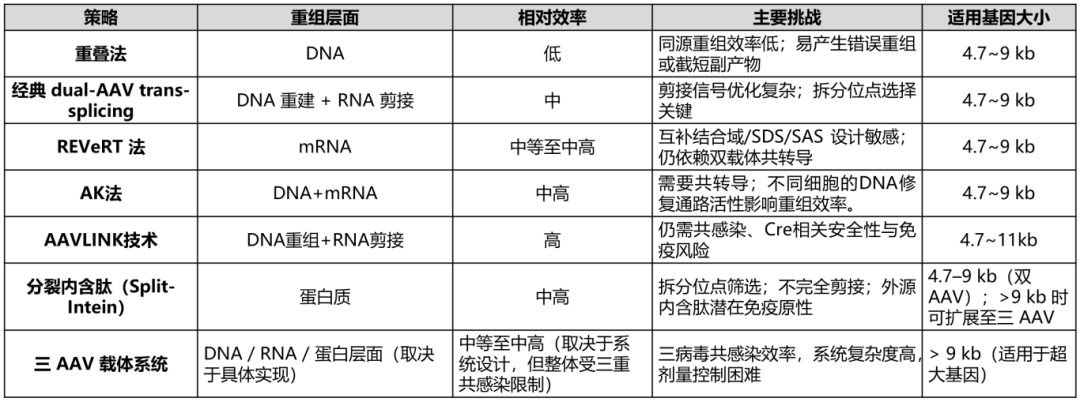
二、经典应用案例分析
案例1:Stargardt遗传性黄斑变性的基因治疗(重叠法)[2]
背景:Stargardt病是最常见的遗传性黄斑变性,由ABCA4基因突变导致。ABCA4基因长达6.8kb,远超AAV病毒载体4.7kb的包装容量,传统方法无法递送完整基因。
策略:McClements 等人采用重叠法双AAV载体策略,将ABCA4基因拆成两段(图9),分别装入两个AAV载体,两段设计207-505bp的DNA重叠区。当两个载体同时进入光感受器细胞核后,通过同源重组自动拼接成完整基因,像”分子拼图”一样恢复全长蛋白表达。
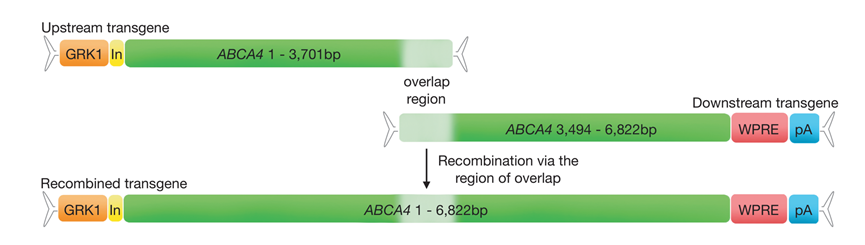
图9 ABCA4重叠双载体系统示意图。腺相关病毒(AAV)转基因元件被拆分为两个独立的转基因(上游和下游)。上游转基因包含启动子及ABCA4编码序列的上游片段,下游转基因携带ABCA4编码序列的下游片段以及WPRE和pA元件。当两个转基因进入同一宿主细胞核后,通过重叠区域进行对齐并重组。
实验操作:
在Abca4基因敲除小鼠视网膜下腔注射双AAV混合物,系统测试6种重叠长度(23-1,173bp)。最优组合为含内含子的207bp重叠载体(InC),剂量1×10¹⁰GC/眼。
实验结果:
Western blot证实全长ABCA4蛋白在光感受器外节正确表达,视网膜毒素水平显著降低(p=0.03)。6个月后,治疗眼眼底自发荧光减弱,脂褐素沉积受控,截短蛋白副产物较少,未见明显安全性信号(图10)。
和Hcn1(红色)染色.png)
图10 小鼠眼球切片的ABCA4(绿色)和Hcn1(红色)染色。细胞核用Hoescht染色。(A) 野生型SVEV 129小鼠光感受器外节的Abca4染色。(B) 未注射的Abca4⁻/⁻小鼠中Abca4染色缺失。(C) 注射上游载体的Abca4⁻/⁻小鼠中ABCA4缺失。(D) 注射下游载体的Abca4⁻/⁻小鼠中ABCA4染色缺失。(E) 注射双载体的Abca4⁻/⁻小鼠光感受器外节的ABCA4染色。
案例2:DFNB9 型先天性耳聋的基因治疗(内含肽策略,从实验室到临床)[8]
背景:OTOF基因突变导致DFNB9型听神经病(占先天性遗传性耳聋2-8%),编码的otoferlin蛋白在内毛细胞中调控突触囊泡释放。由于OTOF基因过大(约6kb),超过单个AAV载体包装容量。
策略:Tang 等人采用双AAV载体介导的蛋白反式剪接策略(图11),在S818和S1114位点拆分小鼠otoferlin蛋白,通过蛋白质结构预测筛选出最优拆分位点(S1114),将N端片段与分裂内含肽N段(IntN)、C端片段与分裂内含肽C段(IntC)分别融合,包装至AAV-PHP.eB血清型,经圆窗膜(RWM)注射导入新生Otof⁻/⁻小鼠耳蜗,利用分裂内含肽自催化拼接恢复完整otoferlin蛋白功能,实现听力长期稳定恢复。
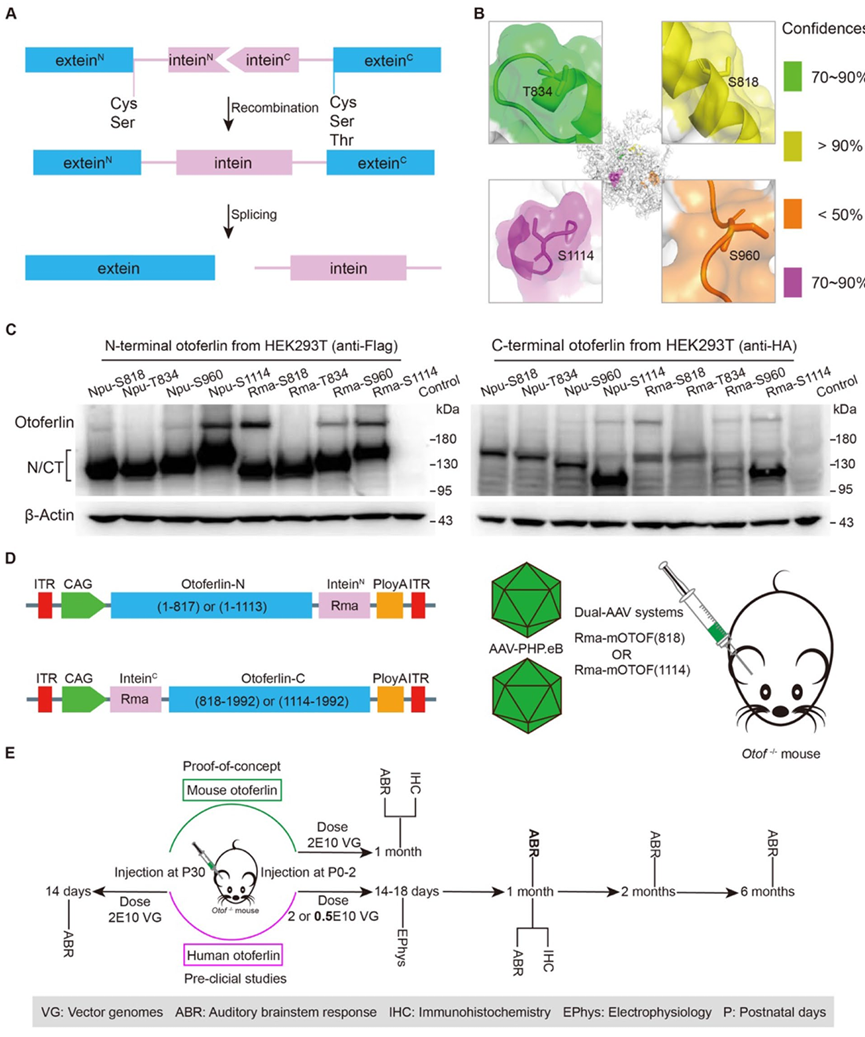
图11 双AAV病毒载体的构建。将小鼠耳畸蛋白(otoferlin)在S818或S1114残基位点处分割,随后将otoferlin的N端和C端片段分别与分割型Rma内含肽(split Rma intein)一起包装进AAV-PHP.eB载体,并通过圆窗膜(RWM)给药方式注射到小鼠耳蜗内。所使用的小鼠模型为Otof基因缺陷型小鼠。
实验操作:
构建双AAV系统:将小鼠/人源OTOF cDNA在筛选位点分割,分别构建至AAV-载体(CAG/CMV启动子)并包装PHP.eB血清型病毒,滴度1×10¹³ vg/mL。
单侧注射:向新生Otof⁻/⁻小鼠右耳蜗注入2μl混合病毒(N:C=1:1),成年鼠经后半规管注射。
功能评估:注射后1/2/6个月测ABR阈值,免疫荧光检测蛋白共表达率,膜片钳记录囊泡释放和Ca²⁺电流。
实验结果:
听力恢复:注射耳click-ABR阈值恢复至野生型水平(43dB),持续6个月以上;对侧耳改善至52-56dB,证实单侧注射实现双侧疗效。
转导效率:注射耳约70%内毛细胞共表达蛋白片段,对侧耳约35%,与听力改善程度正相关。
功能修复:快速囊泡释放(ΔCm 7.15fF)和囊泡补充速率(287个/秒/活性区)均恢复至野生型水平,Ca²⁺电流正常。
临床转化:人源OTOF系统在小鼠模型中同样有效,无耳毒性,为DFNB9耳聋治疗提供了高效、安全的策略。
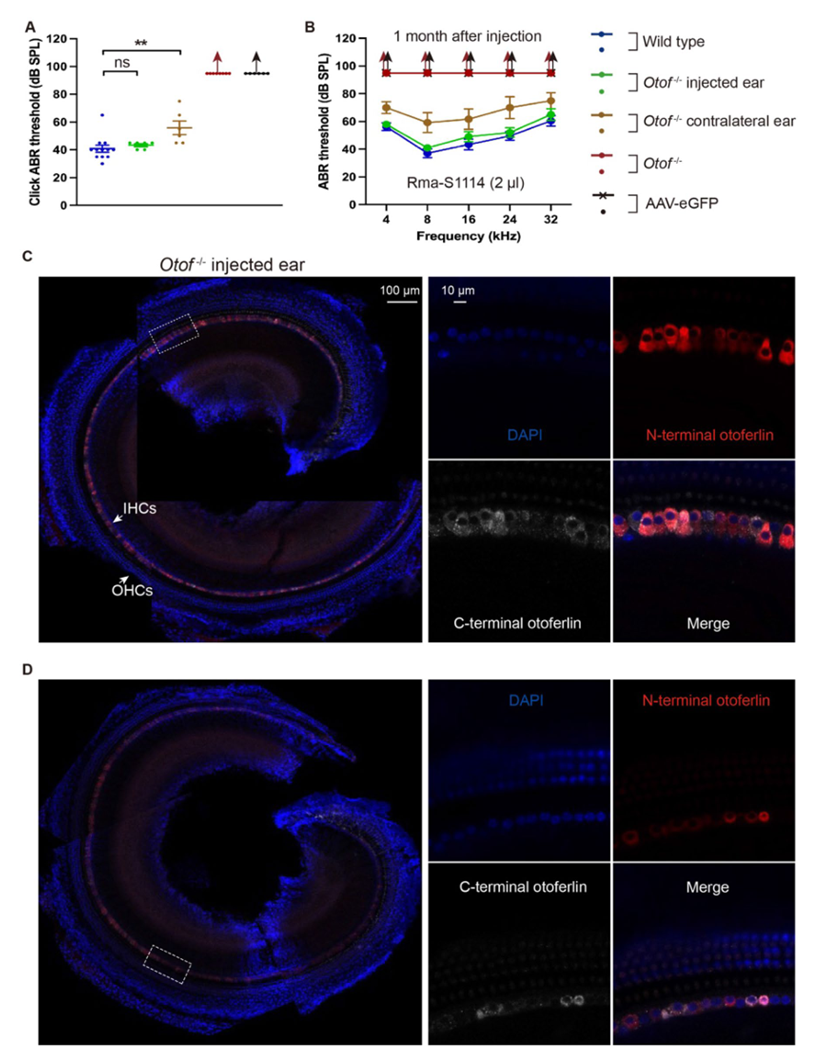
图12 使用内含肽介导的小鼠耳畸蛋白(otoferlin)在P0–P2天注射治疗Otof–/–小鼠的双侧耳聋。A 将Rma-S1114包装进双AAV-PHP.eB后注射到Otof–/–小鼠,记录其click-ABR阈值(野生型组,n = 12;注射耳组,n = 6;对侧耳组,n = 6;Otof–/–组,n = 10;AAV-eGFP组,n = 6)。B 将Rma-S1114包装进双AAV-PHP.eB后注射到Otof–/–小鼠,记录其短纯音ABR阈值(野生型组,n = 12;注射耳组,n = 6;对侧耳组,n = 6;Otof–/–组,n = 10;AAV-eGFP组,n = 6)。C、D 将Rma-S1114包装进双AAV-PHP.eB注射后,分析Otof–/–小鼠(P30)注射耳和对侧耳的免疫荧光结果。蓝色、红色和白色分别表示细胞核、N端otoferlin和C端otoferlin。DAPI是核染色染料,N端和C端耳畸蛋白分别用抗N端和C端耳畸蛋白抗体(ab53233,Abcam;PA552935,Invitrogen)进行免疫染色。AAV-eGFP组指仅注射携带eGFP的AAV载体的Otof−/−小鼠,n = 6。比例尺:100 μm(C、D,左侧),10 μm(C、D,右侧)。数据以均值±标准误表示。ns,无显著性差异;**P < 0.01
案例 3:杜氏肌营养不良症(DMD)的基因治疗(三 AAV 内含肽策略)[6]
背景:杜氏肌营养不良症(DMD) 是由 Dystrophin基因突变引起的遗传性肌肉疾病,该基因编码的抗肌萎缩蛋白(dystrophin)全长 cDNA 约 11.2 kb,是 AAV 大基因递送领域最具挑战性的靶标之一。现有的”微缩化 Dystrophin(micro-Dys / mini-Dys)”策略通过删减非关键结构域将 CDS 压缩至 3.6~5 kb,但删减带来的功能代偿性损失始终是一个争议。
策略:Tasfaout 等人开发了两对正交分裂内含肽介导的三 AAV 系统。将Dystrophin基因拆分成2-3段,分别装入不同AAV载体中,利用两对正交内含肽依次连接。当多个载体同时转导肌肉细胞后,内含肽通过自催化反应将蛋白片段无缝连接成完整的功能性dystrophin蛋白,如”分子缝合”般恢复全长蛋白表达。首次实现了接近全长 Dystrophin(14 个 Rod 结构域,约 8.9 kb CDS)的体内递送(图13)。
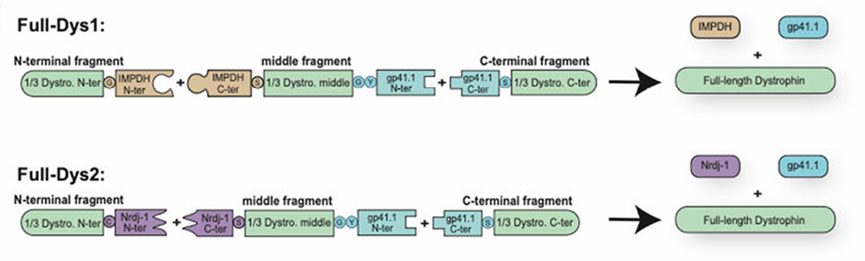
图13 三载体分裂内含肽介导的蛋白反式剪接策略示意图。
实验操作:
- 构建双/三AAV系统:将人源Dystrophin cDNA在优化位点分割,分别构建两种分裂式载体系统:(1) 编码截短型Dystrophin(midi-Dys,ΔSR5-15),由2个AAV载体携带;(2) 编码全长Dystrophin(full-Dys),由3个AAV载体携带。均采用肌肉特异性CK8e启动子。
- 包装肌肉趋向性 AAVMYO 血清型用于系统递送;尾静脉给药设置低和高剂量:2×10¹³ vg/kg 与 2×10¹⁴ vg/kg。
- 在 mdx⁴ᶜᵛ 小鼠中进行给药评估:3 周龄 TA 肌肉注射 5×10¹⁰ vg(用于局部验证,AAV6);8 周龄与 17 月龄进行尾静脉注射(低剂量2×10¹³ vg/kg,高剂量2×10¹⁴ vg/kg,AAV9或AAVMYO)。
- 随访并检测疗效:肌注后约 5 周、静脉给药后约 12 周(≈3 个月)及 6–7 个月,评估 Dystrophin 表达、肌肉组织学改善及肌肉/心脏生理功能恢复。
实验结果:
- AAV6 系统给药可行性验证(8 周龄 mdx⁴ᶜᵛ,治疗 3 个月):Western blot 定量显示,双 AAV 递送 midi-Dys 表达约达 WT 的 75%;三 AAV 递送 full-Dys 约达 WT 的 31%;对照 μDys5 仅约 8%(图14)。
- AAVMYO 系统递送转导优势(老年组对比 AAV9):在 17 月龄 mdx⁴ᶜᵛ 治疗 7 个月的实验中,AAVMYO 可获得约 ~60% dystrophin 阳性肌纤维,而 AAV9-μDys5 仅约 ~5%,约为 12 倍差异。
- 组织学改善(骨骼肌/心肌):治疗后可见病理负担下降,包括中央核肌纤维比例下降,以及纤维化与炎症浸润减轻;整体肌肉结构更接近正常。
- 功能恢复与保护:骨骼肌力量(如 TA specific force)与心脏应激下左室功能均出现明显改善;在老年小鼠中,治疗 7 个月仍维持显著保护效应,可抵御进行性肌肉萎缩与功能退化。
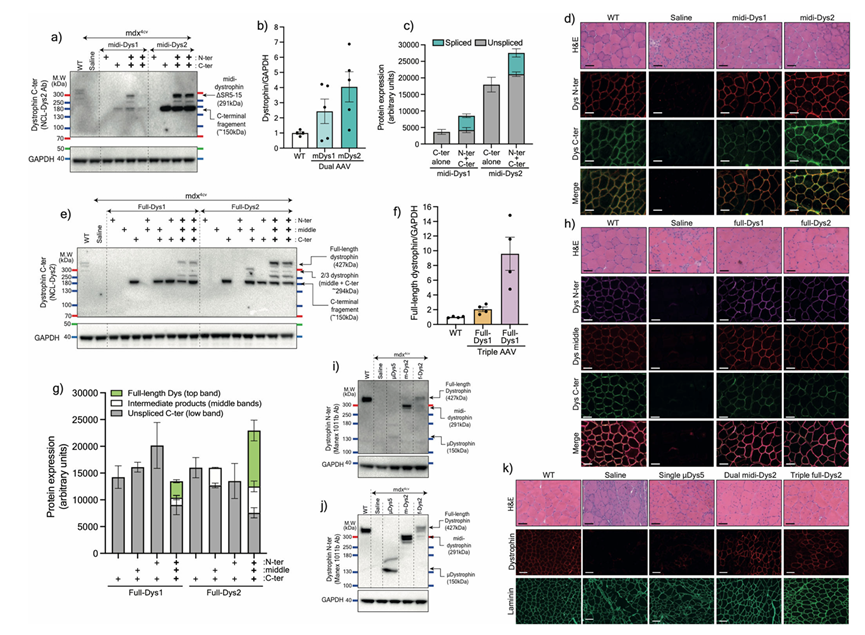
图14 在 mdx4cv 小鼠体内对 AAV6 分体 intein/Dys 构建体的验证。a)对照组或注射 5×10^10 vg 的 AAV6 N 端和/或 C 端分体 mini-Dys/intein 后的胫前肌(T.A)组织裂解液的 Western blot。b)以 GAPDH 归一化后的蛋白表达量,以及c)通过灰度分析(densitometry)计算剪接产物(上方条带)或未剪接产物(下方条带)的比例(WT n=4;注射肌肉 n=5)。d)采用两种不同的双载体组合处理后的胫前肌横切面:苏木精-伊红染色(H&E,上排;比例尺:50 μm),或用针对肌营养不良蛋白(dystrophin)N 端或 C 端结构域的抗体进行免疫标记(下排;比例尺:50 μm)。e)Western blot 显示采用三 AAV 载体策略处理后的胫前肌中全长肌营养不良蛋白的表达。f)全长肌营养不良蛋白表达量以 GAPDH 归一化,以及g)通过灰度分析定量不同产物的比例(每组 n=4 块肌肉)。h)肌肉横断面冷冻切片:H&E 染色(上排;比例尺:50 μm),或用针对 dystrophin 的 N 端、中部或 C 端片段的抗体进行免疫标记(下排;比例尺:50 μm)。i、j)Western blot 显示 WT、注射生理盐水的 mdx4cv,以及接受系统给药(总剂量 2×10^14 vg/kg)的 mdx4cv 小鼠在胫前肌(i)或心肌(j)中 dystrophin 的蛋白表达情况;处理方式包括单载体、双载体或三载体 AAV。k)胫前肌横切面:H&E 染色(上排;比例尺:50 μm),以及 dystrophin 或 laminin 的免疫荧光染色(下排;比例尺:100 μm)
意义:
相比 micro-Dys 策略,该方法递送的蛋白更接近生理结构,理论上可保留更完整的功能,为 DMD 基因治疗提供了新的思路。
四、技术选择的实践建议
在实际设计大基因递送方案时,以下几点建议可供参考:
2. 匹配靶组织的重组效率:分裂内含肽策略在分裂后细胞(神经元、肌肉细胞、光感受器等)中表现尤为稳健,因为这些细胞不依赖 DNA 复制来实现双链化。反之,在快速增殖的细胞类型中,DNA 重组策略可能效率较高。
5. 充分利用已发表的优化数据:针对 OTOF、ABCA4、DMD 等已有大量文献优化拆分位点和载体设计,建议充分参考现有数据,减少探索成本。
五、总结与展望
AAV的容量瓶颈虽然是一个巨大的挑战,但科学家们的智慧和创造力已经为我们开辟了多条“破限”之路。从DNA重组,到mRNA剪接,再到蛋白质自剪接,这些精妙的分子策略不仅极大地拓展了AAV的应用范围,更在多个重大疾病的治疗上展现出巨大的潜力,部分策略已推进到临床研究并出现积极结果。
未来,随着对这些重组机制更深入的理解、新型高效内含肽的发现与改造、以及更精准的基因编辑工具的涌现,我们有理由相信,AAV大基因递送技术将变得更加高效、安全和普适。
我们致力于走在这场技术革命的前沿,与广大科研同道一起,推动基因治疗跨越“容量”的边界,去探索更广阔的生命科学新大陆。
派真生物的技术平台与支持
我们致力于为科研人员提供稳定、可靠的工具病毒和技术支持,与您一同应对挑战。我们相信,强大的工具平台是推动科学发现的基石。
1.载体构建与咨询
面对一个大基因,选择合适的策略是成功的第一步。我们乐于与您共同探讨实验方案,并利用我们成熟的平台优势,将您的设计转化为高质量的AAV工具。
策略探讨:我们可以与您一起分析重叠法、反式剪接法和内含肽法等不同策略的利弊,结合您的具体研究目标和实验体系,提供我们的经验和看法。
载体构建:根据您最终确定的设计方案,我们提供高质量的质粒构建和AAV载体构建服务,确保您的研究建立在可靠的起点之上。
2. 高质量的病毒包装与质控
双载体策略的成功,高度依赖于两种 AAV 病毒的质量和精确的剂量配比。
严格的质控标准:我们提供高纯度、高滴度的AAV病毒,并通过qPCR、银染、ddPCR等多种手段确保病毒的滴度准确、纯度高、空壳率低。
参考文献:
[3] Yan Z, Zhang Y, Duan D, Engelhardt JF. Trans-splicing vectors expand the utility of adeno-associated virus for gene therapy. Proc Natl Acad Sci U S A. 2000, 97(12):6716-21.
[4] Riedmayr LM, Hinrichsmeyer KS, Thalhammer SB, Mittas DM, Karguth N, Otify DY, Böhm S, Weber VJ, Bartoschek MD, Splith V, Brümmer M, Ferreira R, Boon N, Wögenstein GM, Grimm C, Wijnholds J, Mehlfeld V, Michalakis S, Fenske S, Biel M, Becirovic E. mRNA trans-splicing dual AAV vectors for (epi)genome editing and gene therapy. Nat Commun. 2023, 14(1):6578.
[5] Mittas DM, Riedmayr LM, Gavrilov Z, Weber VJ, Otify DY, Mehlfeld V, Szalontai B, Ucambarlic E, Gandor C, Heigl T, Biel M, Becirovic E. Dual AAV vectors for efficient delivery of large transgenes. Nat Protoc. 2025.
[6] Tasfaout H, Halbert CL, McMillen TS, Allen JM, Reyes TR, Flint GV, Grimm D, Hauschka SD, Regnier M, Chamberlain JS. Split intein-mediated protein trans-splicing to express large dystrophins. Nature. 2024 632(8023):192-200.
[7] Lin J, Lin Y, Liu N, Cao W, Zhang J, Wen S, Zhang Y, Liao W, Hong Z, Lin Y, Liu Q, Liu H, Li Q, Chen B, Li M, Luo Z, Yang L, Yang Y, Zheng SH, Wang Y, Chu H, Hu Y, Qin Y, Luo BX, Tian S, Chen Y, Yan T, Yang L, Wang H, Liu T, Jiang Y, Lu Z. AAVLINK: A potent DNA-recombination method for large cargo delivery in gene therapy. Cell. 2026, 189(3):969-986.e17.
[8] Tang H, Wang H, Wang S, Hu SW, Lv J, Xun M, Gao K, Wang F, Chen Y, Wang D, Wang W, Li H, Shu Y. Hearing of Otof-deficient mice restored by trans-splicing of N- and C-terminal otoferlin. Hum Genet. 2023.142(2):289-304.
[9] 李华鹏,陈君霖,卜晔. 一种内含肽联用载体及其应用. CN118308390A[P]. 2024.07.09
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。