2025年12月,美国西北大学与陈-扎克伯格芝加哥生物中心(Chan Zuckerberg Biohub Chicago)的王宗杰团队在Advanced Science(IF=14)上发表了一项开创性研究,通过全基因组CRISPR敲除筛选,系统鉴定了调控LNP细胞摄取的关键遗传因子,并发现抑制PIK3CA基因可将LNP摄取效率提升高达5倍,为RNA治疗领域带来了一个全新的、可直接临床转化的增效策略。

研究亮点
首创”双端筛选”策略:区别于既往仅关注低摄取细胞的研究,本研究同时分离高摄取和低摄取细胞群体,首次系统鉴定出可增强LNP摄取的遗传靶点。
锁定PIK3CA金靶点:发现PI3K信号通路关键基因PIK3CA是LNP摄取的负调控因子,其抑制可使LNP内化效率提升高达5倍。
临床转化前景明确:使用已进入I期临床试验的PIK3CA抑制剂BAY1082439,在癌症和急性肝损伤两种截然不同的疾病模型中均显著
增强siRNA-LNP的治疗效果。
主要研究结果
1.全基因组CRISPR筛选:从18,053个基因中”淘金”
研究团队在结直肠癌SW480细胞系中引入Toronto KnockOut(TKOv3)全基因组CRISPR敲除文库,该文库涵盖针对18,053个蛋白编码基因的70,948条引导RNA(gRNA)。
细胞经LNP(装载荧光标记FAM-siRNA)处理后,通过荧光激活细胞分选(FACS)分离摄取量前5%和后5%的细胞亚群——两组细胞的中位荧光强度相差逾30倍(图1),直接证明了基因型对LNP摄取能力的深刻影响。随后通过二代测序(NGS)与DrugZ算法分析gRNA在不同亚群中的富集情况,计算NormZ评分,精准锁定驱动摄取增强或减弱的候选基因。
基因集富集分析(GSEA)与通路过代表性分析(ORA)进一步验证了筛选结果的生物学合理性:与摄取减少相关的基因显著富集于膜转运和囊泡运输通路(已知LNP内化机制),而与摄取增强相关的基因则在脂质转运与内体转运通路呈现相反的富集趋势,高度契合LNP经脂质介导的内吞和内体逃逸机制。值得注意的是,约20%的候选靶点为可成药基因,其中PIK3CA因其最高的NormZ评分和现成的临床级抑制剂脱颖而出。
递送效率的基因.png)
图1 鉴定促进脂质纳米颗粒(LNP)递送效率的基因
2.体外验证:PIK3CA抑制显著增强多癌种LNP递送效率
研究者选用临床阶段的PIK3CA抑制剂BAY1082439和RPS6KB1抑制剂RSS0680进行体外功能验证:
摄取效率:15 nM BAY1082439预处理24小时后,流式细胞术和荧光显微镜均检测到SW480细胞对Cy5标记LNP的胞内积累量显著增加,荧光信号强度较单纯LNP组提升高达5倍,且在实验浓度下未观察到显著细胞毒性。
功能验证:为进一步评估功能性基因沉默效果,研究者分别在携带KRAS G12V突变的SW480和SW620结直肠癌细胞中递送KRAS靶向siRNA,并在乳腺癌MDA-MB-231(KDM4A靶向siRNA)和肺癌H441(KIF11靶向siRNA)细胞中验证了通用性。结果显示:BAY1082439联合KRAS siRNA-LNP,对SW480和SW620细胞的生长抑制效果提升高达10倍。MDA-MB-231细胞的凋亡比例从20.1%提升至43.4%,H441细胞的凋亡/坏死比例从22.6%提升至40.5%。
机制研究表明,PIK3CA抑制通过促进细胞骨架驱动的摄取途径(如巨胞饮和吞噬作用)以及延缓早期内体向晚期内体的转化,从而延长LNP在早期内体中的驻留时间,增加内体逃逸的机会,最终提升siRNA的胞质递送效率。此外,该增效策略同样适用于搭载mRNA的LNP配方(ALC-0315、SM-102),充分说明其跨货物类型、跨配方的广泛适用性。
3.肿瘤模型体内验证:中位生存期倍增,KRAS蛋白表达显著下调
在SW480裸鼠皮下移植瘤模型中,研究者设置了四个治疗组:PBS对照组、BAY1082439单药组、KRAS siRNA-LNP组,以及BAY1082439(50 mg/kg,腹腔注射)联合KRAS siRNA-LNP(10 μg,瘤内注射,每2天一次)组(图2)。
结果显示:
(1)联合治疗组展现出显著的协同效应,肿瘤体积增长速率明显慢于两个单药组;
(2)中位生存期从PBS组的24天延长至联合治疗组的50天(延长100%);
(3)数字化Western Blot证实,联合组肿瘤内KRAS蛋白表达水平大幅降低;
(4)免疫组化(cleaved Caspase-3染色)显示,联合组瘤内细胞凋亡显著增加;
(5)生物发光成像实验还证实,无论是局部皮下注射还是全身尾静脉给药,PIK3CA抑制均能在不改变LNP生物分布模式的前提下整体提升LNP递送信号,具有良好的安全性特征。
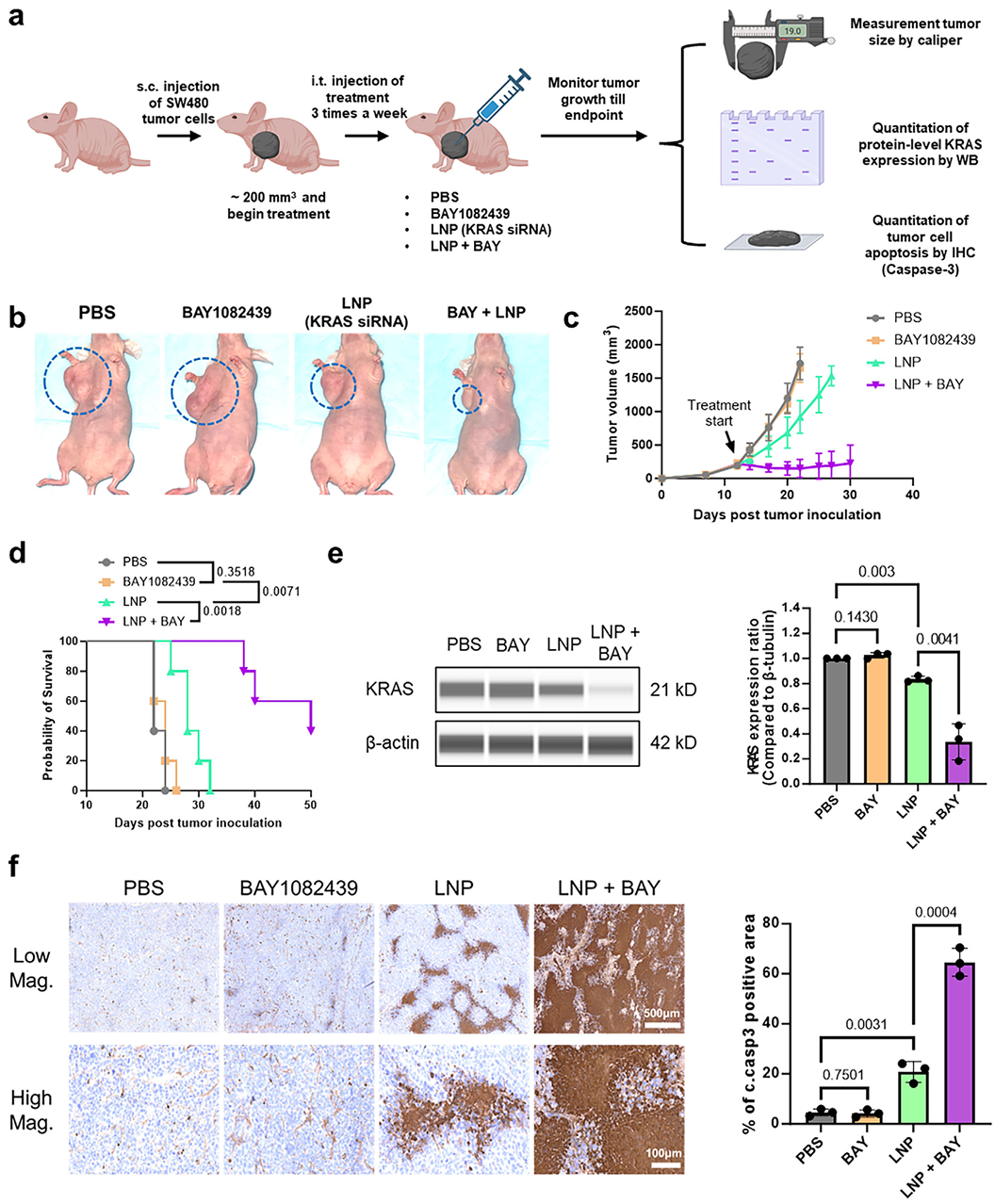
图2PIK3CA抑制增强siRNA负载LNP在小鼠癌症模型中的治疗效果
4.急性肝脏炎症模型验证:跨越癌症边界,拓展至非肿瘤适应症
为验证该策略的广泛适用性,研究者构建了对乙酰氨基酚(APAP)过量诱导的急性肝脏炎症小鼠模型(C57BL/6J,腹腔注射400 mg/kg APAP)。肝损伤后4小时给药,36小时后评估。结果显示,BAY1082439联合Bid siRNA-LNP治疗组中,血清ALT和AST活性显著降低(两者均为临床常用肝损伤生物标志物)。H&E病理切片显示,联合治疗组肝组织坏死面积明显减少,接近正常水平。对照的单纯LNP组仍可见大片坏死区域,提示单药LNP疗效不足。这一发现表明,PIK3CA抑制不仅适用于实体瘤,在非恶性炎症性疾病的LNP治疗场景中同样能够发挥显著的增效作用(图3)。
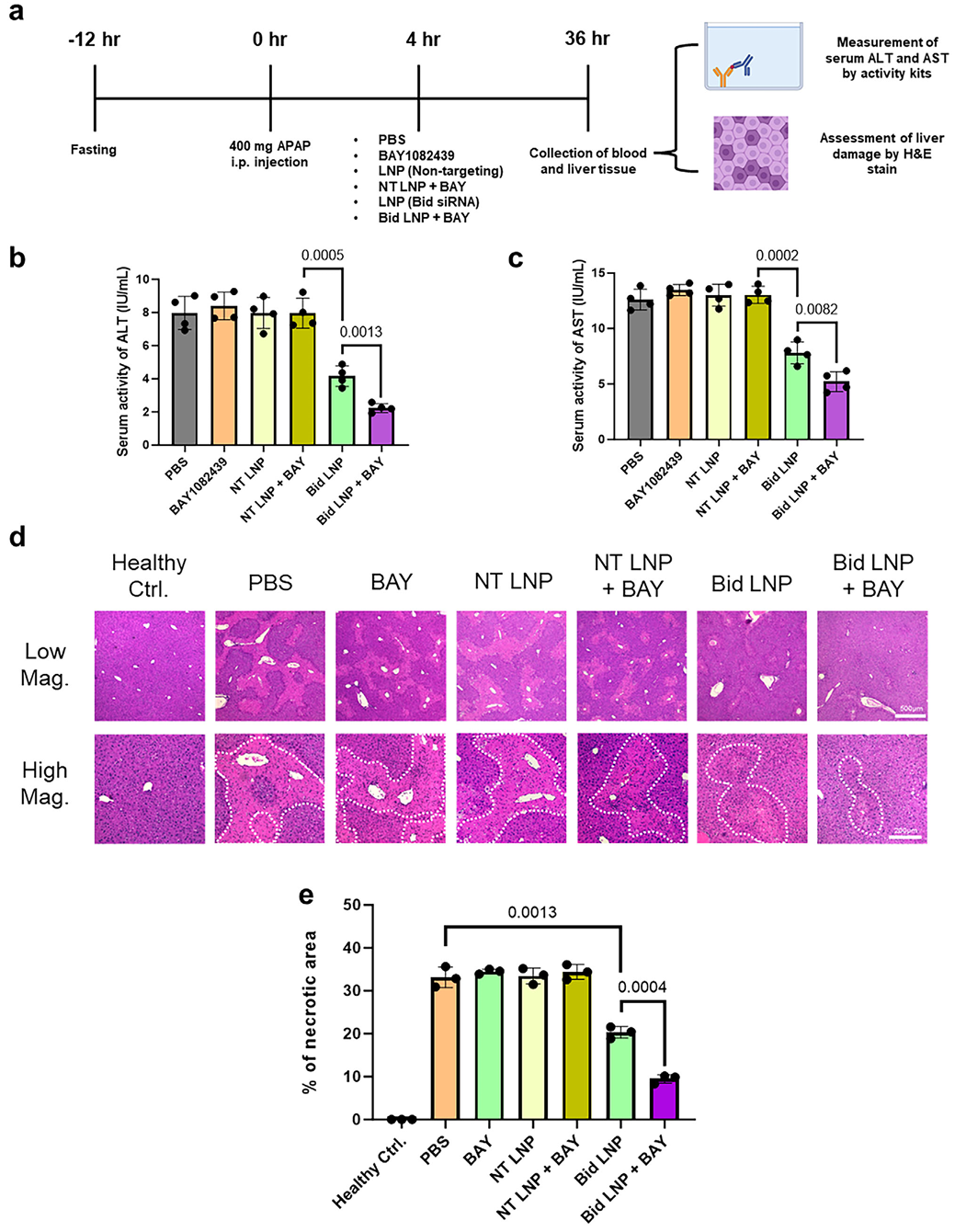
图3PIK3CA抑制增siRNA负载的LNP在小鼠急性肝脏炎症模型中的治疗效果
研究意义
这项研究代表了功能基因组学与纳米医学深度融合的一个重要里程碑。其核心创新之处在于:不再局限于”造更好的颗粒”,而是转变思路——靶向受体细胞的生物学特性来主动提升递送效率,且无需对LNP本身进行任何改造。
PIK3CA抑制剂BAY1082439已进入临床I期试验(NCT01728311),具备口服生物利用度和成熟的药代动力学数据,与LNP治疗联用具有极高的临床可行性。PIK3CA在人体中广泛表达(超过50%的器官呈中至高表达),这赋予了该策略跨组织类型的普适潜力。
对于基因治疗和RNA药物开发领域而言,这项研究的启示尤为深远:通过组合现有LNP配方 + 宿主细胞调控剂的策略,可以在不改动现有GMP工艺的基础上大幅提升疗效,极大降低了临床转化的门槛与成本。未来,该研究框架还为筛选其他具有更高NormZ评分的候选靶点提供了现成的范本,有望催生新一代LNP联合用药方案。
派真生物有幸为本研究提供了mRNA-LNP产品。如您有mRNA-LNP订购需求?请联系派真生物
参考资料:
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。