随着 mRNA 技术在疫苗、肿瘤治疗和基因编辑等领域快速发展,mRNA-LNP(脂质纳米颗粒)已成为当前最重要的递送平台之一。很多人知道实验室里可以制备 mRNA-LNP,但真正走向临床和产业化时,往往需要达到 GMP(Good Manufacturing Practice,药品生产质量管理规范)标准。
这意味着,产品不仅要“做得出来”,更要做到质量稳定、批次一致、过程可追溯,并满足监管要求。那么,GMP级 mRNA-LNP 制备到底需要注意哪些问题?
一、原材料质量是基础
GMP生产首先关注的是原材料质量。对于 mRNA-LNP 而言,主要包括两部分:mRNA原液和脂质原料。
mRNA原液
mRNA本身的质量会直接影响最终制剂效果,需要重点关注:
- 序列是否准确
- 帽结构(Cap)是否完整
- Poly(A)尾长度是否稳定
- 是否存在双链RNA(dsRNA)杂质
- RNA是否降解或截短
- 是否有内毒素或RNase污染
其中,dsRNA残留尤其需要重视,因为它可能引发非预期免疫反应。
脂质原料
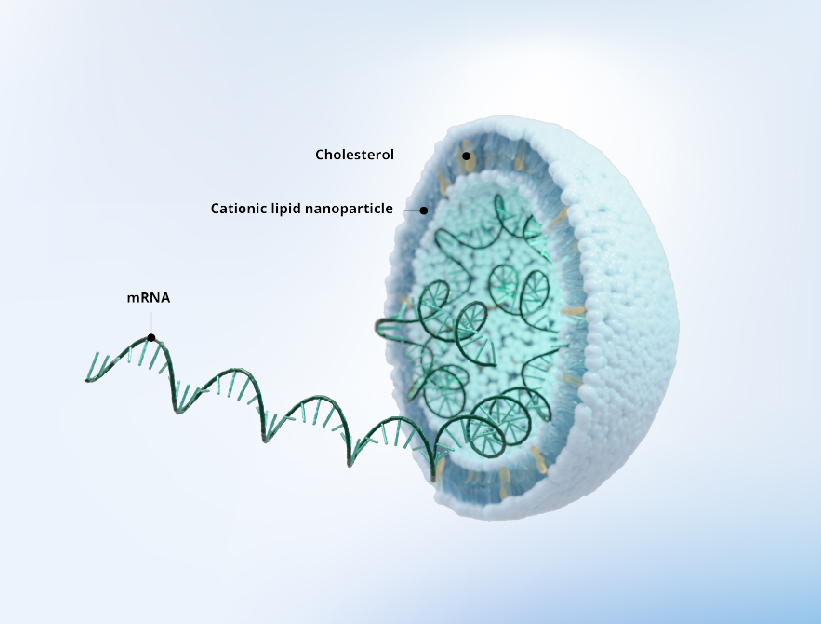
LNP通常由四类脂质组成:
- 可离子化脂质(Ionizable lipid)
- DSPC
- 胆固醇
- PEG脂质
这些脂质的纯度、稳定性和批次一致性非常关键。尤其是核心可离子化脂质,如果批次差异较大,可能导致粒径变化、包封率下降,甚至影响体内递送效率。
二、工艺参数决定产品表现
mRNA-LNP通常通过快速混合工艺制备,即将溶于乙醇的脂质相与含mRNA的水相快速混合,自组装形成纳米颗粒。
这一过程看似简单,但对工艺参数要求很高。
需要重点控制的参数包括:
流速比例(FRR)
即水相与有机相的体积比例。比例变化会影响颗粒大小和RNA包封率。
总流速(TFR)
混合速度越快,形成颗粒的动力学条件越不同,粒径和均一性也会受到影响。
pH条件
制备时通常采用酸性缓冲液,使脂质带正电并与RNA结合。如果pH控制不当,可能导致包封不足或RNA受损。
N/P比
指阳离子脂质与RNA磷酸基团的比例,是影响递送效率和安全性的关键指标。
三、从实验室到GMP生产,不是简单放大
很多团队在研发阶段使用微流控设备,小试数据很好,但放大到GMP生产后却发现性能明显变化。
原因在于:LNP形成高度依赖瞬时混合条件。设备型号、流道结构、剪切力和流速变化,都会影响最终颗粒特性。
因此,工艺放大不能只放大体积,更要做系统的工艺转移和一致性验证,确保商业批次与研发批次具备可比性。
四、无菌控制与RNase防护同样重要
由于 mRNA-LNP 多用于注射制剂,无菌要求非常高。生产环境通常需要符合洁净车间标准,并在无菌条件下完成灌装。
但相比微生物污染,mRNA产品还有一个特殊风险——RNase污染。
RNase广泛存在于环境、人体皮肤和普通耗材表面,一旦进入体系,会迅速降解RNA,导致产品失效。因此生产过程中通常需要:
- 使用RNase-free耗材
- 专用清洁流程
- 人员规范操作
- 环境监测与培训
五、质量检测是放行关键
GMP产品必须建立完整的质量检测体系。mRNA-LNP常见检测项目包括:
理化性质
- 粒径
- 多分散指数(PDI)
- Zeta电位
- pH值
- 渗透压
RNA相关指标
- RNA浓度
- 完整性
- 包封率
- dsRNA残留
- 残留DNA模板
安全性指标
- 无菌检查
- 内毒素
- 残留乙醇或其他溶剂
生物活性
- 细胞转染表达水平
- Potency assay(效价检测)
这些数据共同决定产品是否达到放行标准。
六、稳定性往往决定产品能否真正落地
mRNA-LNP本身较为脆弱,容易受到以下因素影响:
- 温度波动
- 冻融循环
- 氧化
- 聚集
- RNA水解
因此,很多产品会加入蔗糖、海藻糖等保护剂,并采用低温储存。
同时还需要开展系统稳定性研究,包括:
- 长期稳定性
- 加速稳定性
- 开瓶后使用稳定性
- 运输条件稳定性
如果稳定性不足,即使实验数据优秀,也很难真正实现临床应用和商业化供应。
七、文件体系和可追溯性不可忽视
GMP不仅是生产要求,也是管理体系要求。每一批产品都需要完整记录,包括:
- 原料来源
- 生产步骤
- 设备状态
- 人员操作记录
- 偏差与变更管理
- 检测结果
这些内容决定产品是否具备可追溯性,也是监管审查的重要部分。
八、结语
GMP级 mRNA-LNP 制备,远不只是把实验室配方搬进工厂。它涉及原料控制、工艺开发、设备放大、质量分析、稳定性研究以及完整的质量管理体系。
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。