近期,“rAAV研究先锋”RichardJudeSamulski在Molecular Therapy杂志(IF=12.1)上发表了一篇极具影响力的综述,系统回顾了AAV 技术40 年的演进,并展望人工智能驱动的衣壳工程、精准递送及rAAV药物的临床试验和商业化等未来趋势[1],该文无疑是理解AAV行业过去与未来的权威读物。前三期我们分别介绍了AAV药物临床试验进展与现实挑战,AAV载体设计,AAV的分子进化路径,包括载体工程的进展和定向进化平台,本期我们将继续介绍AAV的分子进化路径:包括理性进化平台以及计算机建模、AAV衣壳的跨物种筛选平台等。本文篇幅有点长,但内容非常有价值,相信您读完后一定会有收获。
AAV理性进化:结构驱动的精准设计之路
得益于结构解析技术和生物信息数据库的飞跃式发展,今日的理性设计已更加高效与可控。但在上世纪90年代,科学家对AAV衣壳结构、受体识别机制、免疫原性等方面的认知仍非常有限,使得早期的理性工程充满挑战。
早期AAV理性设计工作的基础,主要建立于:序列同源建模(Homology Modeling),经验性实验验证和以AAV2为核心模型的工程探索。当时,AAV2是唯一拥有成熟生产系统并进入人体临床试验的rAAV血清型,也具备良好的体外转导效率,因此成为AAV工程的“起点”。
1998年,Summerford & Samulski首次确认AAV2的主要细胞受体为硫酸乙酰肝素蛋白聚糖(HSPG),这是AAV研究史上的重大突破。此前,在31种真核细小病毒中,唯一已知的病毒受体是人B19细小病毒结合的红细胞P抗原。这项发现不仅揭示了AAV2与靶细胞结合的分子机制,也为后续的理性衣壳改造与定向递送提供了理论支撑。紧接着在1999年,Samulski实验室识别出共受体αVβ5整合素,Srivastava实验室确认了FGFR1(成纤维细胞生长因子受体)。这一系列发现帮助人们初步勾勒出AAV2转导过程的多步骤机制,为精准设计奠定了基础。
1999年,在缺乏高分辨率晶体结构数据的背景下,Girod等人通过与犬细小病毒(CPV)等已解析结构对比,预测了AAV2衣壳上六个表面暴露环区(loops)。他们在其中一个环区插入了L14肽段(RGD基序),实现了向整合素受体的靶向递送,从而成功绕过HSPG依赖路径。这一研究首次证明:AAV衣壳可通过精准插入功能配体实现靶向性重定向;理性突变可赋予AAV在原本难以感染细胞中的转导能力。这项工作成为后续所有理性设计策略的奠基之作,并为肌肉、神经等组织的特异性基因治疗提供了技术原型。
在2000年,Muzyczka团队开展了AAV2衣壳的大规模位点定向突变研究,在59个位置共构建了93种突变体,系统性探索衣壳结构域在组织嗜性、免疫原性、细胞进入与基因组包装中的功能。其中最关键的突变之一是:将AAV2中585-RGNR/AQAA-588位点中的保守基序突变为丙氨酸(Ala),这是AAV2与HSPG结合的关键区域,直接影响其天然靶向性。此研究首次从结构层面构建了衣壳功能图谱(structure-function map),为后续AAV2定向组织递送的理性改造奠定了基础。
同年,Wobus等人通过单克隆抗体(MAb)定位了AAV2衣壳上的关键抗原位点,进一步确认了免疫识别与细胞附着区域,为免疫逃逸型AAV设计提供了靶点,特别适用于重复给药或长期疗效维持的临床需求。
回顾病毒结构生物学的发展:1953年,Franklin和Gosling拍摄的“照片51”首次证实了DNA的双螺旋结构;1958年,Kendrew首次解析了肌红蛋白的X射线晶体结构;1991年,Tsao等人解析了犬细小病毒(CPV)的三维结构,为AAV结构预测提供了模板;2002年,Xie等人首次公布了AAV2衣壳的高分辨率晶体结构,为后续的理性设计、配体插入与结构建模打开大门。然而,作者也指出:AAV结构的复杂性远超“晶体图片”所能展现的那样,它包含了众多难以预测的动态生物物理现象与多层分子调控机制。
尽管我们已对AAV衣壳的功能域与受体互作有了系统理解,但直到2007年,Srivastava团队首次揭示:AAV2衣壳可被EGFR蛋白酪氨酸激酶磷酸化,磷酸化后触发泛素化(ubiquitination),进而导致胞内运输效率下降,入核受限,转导效率降低。于是,在2008年,研究团队将表面暴露的酪氨酸位点(Y)通过定向突变替换为苯丙氨酸(F),避免其被修饰。代表性成果是AAV2(Y444F、Y500F、Y730F)三位点突变体,在动物实验中显著提升了转导效率,并已进入I/II期临床试验,验证了靶向翻译后修饰的衣壳工程在基因治疗中的临床价值。
AAV衣壳蛋白的翻译后修饰(Post-Translational Modifications,PTMs),不仅发生于体内转导过程,也可能在生产与储存阶段就已发生。研究发现,某些PTMs会显著影响AAV的转导效率,受体结合能力,粒子稳定性和免疫识别,影响因素包括但不限于:表达体系(如HEK293、Sf9等宿主细胞)、纯化方法(亲和、密度梯度等)、储存缓冲液与温度等条件。因此,在制造过程中深入理解并控制PTMs,已成为确保AAV产品质量一致性、临床有效性与可重复性的关键一步。
“大自然并不会在GMP洁净室中生产AAV”。在野生型感染中,AAV的产生通常伴随着腺病毒诱导的细胞裂解过程,其释放出的AAV粒子常附带:宿主细胞蛋白,辅助病毒蛋白,这些蛋白可能残留于AAV粒子的内外表面,并深度参与AAV的体内行为,如:生物分布、细胞识别、免疫系统响应等。
虽然当前生产趋势追求超高纯度载体,但一些研究团队却试图 “模拟自然环境”,通过在AAV配方中加入特定结合或屏蔽蛋白,增强其组织特异性、免疫逃逸能力和体内稳定性。例如,已有研究显示AAV会与血清蛋白发生结合,这提示我们:AAV在不同组织液(如玻璃体液、脑脊液、血清)中可能与可溶性蛋白形成不同“蛋白壳层”,这些蛋白可能承担运输(shuttle)与屏蔽(shielding)的角色;AAV的给药途径及其所处微环境可能比我们当前认知的更为复杂多变。
衣壳与蛋白之间的互作不仅由序列决定,还与电荷分布、pH变化、磷酸化等修饰状态紧密相关。蛋白之间的静电力学相互作用会影响其热力学与动力学行为,进而改变AAV的受体结合力与体内行为模式。例如:AAV2的HSPG结合位点正是通过表面静电势计算预测并实验验证的,这也激发了后续团队系统分析不同血清型的表面电荷图谱,为理性设计新型AAV衣壳提供依据(图1A)。
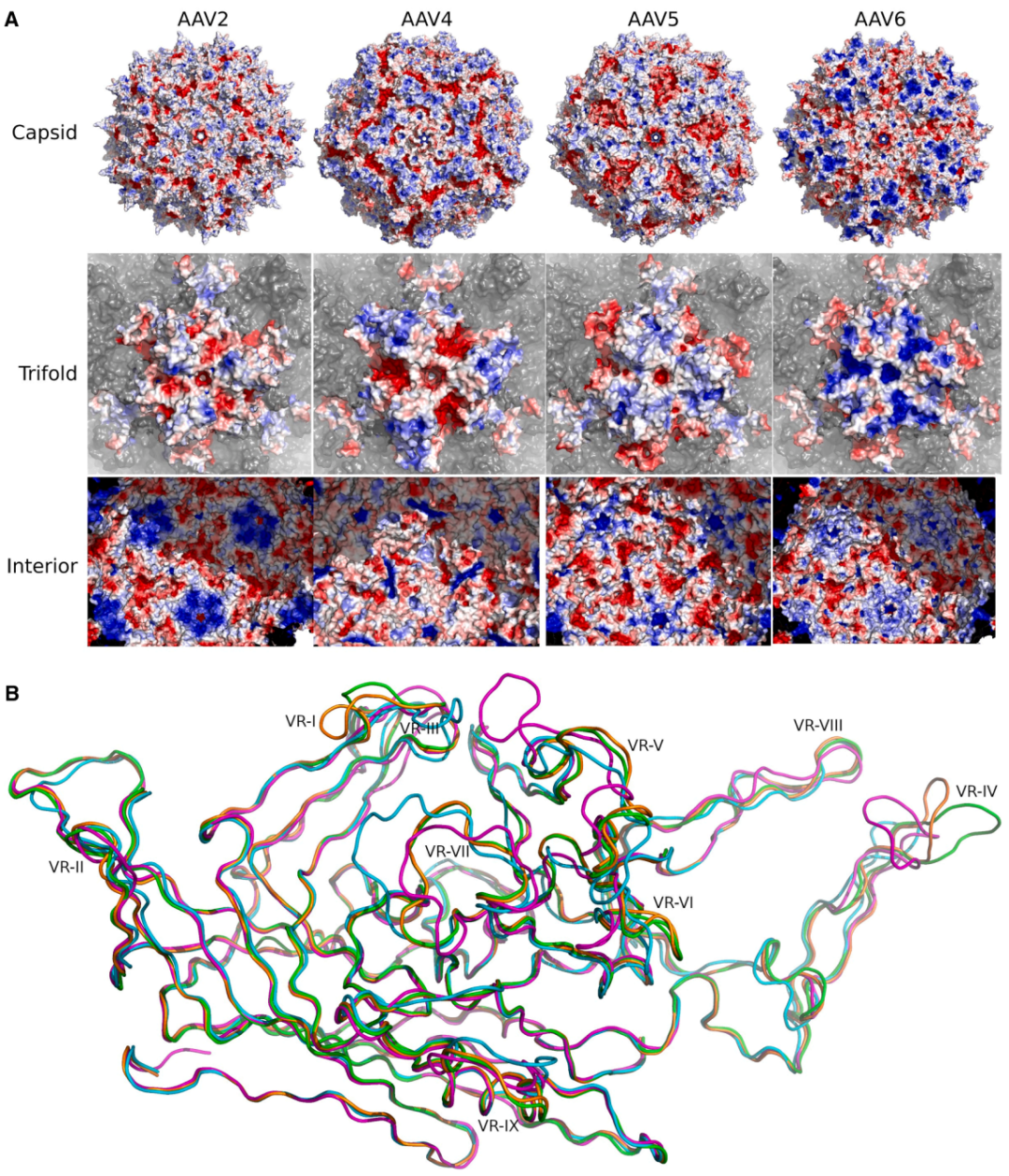
图1 AAV电荷密度分布图。
(A)衣壳电势图。对各血清型衣壳的溶剂可及表面按电势值上色,色阶为红‑白‑蓝渐变,对应 −4 kT/e 到 4 kT/e(约 −100 mV 至 +100 mV,25 °C)。依次展示:以五重对称轴为中心的完整衣壳、以三重对称轴为中心的衣壳以及衣壳内表面。为便于观察,在三重对称轴示意图中,未聚焦的衣壳表面以半透明灰色显示。(B)VP3结构对比。将AAV2(绿色)、AAV4(品红色)、AAV5(青色)和AAV9(橙色)的VP3结构域叠合,均以蛋白主链丝带形式呈现,直观展示它们的构象差异。
AAV 各血清型在维系衣壳稳定性和结构完整性所需的关键区域上高度保守,同时又在决定表型多样性与受体特异性的可变区呈现显著差异。随着分子生物学技术和 DNA 测序手段的飞速发展,天然 AAV 血清型及其变体的“谱系”不断扩充,为载体工程提供了更加丰富的素材库。伴随着数据量的激增,基于同源性的去卷积策略(homology‑based deconvolution)已成为 AAV 理性设计的核心方法之一,可在不同血清型间实现“知识迁移”,预测并构建具有更高治疗潜力的新型衣壳(图 1B)。
2010年,Samulski团队通过位点定向突变技术,改造了AAV2衣壳中位于VR-VIII环区的六肽序列(585-RGNRQA-590),将其替换为其他血清型及非人灵长类来源的对应氨基酸,从而构建出一系列AAV2内环突变体(AAV2i系列)。其中,AAV2i8(AAV2与AAV8的嵌合体)展现出显著的组织靶向性改变:从肝脏递送成功“重定向”至骨骼肌递送,同时对人抗AAV2血清的中和抵抗能力增强,提示其具备更好的免疫逃逸性能。目前,AAV2i8已进入II期临床试验,成为理性设计改进组织靶向性+免疫逃逸双重突破的典型示范。
2012年,AAV2.5成为首个通过结构设计进入临床的嵌合型AAV载体,用于杜氏肌营养不良(DMD)治疗的随机双盲临床试验。该载体融合了AAV1的肌肉递送能力,AAV2的工程平台优势与表达稳定性,并整合了抗原表位修饰以获得抵抗中和抗体的能力。AAV2.5在临床试验中被证实安全、耐受性良好,为后续设计如AAV2G9、AAV2i8G9等嵌合载体打下基础,推动了结构驱动的AAV设计全面走向特定疾病靶向递送与免疫应答规避的时代。
2015年,Luk H. Vandenberghe 团队开创性地引入祖先序列重建(Ancestral Sequence Reconstruction, ASR)方法,预测出一组具有进化代表性的AAV祖先衣壳序列,构建了包含9个“进化节点”的候选序列群。最终,研究团队从中筛选出性能最优的Anc80L65,其具有以下显著特点:被预测为AAV1-3与AAV7-9的共同祖先序列;在肝脏、肌肉、视网膜等组织中均展现出极高的体内转导效率;可作为无天然血清来源的“合成型血清型”,规避人群中常见抗体中和风险。Anc80L65的成功,标志着AAV理性设计由结构域突变和嵌合融合,进化至基于系统进化理论的前沿策略。
人工智能赋能AAV设计:加速基因治疗载体的理性进化
在过去,AAV衣壳工程主要依赖定点突变、饱和突变、结构建模与实验验证等方式,这些方法虽然有效,却耗时长、成本高,探索效率有限。如今,随着人工智能(AI)与机器学习(ML)的迅猛发展,越来越多研究者开始将AI建模与高通量数据融合,用于加速新型AAV衣壳的筛选与优化。
研究者绘制了AAV衣壳的适应性景观图谱(fitness landscape),并通过系统突变分析发现VP1区内潜藏的移码基因MAAP,该基因能通过竞争性排斥机制限制AAV产量。这项工作首次展示了基因组适应性图谱+AI指导设计在揭示AAV生物学机制与衣壳优化方面的巨大潜力。
研究者利用神经网络(ANN)与支持向量机(SVM),预测突变AAV衣壳是否可正确组装。结果发现:特定位点(如N495、G546、I554)与组装能力密切相关,通过ML模型训练生成了新文库,验证了机器学习在预测性结构筛选中的应用价值。
2024年:AI工具走向结构预测与多性状优化
提出了APPRAISE(自动化肽–受体配对分析)方法,利用AlphaFold-Multimer或ESMFold进行结构建模,快速评估蛋白与靶点结合的结构可能性,广泛适用于AAV衣壳、Mini蛋白、纳米抗体、多肽等多类蛋白设计任务。该方法准确性高、结果可解释性强、适应范围广,是结构预测与功能分析结合的AI工具。
随着机器学习、人工智能与计算建模技术的快速发展,AAV衣壳工程正迎来一次前所未有的“计算驱动式理性进化”。然而,这种转变不会在“计算孤岛”中独立完成,而是必须依托于实验验证与循环迭代的协同推进。要真正提升AI模型的预测力与解释性,离不开高质量(High-quality)、多样化(Diverse)、强鲁棒性(Robust)的训练数据。
在当前AI应用热潮之下,数据偏倚(data bias)这一问题往往被忽视。事实上,AAV衣壳的筛选结果高度依赖实验条件、宿主背景、选择压力等因素,若AI模型训练数据未能覆盖这些复杂变量,预测结果可能强化偏差而非消除误差。因此,将以往的AAV实验工程经验系统化整合进模型构建中,不仅是“预测”,更是真正实现“创新”的必要条件。
下一代测序(NGS)技术无疑将在AAV衣壳工程的下一个阶段发挥关键作用,助力我们设计并评估靶向更精准、基因递送效率更高且免疫原性更低的新型变体。然而,需要明确的是,AAV绝不仅仅是一种静态的蛋白结构;它是一个动态的多组分体系,会与多种细胞及血清蛋白、不同受体和辅助受体以组织特异的方式相互作用。这一复杂性必须在计算模型中得到充分体现,否则将导致过度简化并误读其生物学意义。
归根结底,AAV工程的未来在于“计算预测+实验验证”的协同路径:计算模型为理性衣壳设计指明方向,但实验验证仍是评判优劣的金标准。唯有纠正数据偏差、依托高质量数据集精炼机器学习策略,并持续融入实验洞见,才能突破当前AAV基因治疗的局限,迈向精准工程的全新时代。
跨物种AAV文库与其他思考:来自进化边界的反思
作为科研共同体,我们始终尊重动物伦理与跨物种公平,但也必须面对一个现实:不同物种之间存在不可忽视的遗传差异,即便是同一物种内的不同品系,也会存在显著的分子差异。这些差异体现在多个维度:蛋白质氨基酸序列的差异;三维结构构象不同;翻译后修饰(PTMs)模式的独特性;以及包括表观遗传调控、剪接机制、物种/品系特异性宿主因子(如LY6A蛋白)在内的深层生物学变量。
大自然才是真正的“分子工程师”,她所采用的分子生物学工具——甚至包括我们尚未发现的机制——早已实现了种间传播的自然感染路径。相比之下,我们人类对于这些机制的模拟往往仍处于“理解中复杂、操作中受限”的阶段。
筛选 ≠ 临床:多物种筛选带来的希望与失望
AAV的研发历程往往经历如下阶段:小鼠 → 猪或狗 → 非人灵长类(NHP) → 人源细胞或组织 → 临床试验。然而,进化不是线性的。一个在动物模型或类器官系统中表现优异的AAV变体,在人体中却可能失效——这是AAV研发者反复经历的真实困境。
尽管存在挑战,全球多个团队仍持续推进AAV衣壳工程的前沿探索,代表性进展包括:
- AAV2.GL / AAV2.NN:针对眼科疾病优化;
- MYOAAV / AAVMYO系列:精准靶向骨骼肌;
- AAV-BI-hTFR1:优化用于中枢神经系统(CNS);
- AAV.k13 / AAV.k20:专为肾脏递送设计。
这些创新成果充分体现了利用自然复杂性打造跨物种适配+组织靶向递送的策略。同时,也推动了人源化小鼠模型、人组织切片模型等研究平台的兴起,为科研界更大范围地接近临床验证环境提供可能。尽管越来越多优秀的AAV变体被发现,大多数却从未进入临床研究阶段,更难撼动FDA已批准的第一代衣壳(如AAV2、AAV9等)在治疗中的“默认地位”。这种“进化天花板”背后的现实包括:监管路径高度成熟、已批准载体具备先发优势;转化验证成本极高,资源集中度高;行业惯性导致新变体即使性能更好,也难获广泛临床采纳。因此,越来越多研究者选择聚焦于更接近临床情境的模型进行验证,如人源细胞系、类器官、人源敲入模型, 以应对传统动物模型的“类临床偏差”,提高候选载体的人体相关性与转化成功率。
Ex Vivo器官模型:推动AAV基因治疗走向临床的桥梁
近年来,AAV载体工程的研究已逐步从“跨物种筛选”迈向更接近人体实际状态的人类器官。相比动物模型,人类器官在以下方面具有更高的临床相关性:真实反映组织特异性表观遗传修饰(如DNA甲基化、组蛋白修饰、染色质可及性);展现人源信号通路与蛋白互作网络;保持器官级别的受体表达谱与细胞微环境。这种模型能更有效评估AAV衣壳在真实组织内的表达效率与递送特异性,被认为是连接临床前研究与临床应用的关键中间环节。
虽然ex vivo器官模型具备高度组织真实度,但也存在一些天然局限:缺乏完整免疫系统,时间窗口有限,不同个体器官状态差异大。因此,科学家们开始探索人体遗体模型(decedent model):使用临床判定脑死亡但不具器官捐献资格的个体,开展诸如猪-人异种移植研究。这种 “类临床”人体模型在心脏、肾脏等器官的异种移植研究中快速发展,推动了这些领域的科研进展。
当我们思考当前AAV筛选系统(如啮齿类动物、非人灵长类动物、外植器官等)对候选治疗性载体所带来的优劣势时,最终总会回到同一个核心问题:“它在人类中到底会表现如何?”这始终是AAV基因治疗研发无法回避的终极变量,也是所有前临床模型与验证体系需要直面的 “跨越鸿沟”。在动物模型中再出色的转导效率、组织特异性与免疫耐受性,若无法在人体中重现,便难以真正推动临床应用。因此,下一阶段AAV工程的关键词不再只是“优化”,而应是——“真实相关性(Human Relevance)”与“转化可靠性(Translational Reliability)”。
在人体中筛选AAV?听起来激进,其实我们早已开始
在过去25年中,AAV衣壳的工程优化始终围绕一个目标展开:找到最适用于人体临床试验的病毒递送系统。如今,这场“从动物到人体”的循环正在逐步回到原点——“那就直接在人类中进行筛选吧”。
尽管这一理念听起来令人不安,但实际上这并非首次提出,甚至已有多项成功的人体实践基础。
四十多年前,噬菌体展示文库载体(Phage Display Library Vector)诞生于1985年,并在不久后完成了其历史性的一步——首次进入人体进行靶向配体筛选。尽管这项成果在分子药物与肿瘤靶向领域意义非凡,却长期未被基因治疗领域充分重视。与此同时,AAV文库也在1980年代末期悄然诞生,但在实际临床路径上的进展始终缓慢。即便2012年欧洲EMA批准了首个AAV基因治疗产品Glybera,建立了临床安全性基础,整个领域仍深陷于“小鼠→NHP→人体”的临床前优化循环,难以实质突破临床转化瓶颈。
如今,为效仿噬菌体展示在人体筛选中的成功路径,M34公司完成了一项开创性尝试(未公开数据):
实验对象:3位人体捐献者(2男1女,合法脑死亡,非器官捐献者)。
递送系统:
- 4个AAV文库(基于AAV5、AAVrh10、AAV9);
- 4个已获FDA批准的野生型衣壳(AAV2、AAV8、AAV9、AAVrh10);
- 4个工程化AAV变体。
设计亮点:
- 文库均含有随机9-mer肽段(7个de novo插入+2个突变);
- 插入位点集中于VR-VIII环区(血清型决定区);
- 使用NNK简并密码子策略以保证多样性;
- AAV5与AAVrh10文库基于SEBIR平台构建(Selection Based on inter-ITR Recombination)。
在三位捐献者身上,研究团队采集了100余份组织样本(包括肝脏、心脏、脊髓、大脑等),并发现多个组织适应性良好的AAV新变体。这些变体已被成功克隆、包装并递送至小鼠体内,实现了首次记录在案的从人到鼠(Human-to-Mouse)的“反向跨物种进化”。这一策略的目标是推动人源→动物模型→临床的真正闭环,以更接近人类真实条件下评估衣壳性能。
此类人体筛选系统中,研究者可以真实模拟临床递送情境,包括但不限于:AAV衣壳与人血清蛋白互作、活跃免疫系统对病毒的应答、体内生物分布与器官倾向性、病毒清除速度与血浆滞留时间、血管与组织微环境影响递送路径等。我们正向着真正意义上的Human-to-Human(H2H)AAV筛选体系迈进。
小结:基因治疗的下一程,是“回到未来”
AAV进化的终点,或许就是它的起点:不再局限于动物筛选,不再绕行于模型间的误差;直接回到人体,在真实生物学语境中寻找最合适的载体,以此推动更安全、更精准、更有效的下一代AAV疗法(图2)。
AAV的未来,不在模型中,而在人类自身中等待被发现。
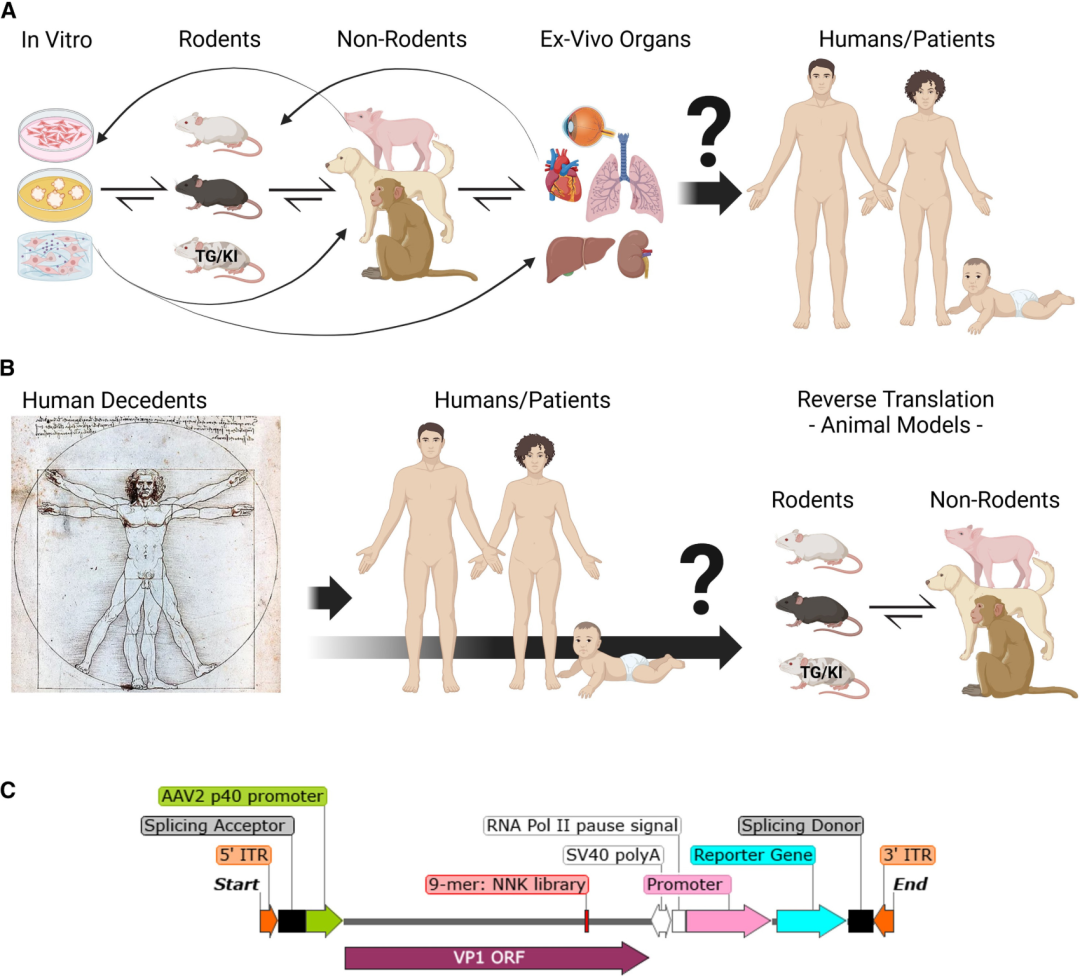
图2不同AAV进化策略的示意图。
(A)不同AAV定向进化策略的概述,涵盖了一系列体外及体内模型。初筛阶段主要在体外系统中进行,如细胞系、类器官以及三维细胞培养,随后是体内模型,包括啮齿类动物(如C57BL/6J、BALB/cJ等野生型小鼠,以及转基因(TG)和敲入(KI)小鼠模型)。进化筛选还会扩展到非啮齿类动物,如猪、狗和非人灵长类动物。此外,还采用了更具创新性的技术手段,比如离体器官灌注和组织离体培养(例如人视网膜离体组织,以及肺、心脏、肝脏和肾脏等器官)。尽管这些方法不断进步,但现有动物和体外模型本身存在的局限性,依然对许多已进化衣壳在人体患者中的转化潜力提出了疑问。(B)展示了M34团队的创新策略:利用人类遗体(以达·芬奇的“维特鲁威人”为代表)进行AAV衣壳筛选、体内分布及靶向研究。这一策略通过Human-to-Human(H2H)项目,强调了直接向临床人类患者转化的可能性。同时,团队还从人类反向翻译到动物模型,筛选出既适用于人类、又可用于人类疾病动物模型的AAV衣壳。(C)SEBIR平台的示意图,该平台基于AAV2衍生的重组基因组和AAV为基础的9肽衣壳文库。其质粒构建包括5ʹ剪接受体位点、AAV2 p40启动子区、工程化的VP1开放阅读框(ORF),后接双向SV40多聚腺苷酸化信号(SV40 PolyA)及RNA聚合酶II转录暂停信号。此外,该质粒还含有由特定启动子驱动的报告基因与3′剪接供体位点,整个结构两端均由反向末端重复序列(ITRs)包裹。
参考资料:
1. Lester Suarez-Amaran,Liujiang Song, Anna P. Tretiakova,et al.AAV Vector Development, Back to the Future. Molecular Therapy. 2025; 33(5): 1903 – 1936.https://doi.org/10.1016/j.ymthe.2025.03.064
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。