腺相关病毒(Adeno-associated virus, AAV)作为一种安全高效的基因递送载体,深受广大科研人员偏爱,常被用于体内基因敲低、基因过表达、基因编辑、动物的模型的构建和基因治疗。然而,AAV的应用涉及众多关键因素,稍有疏忽便可能引发各种问题,影响实验的顺利进行。因此,我们特别整理了使用AAV时容易踩到的“坑”,希望大家在实验中能够提前规避,从而获得理想的实验结果。
一、”一剂量定结论“
常犯的错误:在使用AAV进行实验时,很多研究者常常直接套用文献中的注射剂量。部分研究者为了赶进度,更是直接照搬文献中的参数。这种做法虽然看似保险,实则暗藏隐患。因为不同实验室的AAV滴度定量方法、实验操作细节以及实验动物的遗传背景等因素存在差异,这使得AAV的注射剂量并不能简单地一概而论。
正确的做法:在正式实验之前设置浓度梯度进行预实验,确定最合适的AAV使用剂量。
举例:为了评估AAV介导的光遗传学工具在RGCs中的剂量依赖性表达及其对视觉功能恢复的影响,通过给三重敲除(TKO)盲鼠模型(Opn4−/−Gnat1−/−Cnga3−/−)的玻璃体注射不同剂量的病毒载体(1.5×10⁷至1.5×10¹⁰vg/眼),确定了最佳病毒剂量范围(约10⁸ vg/眼,图1)[1]。
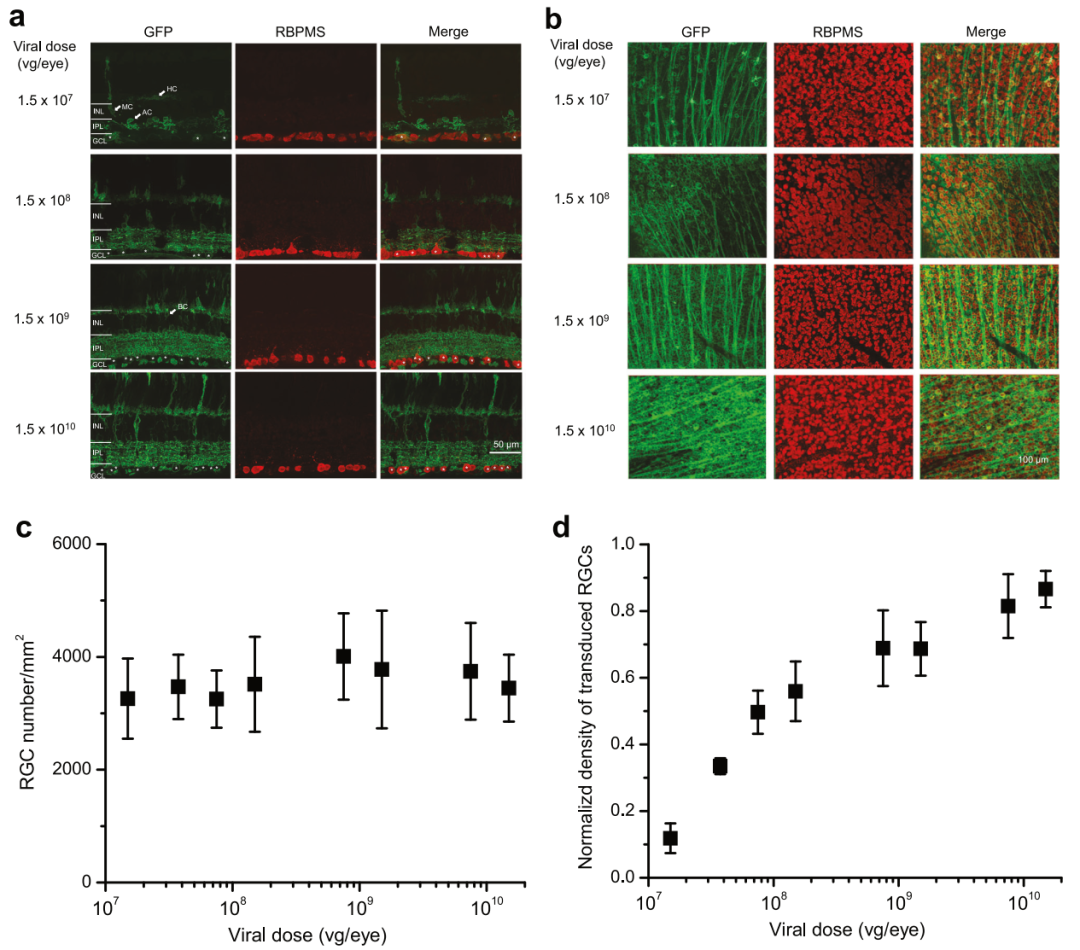
图1 转导效率的病毒剂量依赖关系
体外实验梯度设计方案(供参考):

小鼠体内实验梯度设计方案(供参考):
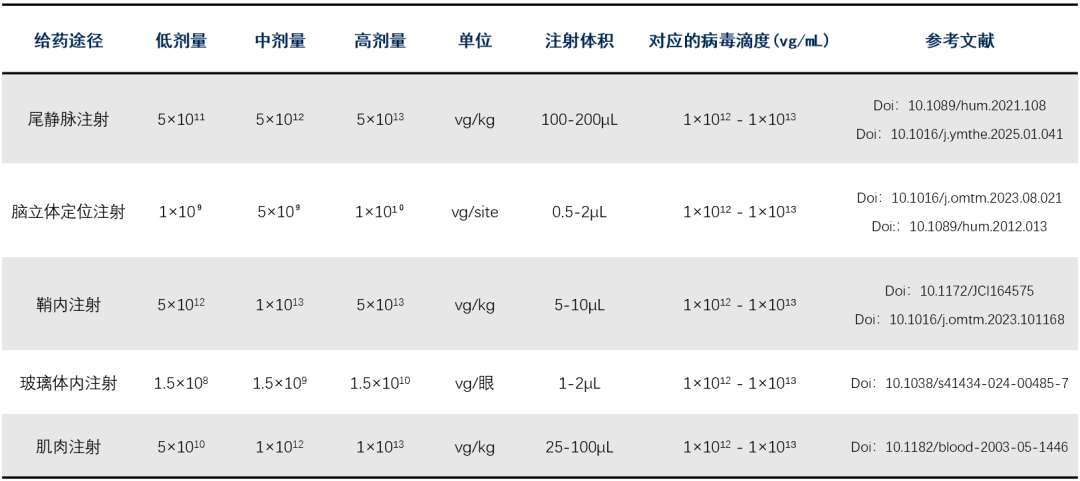
注意:成年小鼠体重约20-25克
操作建议
- 首次实验使用3-5个剂量梯度,确定大致剂量区间。
- 第二轮实验聚焦最佳区间,使用较小间隔(2-3倍)的3-4个剂量点。
二、 对照组缺失或设置不当
常犯的错误:在使用AAV进行实验时,为了节省成本,只设实验组,没有阴性对照和阳性对照组;或者对照组设置不当。
正确的做法:除了实验组以外,根据实验需要,设置阴性对照组和阳性对照组。
(1) 阴性对照组
- 未处理对照:不做任何处理的样本,用于确定基线水平和系统背景。
- 假手术对照:注射PBS或生理盐水,模拟注射操作的物理过程,确保实验组和对照组在操作条件上尽可能一致。
- 空载体对照:含相同血清型但不含目的基因表达盒的AAV载体,用于评估空壳体介导的细胞内信号和免疫反应是否会影响表型。
注意:空载体≠PBS/生理盐水,两者结果常有显著差异
(2) 阳性对照组(以下至少选一)
- 标准报告基因载体:相同血清型的AAV-GFP或AAV-luciferase,用于验证AAV载体系统的感染性。
- 已知有效的治疗载体:已发表研究中证实有效的AAV制剂,用于提供有效性的参考基准。
举例:为了研究纹状体中两轮AAV注射导致的星形胶质细胞向神经元转化的效果,作者设置了同血清型GFP对照组,以验证AAV载体系统的感染效率;同时设置了假手术(Sham)组,以排除注射操作本身对实验结果的潜在影响(图2)[11]。
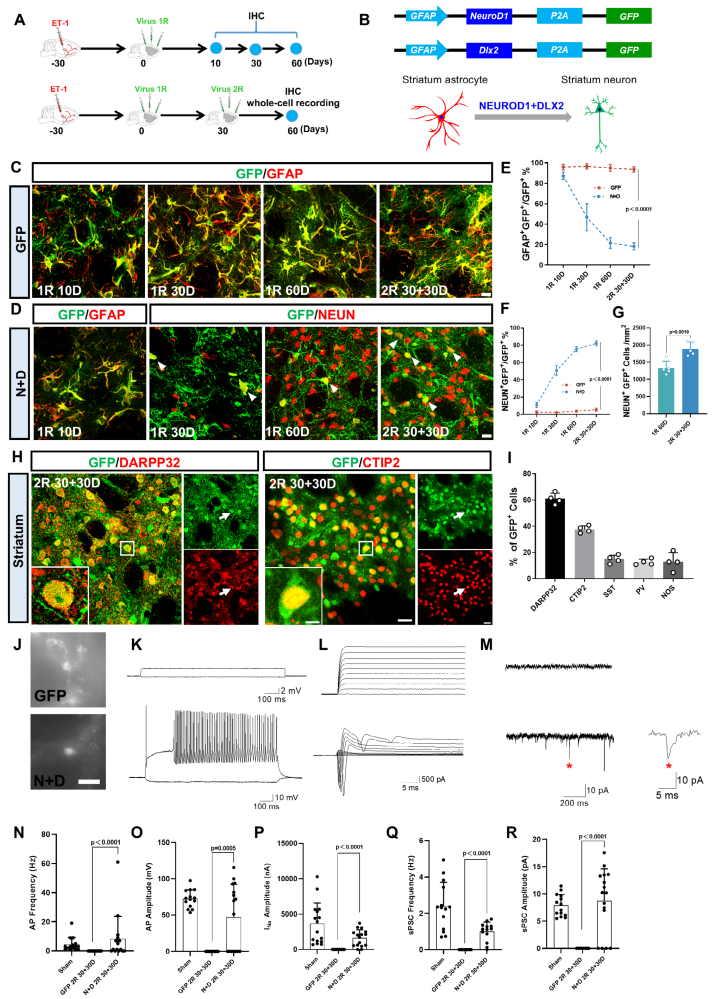
图2 纹状体中两轮AAV介导的星形胶质细胞向神经元转化[11]。
三、常见AAV感染低效问题及解决方案
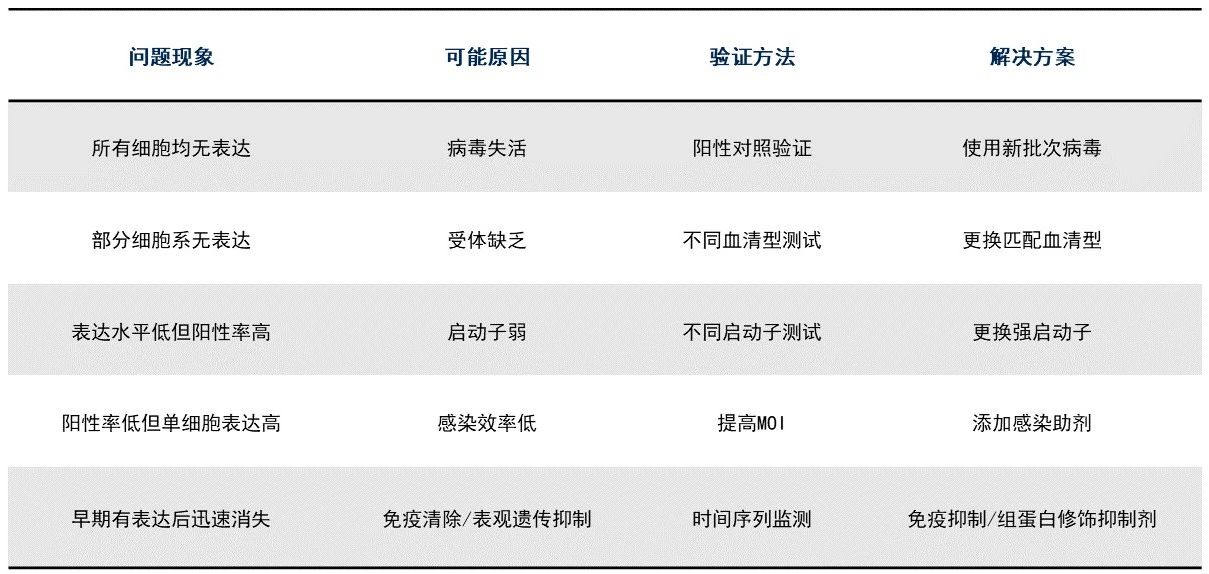
成功的AAV实验需要系统化的设计、精确的执行和科学的分析。本文强调剂量梯度和对照组设计的重要性,希望能帮助研究者避开常见陷阱,获得可靠、可重现的实验结果。
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。