基于上万批次的AAV放行检测成功经验,派真生物率先完成分析方法学开发和方法学验证,并积累了多个项目执行经验。特别是关键的检测项目,如感染滴度(TCID50)、AUC空壳率检测和rcAAV检测等。派真以客户需求为导向,建立了一站式临床前生物药物分析检测服务平台,拥有庞大的数据库,覆盖方法开发、方法验证、批放行检测,能为产品的中间控制和终产品的放行提供全面完善的检测服务,具有包括细胞库、菌株库、质粒、AAV在内的健全的质量标准体系,为满足客户在成药性研究,质量研究,质量控制等方面提供专业的技术支持,能够满足客户不同分析方法开发的需求。派真已成功服务数个IND申报的GMP批放行检测,为AAV基因药物的安全性和有效性保驾护航。
服务内容
检验单项
| 服务货号 | 检测项目 | 检验方法 | 检验描述 | 样品要求 | 交付周期 (工作日) |
交付物 |
|---|---|---|---|---|---|---|
| DT001 | 基因组滴度 | ddPCR | 采用ddPCR对AAV样品进行基因组滴度检测。 | 提供预计滴度范围、引物探针序列,单次检验样品量>20 μL | 7 | 交付检验报告 |
| DT002 | 衣壳滴度 | ELISA | 采用ELISA针对AAV衣壳颗粒数进行检测。 | 提供AAV血清型、样品保存液2 mL,样品保存液的成份和pH,单次检验样品量>200 μL | 7 (试剂盒采购到位后) |
交付检验报告 |
| DT003 | 感染滴度 | TCID50 | 采用梯度稀释AAV感染细胞并通过qPCR进行检测 | 提供基因组滴度或者预计滴度范围,单次检验样品量>20 μL | 21 | 交付检验报告 |
| DT004 | 衣壳蛋白鉴别及纯度 | SDS-PAGE | 采用SDS-PAGE电泳并进行考马斯蓝染色 | 样品滴度>5E+12 vg/mL,单次检验样品量>20 μL | 7 | 交付检验报告 |
| DT005 | 衣壳蛋白纯度 | CE-SDS | SDS变形后通过毛细管电泳进行检测AAV纯度及VP1、VP2、VP3迁移率及比例 | 样品滴度>1E+13 vg/mL,单次检验样品量>20 μL | 7 | 交付检验报告 |
| DT006 | AAV纯度及空壳率 | AEX-HPLC | 采用AEC-HPLC获取AAV纯度和空壳率信息 | 样品滴度>1E+12 vg/mL,样品保存溶液2 mL,单次检验样品量>50 μL | 7 | 交付检验报告 |
| DT007 | AAV纯度及聚集 | SEC-HPLC | 采用SEC-HPLC获取AAV纯度和聚集程度信息 | 样品滴度>1E+12 vg/mL,单次检验样品量>50 μL | 7 | 交付检验报告 |
| DT008 | AAV衣壳肽图分析 | LC-MS | 通过将AAV裂解后,将AAV衣壳蛋白酶切消化成为多肽后通过HPLC-MS/MS进行检测,确保AAV的完整序列覆盖 | 基因组滴度>1E+13 vg/mL,需提供样品保存溶液的成份比例,单次检验样品量>500 μL | 21 | 交付分析报告 |
| DT009 | AAV衣壳完整蛋白分子量及比例分析 | LC-MS | 通过将AAV裂解后通过RP-HPLC-MS确定AAV衣壳结构蛋白的分子量,并提供不同结构蛋白的比例信息。对于部分血清型,提供变异体信息。 | 基因组滴度>1E+13 vg/mL,需提供样品保存溶液的成份比例,单次检验样品量>100 μL | 21 | 交付分析报告 |
| DT010 | 293宿主细胞DNA残留 | qPCR | 采用qPCR检测宿主HEK293细胞DNA残留 | 提供基因组滴度,单次检验样品量>50 μL | 7 | 交付检验报告 |
| DT011 | 293宿主细胞DNA片段大小分布 | qPCR、CE | 采用qPCR或者CE检测宿主HEK293细胞DNA不同大小片段的分布 | 提供基因组滴度,单次检验样品量>50 μL | 7 | 交付分析报告 |
| DT012 | 质粒DNA残留 | ddPCR | 采用ddPCR检测AAV中质粒DNA片段的残留量 | 提供基因组滴度,单次检验样品量>50 μL | 7 | 交付检验报告 |
| DT013 | 宿主细胞E1A残留 | ddPCR | 采用ddPCR检测AAV中E1A片段的残留量 | 提供基因组滴度,单次检验样品量>50 μL | 7 | 交付检验报告 |
| DT014 | 宿主细胞蛋白残留 | ELISA | 基于ELISA的检测 | 提供样品保存液2 mL,样品保存液成份、pH值,单次检验样品量>100 μL | 7 | 交付检验报告 |
| DT015 | 牛血清白蛋白残留 | ELISA | 基于ELISA的检测 | 提供样品保存液 2mL,样品保存液成份、pH值,单次检验样品量>200 μL | 7 | 交付检验报告 |
| DT016 | 核酸酶残留 | ELISA | 基于ELISA的检测 | 提供样品保存液2 mL,样品保存液成份、pH值,单次检验样品量>200 μL | 7 | 交付检验报告 |
| DT017 | 亲和配基残留 | ELISA | 基于ELISA的检测 | 提供样品保存液2 mL,样品保存液成份、pH值,单次检验样品量>200 μL | 7 | 交付检验报告 |
| DT018 | PEI残留 | HPLC | 基于HPLC的检测 | 提供样品保存液2 mL,单次检验样品量>100 μL | 7 | 交付检验报告 |
| DT019 | Tween20残留 | HPLC | 基于HPLC的检测 | 提供样品保存液2 mL,单次检验样品量>100 μL | 7 | 交付检验报告 |
| DT020 | TritonX100残留 | HPLC | 基于HPLC的检测 | 提供样品保存液2 mL,单次检验样品量>100 μL | 7 | 交付检验报告 |
| DT021 | 碘克沙醇残留 | HPLC | 基于HPLC的检测 | 提供样品保存液2 mL,单次检验样品量>100 μL | 7 | 交付检验报告 |
| DT022 | 泊洛沙姆188含量 | HPLC | 基于HPLC的检测 | 提供样品保存液2 mL,提供泊洛沙姆含量范围,单次检验样品量>100 μL | 7 | 交付检验报告 |
| DT023 | rcAAV检查 | 基于细胞培养的rcAAV检测 | 基于细胞培养的分析检测 | 提供AAV血清型和样品的REP序列,样品滴度>1E+12 vg/mL,单次检验样品量>50 μL | 30 | 交付检验报告 |
| DT024 | AAV基因组完整性 | CE | 基于毛细管电泳的分析 | 样品滴度>1E+13 vg/mL,提供基因组滴度和基因组总长,单次检验样品量>50 μL, | 7 | 交付分析报告 |
| DT025 | AAV基因组序列分析 | TGS | 基于第三代测序的分析 | 样品总量>5E+12 vg,单次检验样品量>500 μL, | 40 | 交付分析报告 |
| DT026 | 空壳率 | AUC | 采用AUC进行空壳率分析 | 样品滴度>5E+12 vg/mL,单次检验样品量>1 mL,样品保存液10 mL,提供AAV血清型,保存液背景信息(粘度和密度/直接提供溶液配制方法) | 7 | 交付检验报告 |
分析方法学验证
| 服务货号 | 检测项目 | 检验描述 | 样品要求 | 交付周期(工作日) | 交付物 |
|---|---|---|---|---|---|
| DV001 | 分析方法开发/验证:基因组滴度 | 针对GOI设置基因组滴度方法并进行方法的开发与验证 | 提供预计滴度范围、引物探针序列,样品量>2 mL | 30 | 交付分析方法开发报告、验证报告 |
| DV002 | 分析方法开发/验证:感染滴度 | 针对GOI设置TCID50方法并进行方法的开发与验证 | 提供基因组滴度或者预计滴度范围,提供引物探针序列,样品量>2 mL | 50 | 交付分析方法开发报告、验证报告 |
| DV003 | 分析方法开发/验证:rcAAV检查 | rcAAV检查的方法学开发、验证 | 提供AAV血清型和样品的REP序列,样品滴度>1E+12 vg/mL,样品量>2 mL | 50 | 交付分析方法开发报告、验证报告 |
| DV004 | 分析方法开发/验证:衣壳分析 | AAV衣壳分析(AUC)的方法学开发、验证 | 样品滴度>5E+12 vg/mL,样品量>5 mL,样品保存液10 mL,提供AAV血清型,保存液背景信息(粘度和密度/直接提供溶液配制方法) | 30 | 交付分析方法开发报告、验证报告 |
| DV005 | 分析方法开发/验证:衣壳分析 | AAV衣壳分析(AEX-HPLC)的方法学开发、验证 | 样品滴度>5E+12 vg/mL,样品量>2 mL,样品保存液5 mL,提供AAV血清型,保存液背景信息 | 30 | 交付分析方法开发报告、验证报告 |
| DV006 | 分析方法开发/验证:AAV基因表达量 | AAV基因组表达量的分析方法开发、验证 | 按照方案书沟通提供 | >30 | 交付分析方法开发报告、验证报告 |
| DV007 | 分析方法开发/验证:AAV生物学活性 | AAV生物学活性的分析方法开发、验证 | 按照方案书沟通提供 | TBD | 交付分析方法开发报告、验证报告 |
| DV008 | 分析方法确认:无菌检查 | 按照Ch.P 1101或者USP31-71进行无菌检查方法学确认 | 按照方案书沟通提供 | 30 | 交付分析方法确认报告 |
AAV放行检验与验证
| 类别 | 检测项目 | 检验方法 |
|---|---|---|
| 性状 | 外观 | 灯检法 |
| 可见异物 | 灯检法 | |
| 不溶性微粒 | 电阻法 | |
| 装量 | 容量法 | |
| 理化性质 | pH | 电位法 |
| 渗透压摩尔浓度 | 冰点法 | |
| 鉴别 | 特征序列鉴定 | 一代测序、三代测序、PCR |
| 衣壳蛋白鉴别及纯度 | SDS-PAGE、毛细管电泳、ELISA、HPLC MS | |
| 纯度 | UV纯度 | UV |
| AAV纯度 | AEX-HPLC | |
| 空壳率 | AUC、AEX HPLC、SEC MALS、cyroTEM、TEM | |
| 聚集 | SEC-HPLC、DLS | |
| 效价/滴度 | 基因组滴度 | qPCR、ddPCR |
| 衣壳滴度 | ELISA | |
| 效价-感染性 | TCID50或其他感染滴度检测方法 | |
| 效价-基因表达 | 基于细胞的体外mRNA表达或蛋白表达(qPCR、ELISA、Western blot) | |
| 效价活性 | 基于细胞的体外生物学活性、动物实验 | |
| 杂质 | 宿主细胞DNA残留 | qPCR、ddPCR |
| 残留DNA片段大小分布 | qPCR、毛细管电泳 | |
| 宿主细胞蛋白残留 | ELISA、HPLC-MS | |
| 宿主细胞E1A残留 | qPCR、ddPCR | |
| 质粒DNA残留 | qPCR、ddPCR | |
| 牛血清白蛋白残留 | ELISA | |
| 核酸酶残留 | ELISA | |
| 亲和配基残留 | ELISA | |
| 碘克沙醇残留 | HPLC | |
| 转染试剂残留 | HPLC | |
| 吐温20残留 | HPLC | |
| TritonX100残留 | HPLC | |
| 安全性 | 无菌检查 | 薄膜过滤法 |
| 细菌内毒素 | 凝胶法、显色基质法 | |
| 支原体检查 | 培养法、DNA染色法、qPCR | |
| 复制型AAV(rcAAV) | 基于细胞培养的rcAAV检测 | |
| 异常毒性 | 动物实验 |
质粒放行检验与验证
| 类别 | 检测项目 | 检验方法 |
|---|---|---|
| 性状 | 外观 | 灯检法 |
| 理化性质 | pH | pH值测定法 |
| 鉴别 | 质粒限制性酶切图谱 | 凝胶电泳法 |
| 质粒序列鉴定 | 一代测序 | |
| 纯度 | 质粒浓度 | UV |
| 质粒纯度 | UV | |
| DNA同质性(超螺旋比例) | HPLC | |
| 残留 | 宿主蛋白残留(大肠杆菌) | ELISA |
| 宿主DNA残留(大肠杆菌) | qPCR | |
| 卡那霉素残留 | ELISA | |
| 大肠杆菌RNA残留 | qPCR、凝胶电泳法 | |
| 安全性 | 无菌检查 | 薄膜过滤法 |
| 细菌内毒素 | 凝胶法、显色基质法 |
特殊样品检验
| 样品描述 | 样品类型 | 检测套餐 | 检验项目 | 检验描述 | 样品要求 | 检验周期 (工作日) |
|---|---|---|---|---|---|---|
| 未知的AAV样品进行初步的测试,了解样品的大概情况;或者样品的杂质复杂。 | AAV | A | 衣壳蛋白鉴别及纯度<SDS-PAGE> | 对样品进行蛋白情况进行分析 | 样品滴度>5E+12 vg/mL,样品量>20 μL | 10 |
| UV纯度 | 对样品的核酸、蛋白浓度进行初步分析 | 提供样品保存液1 mL,样品量>10 μL | ||||
| DLS | 初步了解样品的滴度、聚集 | 样品保存液1 mL,提供血清型,目的基因长度,样品溶液碘克沙醇残留量需<0.01%,样品量>10 μL | ||||
| 基因组滴度 | 确认样品的基因组滴度 | 提供预计滴度范围、引物探针序列,样品量>20 μL | ||||
| 293宿主细胞DNA残留 | 确认样品的宿主细胞DNA残留 | 提供基因组滴度,样品量>50 μL | ||||
| 质粒DNA残留 | 确认样品的质粒DNA残留 | 提供基因组滴度,样品量>50 μL | ||||
| 已通过套餐A检验完成的样品;或者客户能提供样品的具体指标(包括基因组滴度、OD260/280比值、宿主细胞DNA残留量、宿主细胞蛋白残留量等) | AAV | B | AAV纯度及聚集<SEC-HPLC> | 采用SEC-HPLC获取AAV纯度和聚集程度信息 | 样品滴度>1E+12 vg/mL,样品量>50 μL | 7 |
| 空壳率(AUC) | 采用AUC进行空壳率分析 | 样品滴度>5E+12 vg/mL,样品保存液10 mL,提供AAV血清型,保存液背景信息(粘度和密度/直接提供溶液配制方法) | 7 | |||
| 已通过套餐B检验完成的样品;或者客户能提供样品的具体指标(包括基因组滴度、OD260/280比值、宿主细胞DNA残留量、宿主细胞蛋白残留量、空壳率等) | AAV | C | 293宿主细胞DNA分布 | 采用qPCR检测宿主HEK293细胞DNA不同大小片段的分布 | 提供基因组滴度,样品量>50 μL | 7 |
| 宿主细胞E1A残留 | 采用ddPCR检测AAV中E1A片段的残留量 | 提供基因组滴度,样品量>50 μL | 7 | |||
| 宿主细胞蛋白残留 | 基于ELISA的检测 | 提供样品保存液2 mL,样品保存液成份、pH值、样品量>100 μL | 7 | |||
| 牛血清白蛋白残留 | 基于ELISA的检测 | 提供样品保存液2 mL,样品保存液成份、pH值、样品量>200 μL | 7 | |||
| 核酸酶残留 | 基于ELISA的检测 | 提供样品保存液2 mL,样品保存液成份、pH值、样品量>200 μL | 7 | |||
| 亲和配基残留 | 基于ELISA的检测 | 提供样品保存液2 mL,样品保存液成份、pH值、样品量>200 μL | 7 | |||
| PEI残留 | 基于HPLC的检测 | 提供样品保存液2 mL,样品量>100 μL | 7 | |||
| Tween20残留 | 基于HPLC的检测 | 提供样品保存液2 mL,样品量>100 μL | 7 | |||
| TritonX100残留 | 基于HPLC的检测 | 提供样品保存液2 mL,样品量>100 μL | 7 | |||
| 碘克沙醇残留 | 基于HPLC的检测 | 提供样品保存液2 mL,样品量>100 μL | 7 | |||
| 泊洛沙姆188含量 | 基于HPLC的检测 | 提供样品保存液2 mL,提供泊洛沙姆含量范围,样品量>100 μL | 7 | |||
| rcAAV检查 | 基于细胞感染的分析检测 | 提供AAV血清型和样品的REP序列,样品滴度>1E+12 vg/mL,样品量>50 μL | 30 |
成药性研究
- 药物发现不同阶段的成药性评估
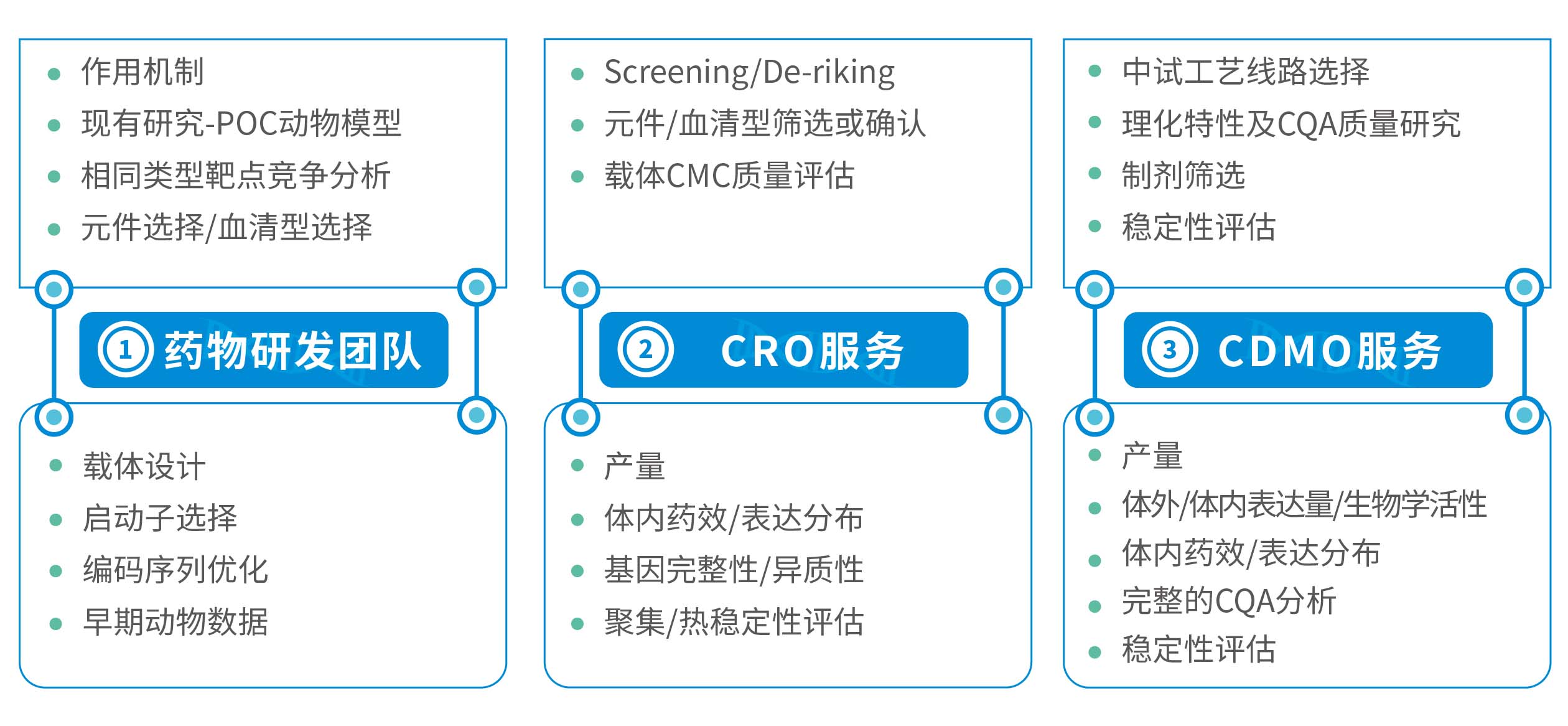
- 派真成药性分析平台

分析方法案例
针对AAV的感染滴度(TCID50)测试方法,派真生物通过建立均一的细胞库和辅助病毒库,同时对细胞培养板、培养时间、qPCR反应体系等因素进行摸索和优化,提高TCID50方法的可重复性、稳定性和敏感性,并把双人操作的CV%值提高至40%以内。派真生物优化的感染滴度(TCID50)测试方法通过了方法学验证,包括专属性、精密度、检测限和线性范围,结果表明本方法是一种高效、准确、快速的检验AAV病毒感染滴度的方法。
- 制备均一标定的辅助病毒库
- 建立均一的检定用细胞工作库
- 基于qPCR反应体系的优化
| 精密度验证结果 | |||
|---|---|---|---|
| 样品名称 | 感染滴度(IU/mL) | 6份感染滴度CV% | 12份感染滴度CV% |
| 重复性样品-1 | 2.14×1010 | 20.68 | 32.60 |
| 重复性样品-2 | 1.20×1010 | ||
| 重复性样品-3 | 1.46×1010 | ||
| 重复性样品-4 | 1.46×1010 | ||
| 重复性样品-5 | 1.46×1010 | ||
| 重复性样品-6 | 1.46×1010 | ||
| 中间精密度样品-1 | 8.20×109 | 39.46 | |
| 中间精密度样品-2 | 1.46×1010 | ||
| 中间精密度样品-3 | 9.93×109 | ||
| 中间精密度样品-4 | 8.20×109 | ||
| 中间精密度样品-5 | 1.77×1010 | ||
| 中间精密度样品-6 | 6.77×109 | ||
| 专属性 | 检测限 | 线性范围 |
|---|---|---|
| 通过 | 10 copies | 4×104copies/μL~4copies/μL |
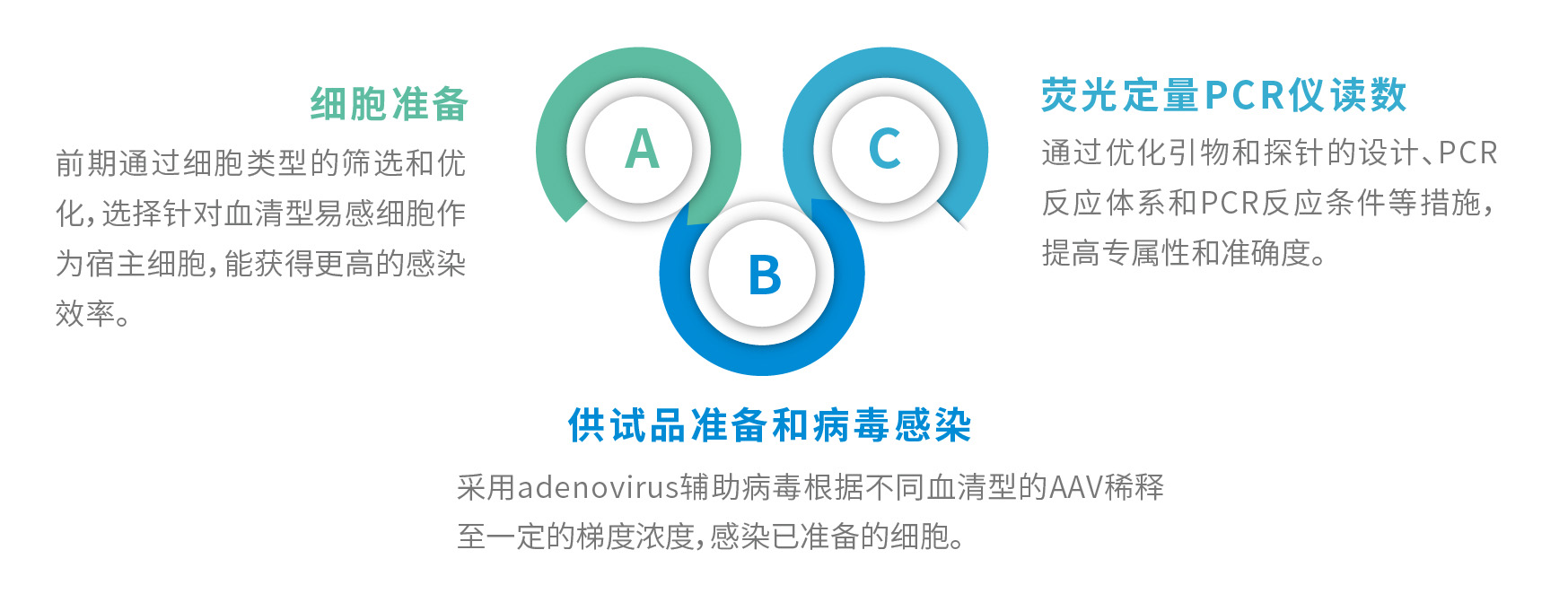
重组腺相关病毒载体(rAAV)源于非致病的野生型腺相关病毒,由于其安全性好、宿主细胞范围广、免疫源性低,在体内表达外源基因时间长等特点,被视为最有前途的基因转移载体之一,在世界范围内的基因治疗和疫苗研究中得到广泛应用。rcAAV检验是AAV药物安全性的重要指标。目前药典或文献未有可实践的复制完整型AAV检测方法,其开发难点在于需要用到经过标定的辅助病毒和野生阳性病毒,可接受标准限度低。通常是在P2实验室条件下采用检定用的wtAAV和样本在辅助病毒辅助下经过多轮感染靶细胞,并提取样品进行qPCR检测。
派真生物开发了特有的rcAAV PackRich技术,在低至5-10 IU的阳性对照病毒下仍然能检出,同时重现性和稳健性更高。
- P2实验室资质
- 检定用的易感细胞株
- 制备均一标定的辅助病毒库
- 建立均一的检定用wtAAV
- 派真特有的PackRich rcAAV富集技术,方法检出限低至5 IU
rcAAV检验原理
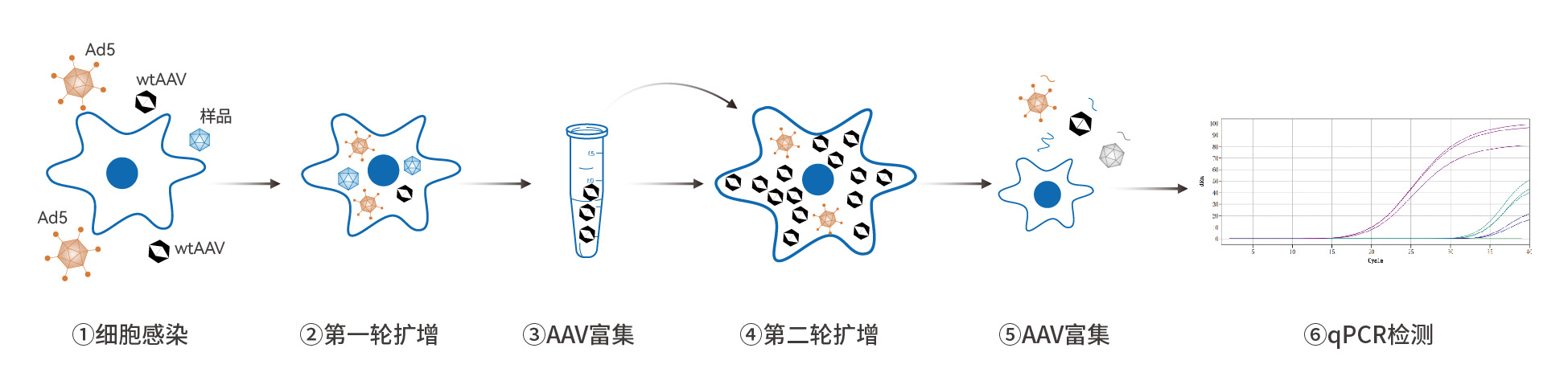
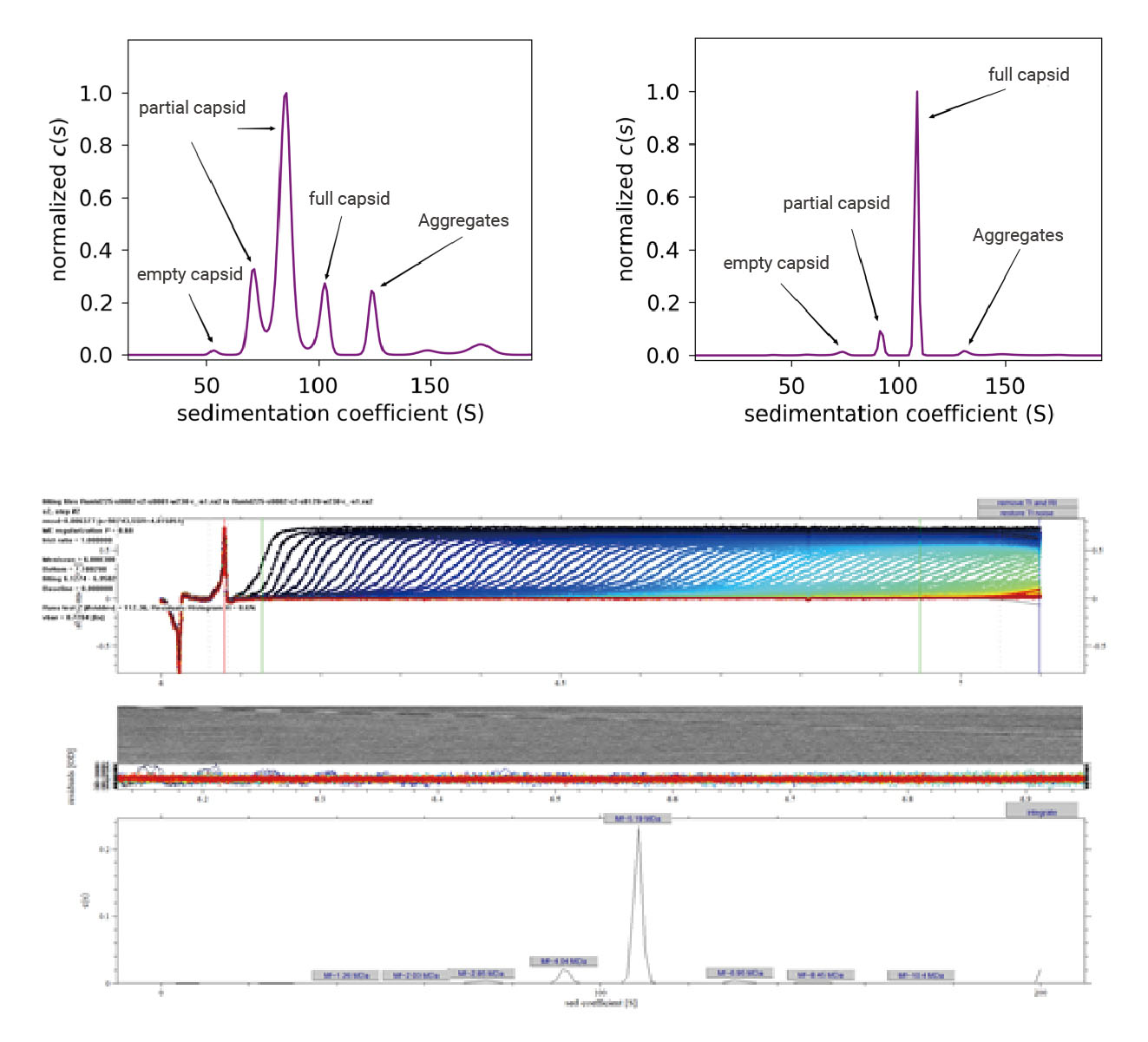
分析型超速离心技术(AUC,Analytical ultracentrifugation)通过将离心机与光学模块相结合,前者能够沉降颗粒物,后者能够检测随时间变化的沉降情况。根据物质的沉降系数、质量和密度等要素,通过超速离心将不同沉降系数的样品,先后沉降至样品池底部,在此过程中扫描记录样品分布状态,通过分析其随时间的变化过程,获得不同组分样品的沉降性质和相对比例。依据full capsid与其他病毒颗粒沉降系数的不同,可以精确测定rAAV的样品中不同类型衣壳颗粒的沉降系数和相对比例,同时可以检测中间产物、病毒载体碎片、基因组碎片、病毒聚集体等。目前已成为检测AAV空壳率的“金标准”,被业内人士广泛认可。
- 能精确表征样本中各个组分
- 具有高度可重复性
- 能从空壳病毒颗粒和实心病毒颗粒中区分出包装了部分基因组的病毒颗粒,具有其他分析方法所达不到的分辨率
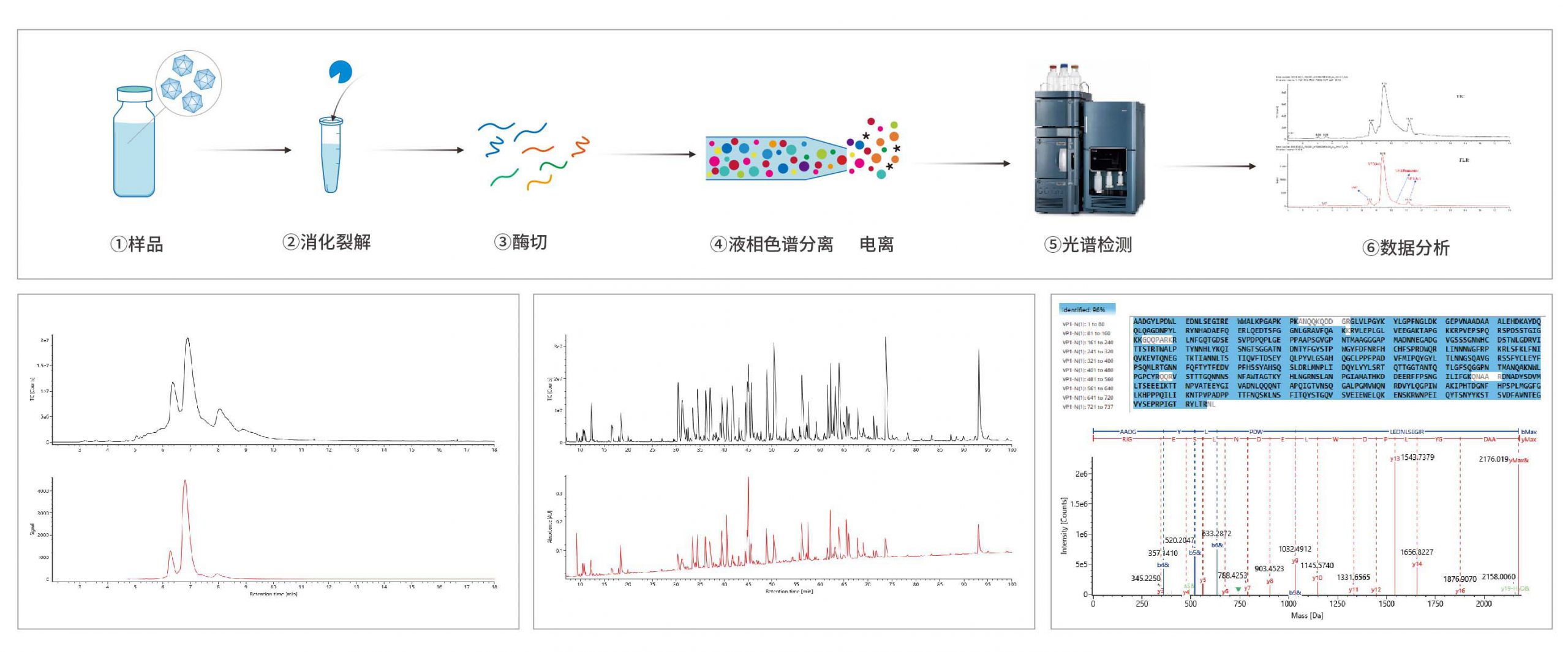
高效液相色谱质谱联用技术(HPLC-MS,liquid Chromatograph Mass Spectrometer),以高效液相色谱作为分离系统(拥有高分离度),质谱为检测系统(拥有高灵敏度)。衣壳蛋白离子化后进行检测,再经质量分析仪将离子碎片按质量数分开,能准确得出蛋白的分子量大小和肽段覆盖率的情况,准确鉴别出AAV血清型。
- AAV衣壳蛋白分子量及比例分析
- AAV衣壳肽图分析
服务优势
先进的实验设施和检验仪器
细胞培养室、效价室、无菌室和PCR实验室,均获得BLS-2生物实验室资质并且符合GMP标准;拥有多台先进的分析仪器,包括:Optima AUC分析型超速离心机、高效液相色谱仪、毛细管电泳仪、液质联用仪、数字PCR仪、荧光定量PCR仪等。

专业稳定的技术团队
技术团队博士和硕士占比超过30%,具有十五年以上检测经验,可为客户提供专业的技术需求,满足不同阶段的检验方法开发和验证的需求。与国内外多家大型药企及创新药研发公司保持合作关系,并完成多个分析订单,助力IND申报。

创新的技术平台
针对质粒和AAV质控建立60多套检验方法,同时完成分析方法学验证,并不断进行优化和改进。自主建立感染滴度(TCID50)、rcAAV检测、中和抗体检测、AAV空壳分析(AUC)、AAV血清型表征分析(LC-MS)等特色技术平台,并提供个性化的解决方案。
专业的特色检验服务
多年AAV质控经验的积累,熟悉AAV产品的特性,在GLP规范的实验室管理体系下建立成熟稳定的AAV分析技术平台,提供药物开发过程中的成药性研究、工艺开发过程中的质量研究、中试生产的质量控制等服务,满足不同研发阶段的检验需求。

安全可靠的数据保障
我们严格遵守行业标准和规定,保障客户的数据安全和隐私。我们使用最先进的数据加密和保护技术,确保客户数据不会泄露或丢失。
我们致力于为细胞与基因治疗企业提供最佳的CMC解决方案,帮助客户降低研发成本、提高研发效率,并全方位做好质量控制策略以便更好地为新药申报保驾护航。如果您需要AAV CDMO或检测质控等服务,欢迎拨打400-835-0680或者点击右侧在线咨询按钮联系我们,我们专业的团队将竭诚为您服务。
联系我们
