CRISPR系统是细菌和古菌特有一种防御系统,自2012年开始被开发和改造为新一代的基因编辑工具,其中CRISPR-Cas9已成为革命性的基因组编辑平台,被广泛应用于生物技术和医学领域。其中来自化脓链球菌的Cas9(spCas9),由于其高效和识别松弛的5′-NGG-3′ PAM序列,而得到了最广泛的应用。此外,基于spCas9的碱基编辑器(BE)还能实现对基因组DNA中单个碱基的替换。
然而,spCas9在实际临床应用中面临着一个大难题,spCas9蛋白长达1368个氨基酸,当其与sgRNA形成复合物时,已经超出了腺相关病毒(AAV)的装载能力范围(4.7kb)。这大大限制了spCas9的体内基因编辑疗法的开发。
2022年6月,吉林大学李占军教授团队、赖良学教授团队合作在 The CRISPR Journal 发表了题为:Compact Cje3Cas9 for Efficient In Vivo Genome Editing and Adenine Base Editing 的研究论文。
该研究开发了一种名为 Cje3Cas9 的新型紧凑型 Cas9,可用于体内的高效基因编辑和腺嘌呤碱基编辑。

目前,已经有一些策略可以一定程度上克服AAV对Cas9的递送难题,例如将spCas9和sgRNA分别用AAV包装并递送,以及将基于spCas9的碱基编辑器拆成两部分,用两个AAV分别递送再组装。
该项研究使用的 AAV-Cje3Cas9和AAV-8e-nCjeCas9 过表达质粒及病毒包装由派真生物提供。作为一家专注于重组腺相关病毒(rAAV)载体包装的CRO &CTDMO科技公司,派真生物致力于为基因功能以及基因治疗研究提供从质粒克隆到AAV包装的一站式解决方案,助力AAV在神经领域及眼睛、肝脏、心脏、肌肉等组织中的科学研究进展。
此外,还有研究致力于开发尺寸更小的Cas9同源物,以实现通过单个AAV的递送。例如saCas9(1053个氨基酸)、Nme1Cas9(1082个氨基酸)、Cje1Cas9(984个氨基酸)等等。
2021年6月,李占军、赖良学团队在 Molecular Therapy 期刊发表论文,在巴氏链球菌中发现并优化了名为SpaCas9的小型Cas9(1130个氨基酸)。SpaCas9可通过单个AAV递送并在体内进行有效的基因编辑。但和其他的基于Cas9的碱基编辑器(BE)一样,SpaCas9-BE无法包装到单个AAV载体中。

在众多小型Cas9中,来自空肠弯曲杆菌的Cje1Cas9仅984个氨基酸,因此特别适合使用AAV进行体内递送,更重要的是,基于Cje1Cas9的碱基编辑系统具有通过单个AAV递送的潜力。然而,Cje1Cas9需要识别非常复杂的 N3VRYAC PAM序列(V=A/C/G,R=A/G,Y=C/T),这极大地限制了其靶向基因组的范围。
因此,探索具有简单PAM序列要求的小型化CRISPR-Cas酶,以扩大对基因组的靶向范围非常重要。
在这项最新研究中,李占军、赖良学团队确定了两个CjeCas9的直系同源物,分别是Cje2Cas9和Cje3Cas9,它们的PAM序列不同于Cje1Cas9的N3VRYAC,而是更为简单的N4CYA。
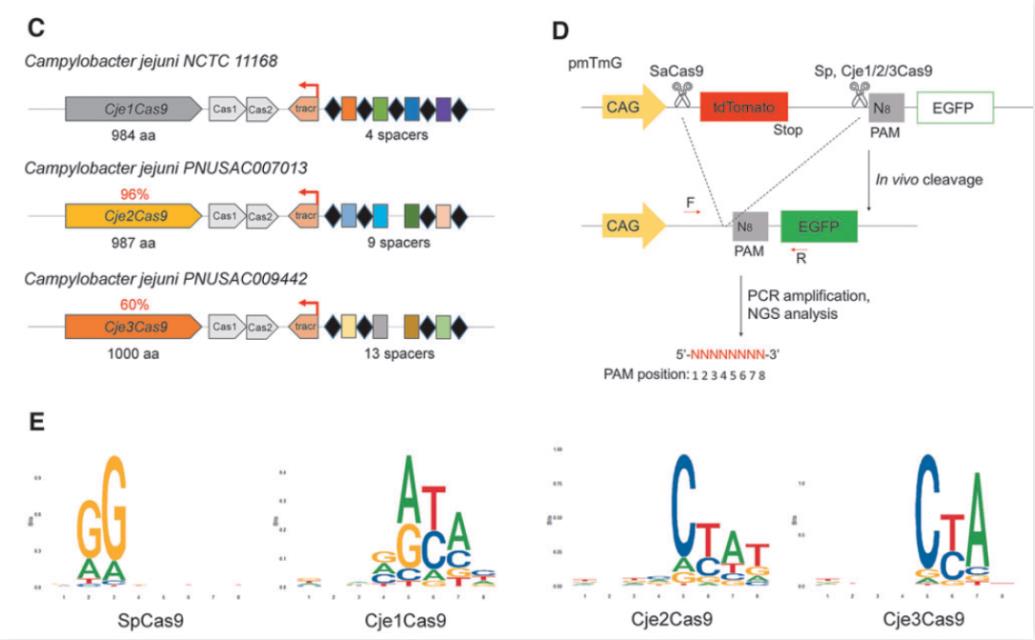
研究团队接下来进行了体外和体内的基因编辑实验,实验结果显示,它们可以在人类细胞中诱导有效的基因组编辑,而且由于简单的PAM序列要求,显著扩大了基因组靶向范围。
该项研究使用的 AAV8-SpaCas9载体由派真生物提供。作为一家专注于重组腺相关病毒(rAAV)载体包装的CRO &CTDMO科技公司,派真生物致力于为基因功能以及基因治疗研究提供从质粒克隆到AAV包装的一站式解决方案,助力AAV在神经领域及眼睛、肝脏、心脏、肌肉等组织中的科学研究进展。
此外,将Cje3Cas9与sgRNA微量注射到小鼠受精卵中后,可以有效地敲除小鼠的Tyr基因。它还能够通过单个AAV递送,有效敲除8周龄小鼠的肝脏中的Pcsk9基因,并有效降低小鼠的胆固醇水平。
更重要的是,研究团队进一步证实了,基于Cje3Cas9的碱基编辑器——8e-nCje3-ABE,能够与sgRNA一起包装到单个AAV中,并在成年小鼠肝脏中成功编辑Pcsk9基因,编辑效率高达12%。
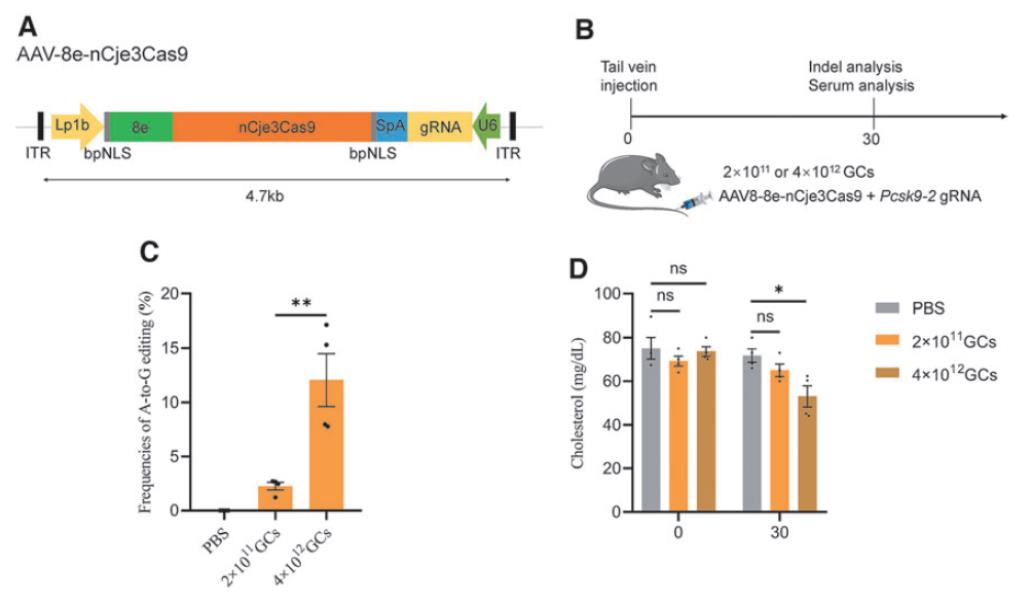
总的来说,该研究开发了紧凑型的Cas9——Cje2Cas9和Cje3Cas9,他们具有更简单的PAM序列要求,而且能够包装到单个AAV中,扩展了CRISPR-Cas9工具的基因组八项范围,具有巨大的临床治疗价值。
值得一提的是,碱基编辑技术开创者刘如谦(David Liu)团队于2022年7月28日在 Nature 子刊 Nature Biomedical Engineering 发表论文【3】,开发了一套紧凑型腺嘌呤碱基编辑器,能够使用单AAV载体递送并在肝脏、心脏、肌肉等组织中实现高效碱基编辑,编辑效率优于双AAV载体。
对人PCSK9基因(人源化小鼠)、小鼠Pcsk9基因和Angptl3的体内编辑显示,能够降低目标蛋白水平90%以上,同时血浆胆固醇和甘油三酯也显著降低。
这项研究提高了碱基编辑的治疗潜力,确立了单AAV碱基编辑器系统的优势,并提供了一套具有广泛靶向能力的单AAV腺嘌呤碱基编辑器,以支持高效的体内碱基编辑。

