
艾滋病(AIDS),即获得性免疫缺陷综合征,是一种由人类免疫缺陷病毒(HIV)感染引起的危害性极大的传染病。HIV 病毒把人体免疫系统中最重要的 CD4+T 细胞作为主要攻击目标,大量破坏该细胞,经过数年、甚至长达10年或更长的潜伏期后发展成艾滋病病人,使人体丧失免疫功能,因抵抗力极度下降会出现多种感染,后期常常发生恶性肿瘤,以至全身衰竭而死亡。
在过去的几十年里,何大一等人提出的“鸡尾酒疗法”等联合治疗方案使得艾滋病成为了一种相对可控的慢性疾病,HIV 感染患者的存活时间和生活质量也得到了极大的改善。然而,这些疗法只能抑制患者体内的 HIV 病毒,而不能彻底清除,因此也就无法治愈。
据联合国艾滋病规划署数据,目前全球范围内现存HIV携带者和艾滋病患者人数高达3800万人,且数量仍在快速增长中。
近日,以色列特拉维夫大学的研究人员在 Nature Biotechnology 期刊上发表了题为:In vivo engineered B cells secrete high titers of broadly neutralizing anti-HIV antibodies in mice 的研究论文。
该研究使用两种腺相关病毒载体(AAV)同时递送 CRISPR-Cas9 基因编辑系统和靶向免疫球蛋白基因的修复模板,直接编辑小鼠内源 B 细胞的免疫球蛋白基因位点,有效地在体内修饰 B 细胞,使之能产生针对 HIV 病毒的中和抗体,让一次性注射治疗艾滋病成为可能。

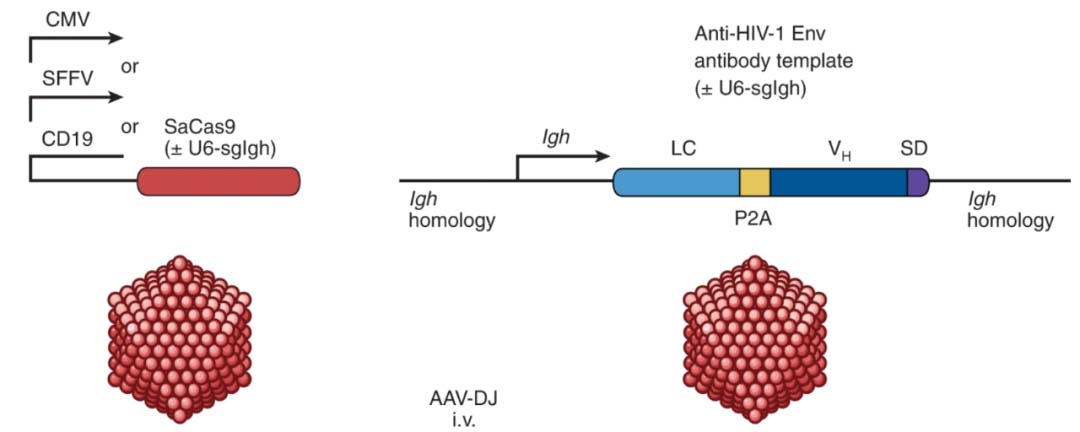
两种重组腺相关病毒递送CRISPR-Cas9基因编辑系统和HDRT
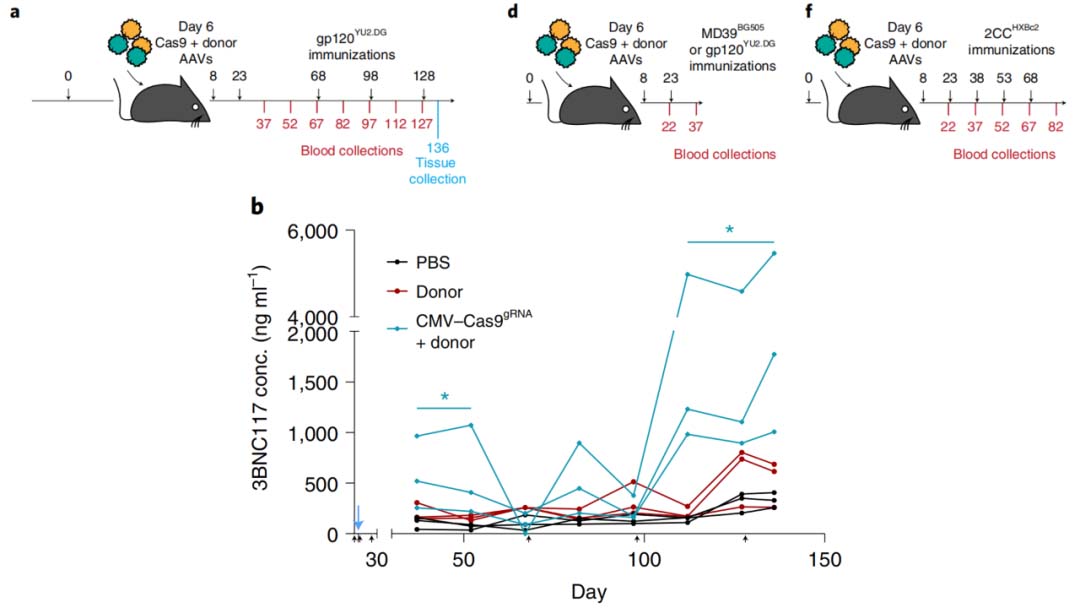
两种重组腺相关病毒递送CRISPR-Cas9基因编辑系统和HDRT
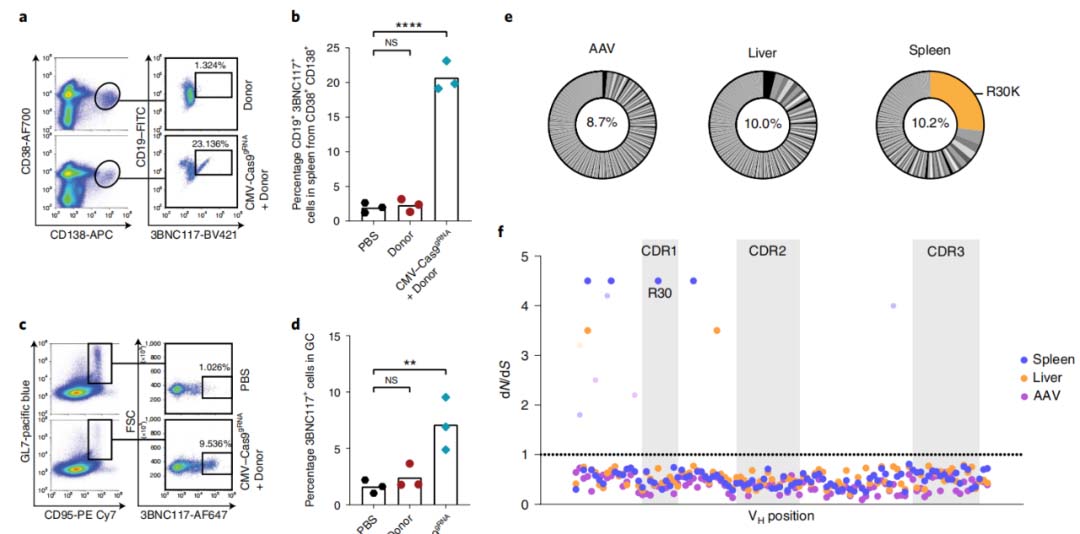
注射AAV后130天,在免疫小鼠的淋巴组织中发现了体内工程B细胞
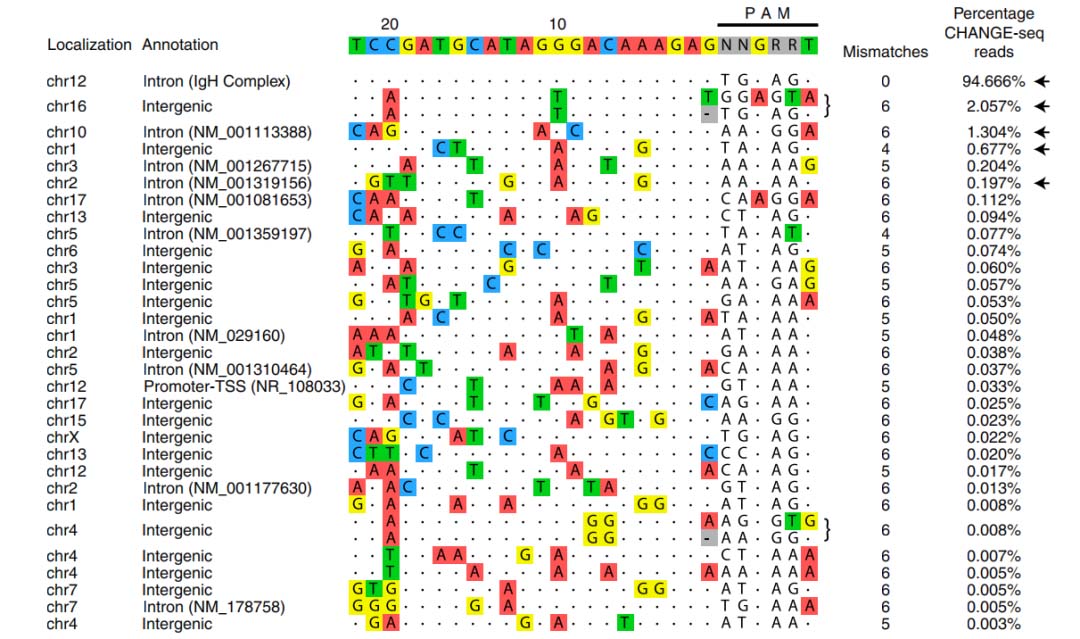
脱靶切割分析显示了较高的安全性
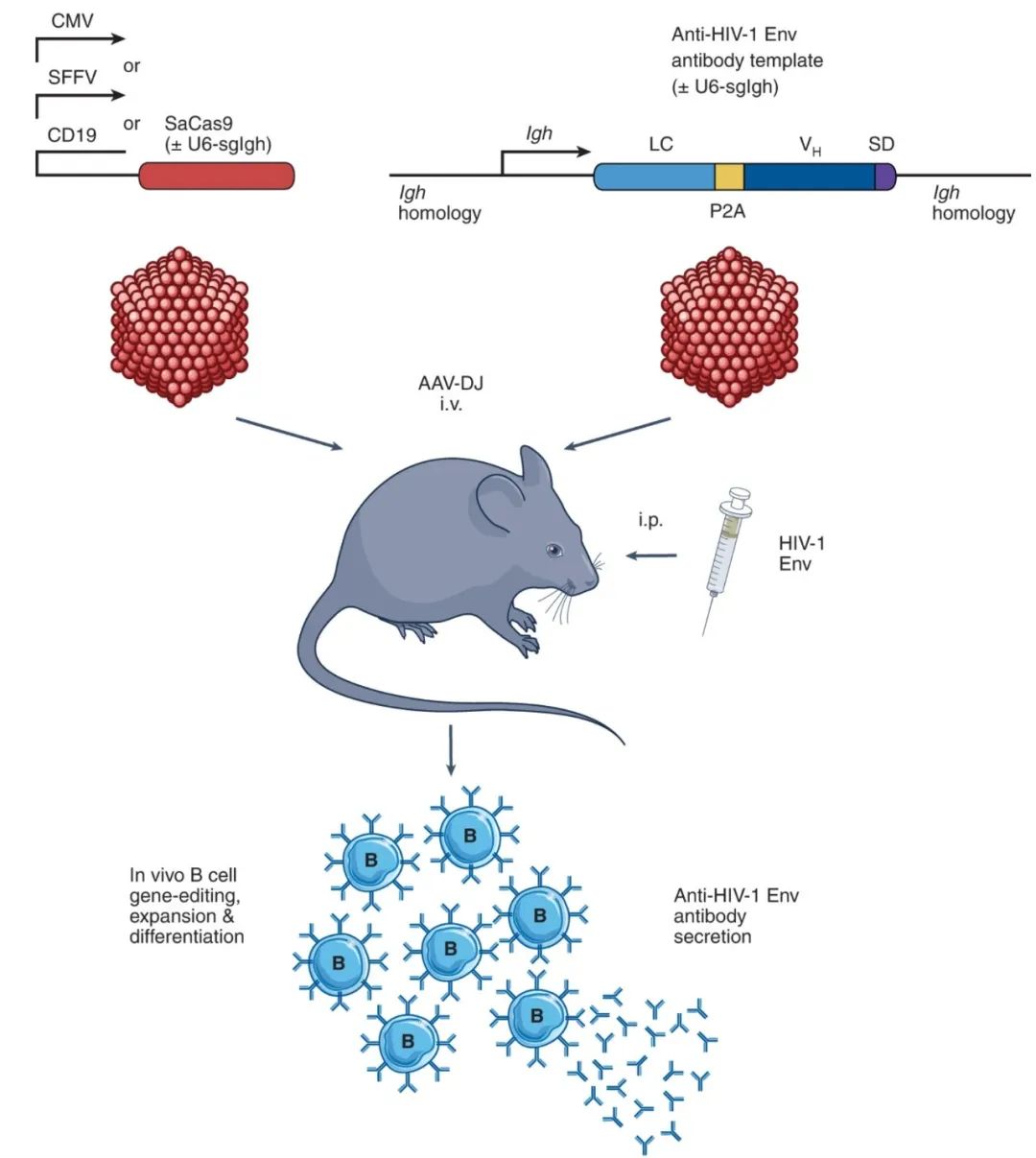
研究模式图
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。

