
AAV载体的原理
腺相关病毒(Adeno-Associated Virus,AAV)载体是一种被广泛用于基因递送的工具,其主要功能是将特定的基因载荷传递至目标细胞和组织中。AAV载体具有一系列突出的特点,包括低免疫原性、广泛的细胞感染能力以及稳定的基因表达水平。
AAV基因组结构
AAV属于小型非包膜DNA病毒,其基因组大小约为4.7 kb。AAV基因组的两端分别存在反向末端重复序列(Inverted Terminal Repeat,ITR),这些序列在病毒生命周期中起着重要作用,包括病毒复制和包装等关键过程。AAV基因组编码有Rep蛋白和Cap蛋白,这两类蛋白在基因组复制、病毒组装和包装等步骤中扮演关键角色。
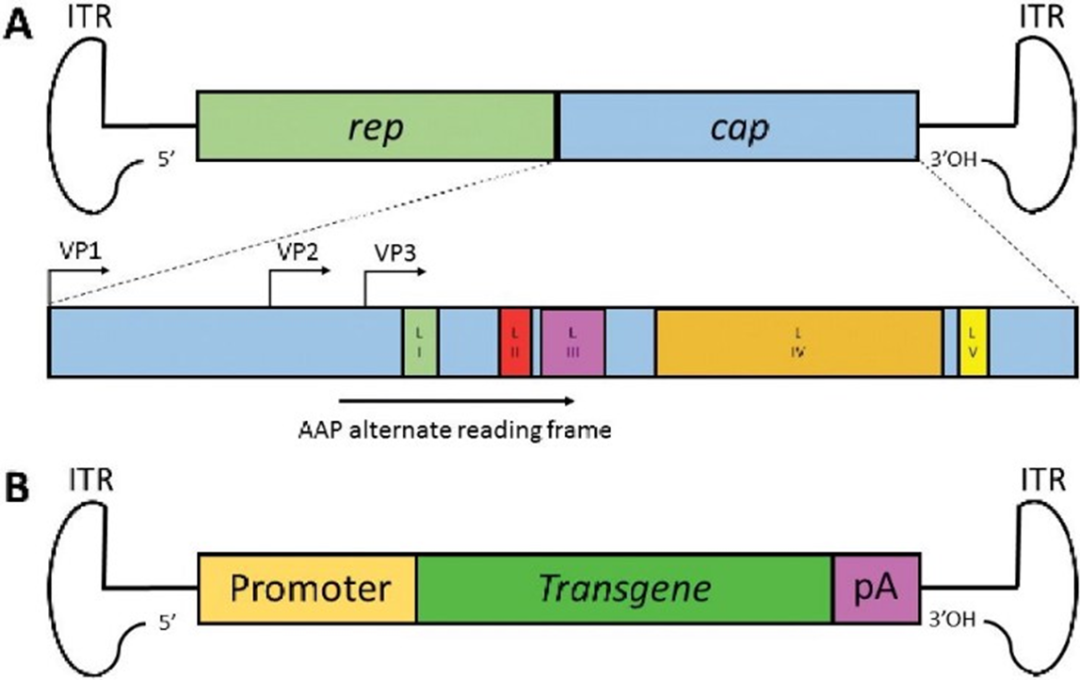
AAV载体构建
制备AAV载体的常见策略是将目标基因序列插入到AAV基因组编码区域,同时保留两端的ITR序列。通过这样的构建,目标基因的表达将受到AAV生物学机制的精细调控,从而实现在目标细胞中的稳定表达。
表达Cap和Rep蛋白
为了支持AAV载体的复制和包装,研究人员需要同时提供CAP和REP蛋白。CAP蛋白作为外壳蛋白参与病毒颗粒的包装,而REP蛋白则参与基因组复制和调控等关键过程。通常,CAP和REP蛋白会通过共转染方式被表达在目标细胞中。
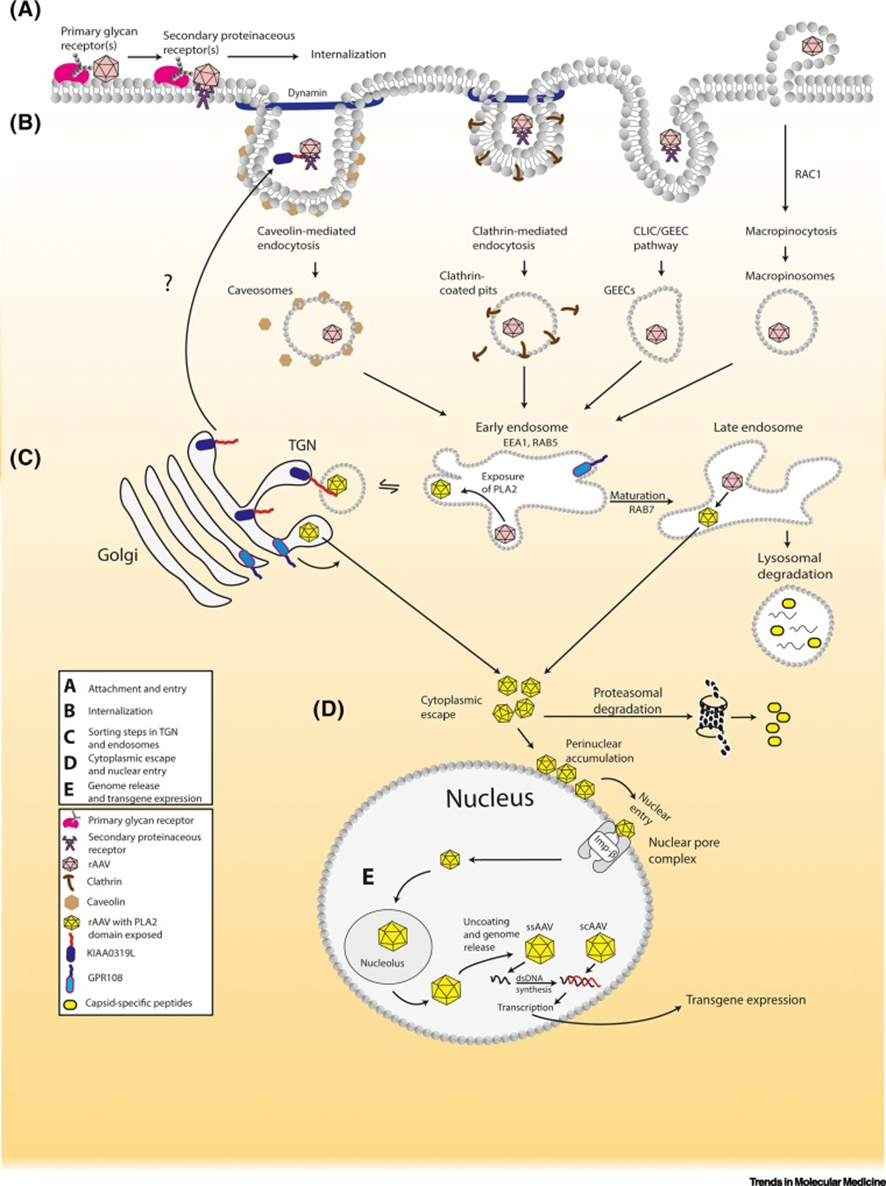
AAV载体的生命周期
细胞内生命周期
一旦AAV载体进入目标细胞,其基因组将被转录成mRNA,并随后通过细胞的翻译机制产生CAP和REP蛋白。这些蛋白协同作用促进AAV基因组的复制和组装,形成成熟的病毒颗粒。同时,目标基因也会通过细胞机制进行表达,从而实现稳定的基因表达。
基因递送
在经历复制和包装过程后,AAV载体将生成成熟的病毒颗粒,这些颗粒携带着目标基因。这些病毒颗粒可以被细胞释放到外部环境,随后再感染其他细胞。目标基因将在被感染细胞中表达,从而实现基因递送的目标。
AAV载体的制备
制备腺相关病毒(AAV)载体通常需要一系列实验步骤和技术,以下是一般的制备过程概述:
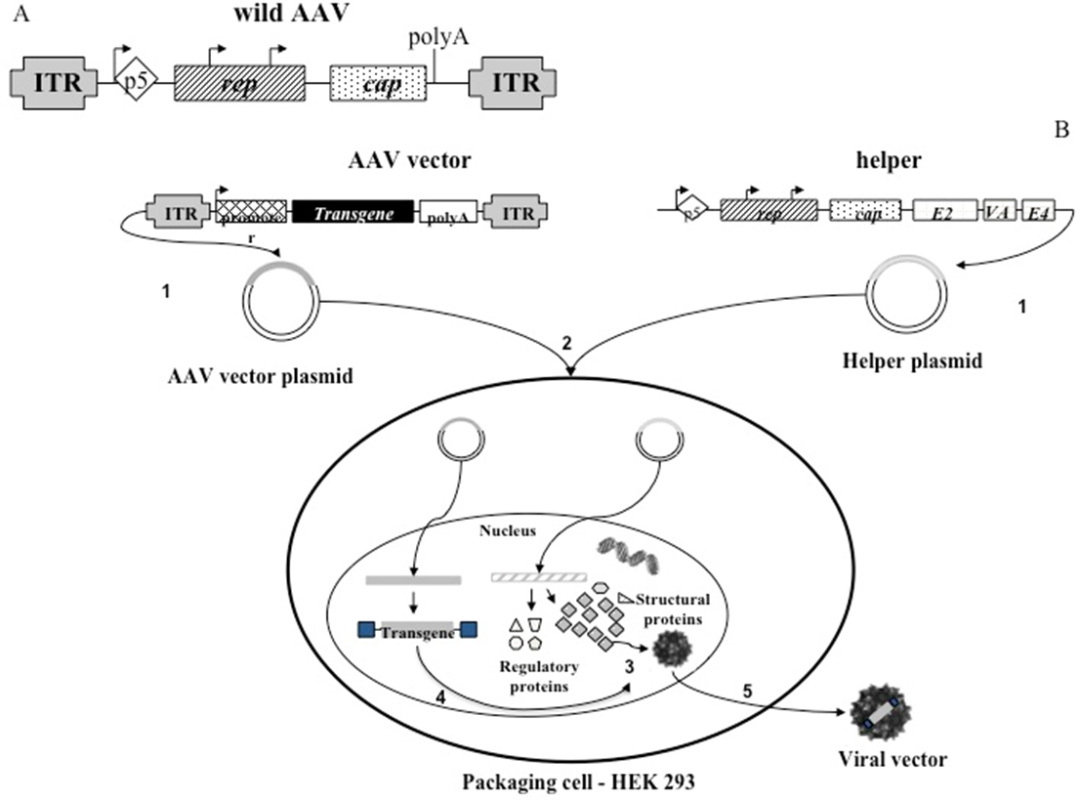
载体构建
共转染细胞:通常使用三质粒共转染法,将含有AAV载体基因组的质粒、表达CAP和REP蛋白的质粒以及腺病毒共基因质粒一同转染到细胞中。这样,CAP和REP蛋白将协助AAV载体的复制和包装。
病毒提取:在适当的时间点,收集转染细胞培养液,并进行细胞破裂和病毒颗粒提取。这些病毒颗粒含有目的基因,可以用于后续的基因递送实验。
病毒纯化:从细胞提取物中纯化AAV颗粒,通常采用离心、密度梯度离心等技术来分离和富集AAV病毒颗粒。
病毒滴度测定:测定病毒颗粒的滴度,即单位体积中含有多少个感染性AAV颗粒。这将帮助在后续实验中确定合适的病毒用量。
AAV载体的优势
高安全性和极低免疫原性
野生型AAV是一种天然缺陷病毒,不与任何已知疾病相关。此外,重组AAV在基因治疗中并不整合到宿主细胞基因组中,从而降低了插入相关的风险。由于其非致病性和低免疫原性,AAV被认为是相对安全的基因治疗载体。
感染宿主范围广
AAV具有广泛的细胞感染能力,不仅可以感染分裂细胞,还可以感染非分裂细胞,这使其在基因治疗中具有灵活的应用范围。
高组织嗜性
AAV有多个血清型,每种血清型都具有特定的组织嗜性,可以选择性地感染不同的组织或器官。这种组织特异性使得基因治疗可以更准确地针对特定的疾病部位。
感染扩散能力强、特异性强
AAV具有较小的体积和高滴度,这使得它在体内具有较强的感染扩散能力。同时,AAV具有高度的组织特异性,可以针对特定组织或细胞类型实现特异性感染,减少了对非目标组织的影响。
体内表达时间长
AAV具有较高的滴度,可以在体内稳定地表达基因,使基因治疗效果能够持续一段较长的时间。
关于派真
作为一家专注于AAV 技术十余年,深耕基因治疗领域的CRO&CDMO,派真生物可提供从载体设计、构建到 AAV、慢病毒和 mRNA 服务的一站式解决方案。凭借深厚的技术实力、卓越的运营管理和高标准的服务交付,我们为全球客户提供一站式CMC解决方案,包括从早期概念验证、成药性评估到IIT、IND及BLA的各个阶段。
凭借我们独立知识产权的π-alphaTM 293 细胞AAV高产技术平台,我们能将AAV产量提高多至10倍,每批次产量可达1×10¹⁷vg,以满足多样化的商业化和临床项目需求。此外,我们定制化的mRNA和脂质纳米颗粒(LNP)产品及服务覆盖药物和疫苗开发的各个阶段,从研发到符合GMP的生产,提供端到端的一站式解决方案。

